Elavil 10mg, 25mg, 50mg Amitriptyline Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Elavil y cómo se usa?
Elavil 10 mg es un medicamento recetado que se usa para tratar los síntomas de ansiedad o agitación con depresión y esquizofrenia con depresión. Elavil se puede usar solo o con otros medicamentos.
Elavil pertenece a una clase de medicamentos llamados Combos Psicoterapéuticos.
No se sabe si Elavil es seguro y efectivo en niños.
¿Cuáles son los posibles efectos secundarios de Elavil 25mg?
Elavil puede causar efectos secundarios graves que incluyen:
- moretones o sangrado fácil,
- acidez estomacal persistente,
- sacudida,
- expresiones faciales como máscaras,
- espasmos musculares,
- dolor de estómago severo,
- disminución del deseo sexual,
- senos agrandados o dolorosos,
- taburetes negros,
- vómito que parece café molido,
- mareos severos,
- desmayo,
- convulsiones,
- dolor, enrojecimiento o hinchazón de los ojos,
- cambios de visión,
- fiebre,
- rigidez muscular,
- confusión severa,
- sudoración, y
- latidos del corazón rápidos o irregulares
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Elavil incluyen:
- somnolencia,
- mareo,
- boca seca,
- visión borrosa,
- estreñimiento,
- aumento de peso, y
- dificultad para orinar
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Elavil. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
Medicamentos suicidas y antidepresivos
Los antidepresivos aumentaron el riesgo de pensamientos y conductas suicidas (tendencia suicida) en comparación con placebo en niños, adolescentes y adultos jóvenes en estudios a corto plazo de trastorno depresivo mayor (TDM) y otros trastornos psiquiátricos. Cualquiera que esté considerando el uso de tabletas de clorhidrato de amitriptilina o cualquier otro antidepresivo en un niño, adolescente o adulto joven debe sopesar este riesgo con la necesidad clínica. Los estudios a corto plazo no mostraron un aumento en el riesgo de tendencias suicidas con antidepresivos en comparación con placebo en adultos mayores de 24 años; hubo una reducción del riesgo con los antidepresivos en comparación con el placebo en adultos de 65 años o más. La depresión y ciertos otros trastornos psiquiátricos están asociados con aumentos en el riesgo de suicidio. Los pacientes de todas las edades que comienzan con la terapia antidepresiva deben ser monitoreados apropiadamente y observados de cerca para detectar empeoramiento clínico, tendencias suicidas o cambios inusuales en el comportamiento. Se debe advertir a las familias y cuidadores de la necesidad de una estrecha observación y comunicación con el prescriptor. Las tabletas de clorhidrato de amitriptilina no están aprobadas para su uso en pacientes pediátricos (ver ADVERTENCIAS: Empeoramiento clínico y riesgo de suicidio, INFORMACIÓN PARA EL PACIENTE y PRECAUCIONES: Uso pediátrico).
DESCRIPCIÓN
La amitriptilina HCl es clorhidrato de 3-(10,11-dihidro-5H-dibenzo [a,d] ciclohepteno-5-ilideno)-N,N-dimetil-1-propanamina. Su fórmula empírica es C20H23N•HCl, y su fórmula estructural es:
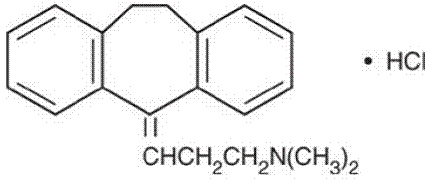
La amitriptilina HCl, un derivado del dibenzocicloheptadieno, tiene un peso molecular de 313,87. Es un compuesto blanco, inodoro y cristalino que es fácilmente soluble en agua.
El clorhidrato de amitriptilina se suministra en comprimidos de 10 mg, 25 mg, 50 mg, 75 mg, 100 mg o 150 mg. Cada tableta contiene los siguientes ingredientes inactivos: dióxido de silicio coloidal, hipromelosa, lactosa monohidrato, estearato de magnesio, celulosa microcristalina, polietilenglicol, polisorbato, glicolato de almidón de sodio y dióxido de titanio. Las tabletas de 10 mg también contienen laca azul #1 FD&C. Las tabletas de 25 mg también contienen laca amarilla n.° 10 de D&C y laca azul n.° 2 de FD&C. Los comprimidos de 50 mg también contienen óxido de hierro negro sintético, óxido de hierro rojo sintético y óxido de hierro amarillo sintético. Las tabletas de 75 mg también contienen laca amarilla #6 FD&C. Las tabletas de 100 mg también contienen laca roja n.° 33 de D&C y laca roja n.° 40 de FD&C. Las tabletas de 150 mg también contienen laca azul #2 FD&C y laca amarilla #6 FD&C.
INDICACIONES
Para el alivio de los síntomas de la depresión. Es más probable que se alivie la depresión endógena que otros estados depresivos.
DOSIFICACIÓN Y ADMINISTRACIÓN
La dosis debe iniciarse a un nivel bajo y aumentarse gradualmente, observando cuidadosamente la respuesta clínica y cualquier evidencia de intolerancia.
Dosis inicial para adultos
Para pacientes ambulatorios, 75 mg de clorhidrato de amitriptilina al día en dosis divididas suele ser satisfactorio. Si es necesario, esto se puede aumentar a un total de 150 mg por día. Los aumentos se realizan preferentemente en las dosis de la tarde y/o la hora de acostarse. Un efecto sedante puede ser evidente antes de que se note el efecto antidepresivo, pero un efecto terapéutico adecuado puede tardar hasta 30 días en desarrollarse.
Un método alternativo para iniciar la terapia en pacientes ambulatorios es comenzar con 50 a 100 mg de amitriptilina HCl a la hora de acostarse. Esto se puede aumentar en 25 o 50 mg según sea necesario en la dosis antes de acostarse hasta un total de 150 mg por día.
Los pacientes hospitalizados pueden requerir 100 mg al día inicialmente. Esto se puede aumentar gradualmente a 200 mg al día si es necesario. Un pequeño número de pacientes hospitalizados puede necesitar hasta 300 mg al día.
Pacientes adolescentes y ancianos
En general, se recomiendan dosis más bajas para estos pacientes. Diez mg 3 veces al día con 20 mg al acostarse pueden ser satisfactorios en pacientes adolescentes y ancianos que no toleran dosis más altas.
Mantenimiento
La dosis habitual de mantenimiento de amitriptilina HCl es de 50 a 100 mg por día. En algunos pacientes, 40 mg por día es suficiente. Para la terapia de mantenimiento, la dosis diaria total puede administrarse en una dosis única, preferiblemente a la hora de acostarse. Cuando se haya alcanzado una mejoría satisfactoria, la dosis debe reducirse a la cantidad más baja que mantenga el alivio de los síntomas. Es apropiado continuar la terapia de mantenimiento durante 3 meses o más para disminuir la posibilidad de recaída.
Uso en pacientes pediátricos
Dada la falta de experiencia en el uso de este fármaco en pacientes pediátricos, actualmente no se recomienda para pacientes menores de 12 años.
Niveles de plasma
Debido a la amplia variación en la absorción y distribución de los antidepresivos tricíclicos en los fluidos corporales, es difícil correlacionar directamente los niveles plasmáticos y el efecto terapéutico. Sin embargo, la determinación de los niveles plasmáticos puede ser útil para identificar pacientes que parecen tener efectos tóxicos y pueden tener niveles excesivamente altos, o aquellos en quienes se sospecha falta de absorción o incumplimiento. Debido al aumento del tiempo de tránsito intestinal y la disminución del metabolismo hepático en pacientes de edad avanzada, los niveles plasmáticos son generalmente más altos para una dosis oral dada de clorhidrato de amitriptilina que en pacientes más jóvenes.
Los pacientes de edad avanzada deben ser monitoreados cuidadosamente y los niveles séricos cuantitativos deben obtenerse según corresponda desde el punto de vista clínico. El ajuste de la dosis debe hacerse de acuerdo con la respuesta clínica del paciente y no en función de los niveles plasmáticos.**
CÓMO SUMINISTRADO
10 miligramos Los comprimidos son azules, redondos, sin ranurar, recubiertos con película, grabados con "2101" en un lado y con una "V" grabada en el reverso. Se suministran de la siguiente manera:
Botellas de 30: CDN 0603-2212-16 Botellas de 90: CDN 0603-2212-02 Botellas de 100: CDN 0603-2212-21 Botellas de 1000: CDN 0603-2212-32
25 miligramos Los comprimidos son amarillos, redondos, sin ranurar, recubiertos con película, grabados con "2102" en un lado y con una "V" grabada en el reverso. Se suministran de la siguiente manera:
Botellas de 90: CDN 0603-2213-02 Botellas de 100: CDN 0603-2213-21 Botellas de 1000: CDN 0603-2213-32 Botellas de 2500: CDN 0603-2213-30
50 miligramos Los comprimidos son de color beige, redondos, sin ranurar, recubiertos con película, grabados con “2103” en un lado y con una “V” grabada en el reverso. Se suministran de la siguiente manera:
Botellas de 100: CDN 0603-2214-21 Botellas de 1000: CDN 0603-2214-32
75 miligramos Los comprimidos son naranjas, redondos, sin ranurar, recubiertos con película, grabados con “2104” y “V”. Se suministran de la siguiente manera:
Botellas de 100: CDN 0603-2215-21 Botellas de 300: CDN 0603-2215-25
100 miligramos Los comprimidos son de color malva, redondos, sin ranurar, recubiertos con película, grabados con “2105” y “V”. Se suministran de la siguiente manera:
Botellas de 100: CDN 0603-2216-21 Botellas de 300: CDN 0603-2216-25
150 miligramos Los comprimidos son azules, con forma de cápsula, sin ranurar, recubiertos con película, grabados con "2106" en un lado y con una "V" grabada en el reverso. Se suministran de la siguiente manera:
Botellas de 100: CDN 0603-2217-21 Botellas de 300: CDN 0603-2217-25
Almacenamiento y manipulación
Almacenamiento
Almacenar en un recipiente bien cerrado. Almacenar a 20°-25°C (68°-77°F) [ver Temperatura ambiente controlada por USP ]. Además, las tabletas de amitriptilina deben protegerse de la luz y almacenarse en un recipiente bien cerrado y resistente a la luz.
REFERENCIAS
Ayd FJ Jr: Terapia con amitriptilina para las reacciones depresivas. Psicosomática 1960; 1: 320–325.
Diamond S: metabolizador humano de amitriptilina marcado con carbono 14. Curr Ther Res, marzo de 1965, págs. 170–175.
Dorfman W: Experiencias clínicas con amitriptilina: un informe preliminar. Psicosomática 1960; 1: 153– 155.
Fallette JM, Stasney CR, Mintz AA: Envenenamiento por amitriptilina tratado con fisostigmina. South Med J 1970;63:1492–1493.
Hollister LE, Overall JE, Johnson M, et al: Comparación controlada de amitriptilina, imipramina y placebo en pacientes deprimidos hospitalizados. J Nerv Ment Dis 1964; 139: 370–375.
Hordern A, Burt CG, Holt NF: Estados depresivos: un estudio farmacoterapéutico, estudio de Springfield. Springfield, Ill, Charles C. Thomas, 1965. Jenike MA: Tratamiento de enfermedades afectivas en ancianos con fármacos y terapia electroconvulsiva. J Geriatr Psiquiatría 1989; 22(1):77–112.
Klerman GL, Cole JO: Farmacología clínica de la imipramina y compuestos antidepresivos relacionados. Int J Psiquiatría 1976;3:267–304.
Liu B, Anderson G, Mittman N, et al: Uso de inhibidores selectivos de la recaptación de serotonina o antidepresivos tricíclicos y riesgo de fracturas de cadera en personas mayores. Lancet 1998; 351 (9112): 1303–1307.
McConaghy N, Joffe AD, Kingston WA, et al: Correlación de características clínicas de pacientes ambulatorios deprimidos con respuesta a amitriptilina y protriptilina. Br J Psiquiatría 1968; 114: 103–106.
McDonald IM, Perkins M, Marjerrison G, et al: Una comparación controlada de amitriptilina y terapia electroconvulsiva en el tratamiento de la depresión. Am J Psiquiatría 1966; 122: 1427–1431.
Slovis T, Ott J, Teitelbaum D, et al: Terapia con fisostigmina en la intoxicación aguda por antidepresivos tricíclicos. Clin Toxicol 1971;4:451–459.
Simposio sobre depresión con estudios especiales de un nuevo antidepresivo, amitriptilina. Dis Nerv Syst, (Sección 2) mayo de 1961, págs. 5–56.
*Basado en una dosis máxima recomendada de amitriptilina de 150 mg/día o 3 mg/kg/día para un paciente de 50 kg.
**Hollister LE: Supervisión de las concentraciones plasmáticas de antidepresivos tricíclicos. JAMA 1979; 241(23):2530–2533.
Los comprimidos de Elavil de 25 mg son comprimidos recubiertos con película, amarillos, redondos, sin ranurar, grabados con "2102" en un lado y con una "V" grabada en el reverso. Se suministran de la siguiente manera: Botellas de 100: CDN 69874-422-10
Fabricado por: Qualitest Pharmaceuticals/Vintage Pharmaceuticals, Huntsville, AL 35811. Fabricado para: Thompson Medical Solutions, Birmingham, AL 35242. Revisado: abril de 2016
EFECTOS SECUNDARIOS
No se proporcionó informaciónINTERACCIONES CON LA DROGAS
Fármacos metabolizados por P450 2D6
La actividad bioquímica del fármaco que metaboliza la isoenzima citocromo P450 2D6 (debrisoquina hidroxilasa) se reduce en un subconjunto de la población caucásica (alrededor del 7 al 10 % de los caucásicos se denominan “metabolizadores lentos”); Aún no se dispone de estimaciones fiables de la prevalencia de la actividad reducida de la isoenzima P450 2D6 entre las poblaciones asiáticas, africanas y otras. Los metabolizadores lentos tienen concentraciones plasmáticas de antidepresivos tricíclicos (TCA) más altas de lo esperado cuando se les administran las dosis habituales. Dependiendo de la fracción de fármaco metabolizado por P450 2D6, el aumento en la concentración plasmática puede ser pequeño o bastante grande (aumento de 8 veces en el AUC plasmático del TCA).
Además, ciertos fármacos inhiben la actividad de esta isoenzima y hacen que los metabolizadores normales parezcan metabolizadores lentos. Un individuo que está estable con una dosis dada de TCA puede volverse tóxico repentinamente cuando se le administra uno de estos fármacos inhibidores como terapia concomitante. Los fármacos que inhiben el citocromo P450 2D6 incluyen algunos que no son metabolizados por la enzima (quinidina, cimetidina) y muchos que son sustratos del P450 2D6 (muchos otros antidepresivos, fenotiazinas y los antiarrítmicos tipo 1C propafenona y flecainida). Si bien todos los inhibidores selectivos de la recaptación de serotonina (ISRS), por ejemplo, fluoxetina, sertralina y paroxetina, inhiben la P450 2D6, pueden variar en el grado de inhibición. La medida en que las interacciones ISRS-TCA pueden plantear problemas clínicos dependerá del grado de inhibición y la farmacocinética del ISRS involucrado. No obstante, se recomienda precaución en la coadministración de TCA con cualquiera de los ISRS y también en el cambio de una clase a otra. De particular importancia, debe transcurrir suficiente tiempo antes de iniciar el tratamiento con ATC en un paciente al que se le retira la fluoxetina, dada la larga vida media del metabolito original y activo (pueden ser necesarias al menos 5 semanas).
El uso concomitante de antidepresivos tricíclicos con fármacos que pueden inhibir el citocromo P450 2D6 puede requerir dosis más bajas que las prescritas normalmente para el antidepresivo tricíclico o el otro fármaco. Además, cada vez que uno de estos otros medicamentos se retira de la coterapia, puede ser necesario aumentar la dosis de antidepresivos tricíclicos. Es deseable controlar los niveles plasmáticos de TCA cada vez que se coadministre un TCA con otro fármaco conocido por ser un inhibidor de P450 2D6.
Inhibidores de la monoaminooxidasa
Ver CONTRAINDICACIONES sección. guanetidina o compuestos de acción similar; medicamento para la tiroides; alcohol, barbitúricos y otros depresores del SNC; y disulfiram – ver ADVERTENCIAS sección. Cuando el clorhidrato de amitriptilina se administra con agentes anticolinérgicos o fármacos simpaticomiméticos, incluida la epinefrina combinada con anestésicos locales, se requiere una estrecha supervisión y un ajuste cuidadoso de las dosis.
Se ha informado hiperpirexia cuando se administra clorhidrato de amitriptilina con agentes anticolinérgicos o con fármacos neurolépticos, particularmente durante climas cálidos.
El íleo paralítico puede ocurrir en pacientes que toman antidepresivos tricíclicos en combinación con medicamentos de tipo anticolinérgico.
Se informa que la cimetidina reduce el metabolismo hepático de ciertos antidepresivos tricíclicos, lo que retrasa la eliminación y aumenta las concentraciones en estado estacionario de estos fármacos. Se han informado efectos clínicamente significativos con los antidepresivos tricíclicos cuando se usan concomitantemente con cimetidina. Se han informado aumentos en los niveles plasmáticos de antidepresivos tricíclicos y en la frecuencia y gravedad de los efectos secundarios, particularmente anticolinérgicos, cuando se agregó cimetidina al régimen farmacológico. La interrupción de la cimetidina en pacientes bien controlados que reciben antidepresivos tricíclicos y cimetidina puede disminuir los niveles plasmáticos y la eficacia de los antidepresivos.
Se recomienda precaución si los pacientes reciben grandes dosis de etlorvinol al mismo tiempo. Se ha informado delirio transitorio en pacientes que fueron tratados con un gramo de etlorvinol y 75 a 150 mg de clorhidrato de amitriptilina.
EFECTOS SECUNDARIOS
Dentro de cada categoría, las siguientes reacciones adversas se enumeran en orden de gravedad decreciente. En la lista se incluyen algunas reacciones adversas que no se han informado con este medicamento específico. Sin embargo, las similitudes farmacológicas entre los fármacos antidepresivos tricíclicos requieren que se considere cada una de las reacciones cuando se administra amitriptilina.
Cardiovascular: Infarto de miocardio; carrera; cambios ECG inespecíficos y cambios en la conducción AV; bloqueo cardíaco; arritmias; hipotensión, particularmente hipotensión ortostática; síncope; hipertensión; taquicardia; palpitación.
SNC y Neuromusculares: Coma; convulsiones; alucinaciones; engaño; estados confusionales; desorientación; incoordinación; ataxia; temblores; neuropatía periférica; entumecimiento, hormigueo y parestesias de las extremidades; síntomas extrapiramidales que incluyen movimientos involuntarios anormales y discinesia tardía; disartria; concentración perturbada; excitación; ansiedad; insomnio; inquietud; pesadillas; somnolencia; mareo; debilidad; fatiga; dolor de cabeza; síndrome de secreción inadecuada de ADH (hormona antidiurética); tinnitus; alteración en los patrones EEG.
Anticolinérgico: Íleo paralítico; hiperpirexia; retención urinaria; dilatación del tracto urinario; estreñimiento; visión borrosa, alteración de la acomodación, aumento de la presión ocular, midriasis; boca seca.
Alérgico: Erupción cutanea; urticaria; fotosensibilización; edema de cara y lengua.
hematológico: depresión de la médula ósea que incluye agranulocitosis, leucopenia, trombocitopenia; púrpura; eosinofilia.
Gastrointestinal: Raramente hepatitis (incluyendo función hepática alterada e ictericia); náuseas; malestar epigástrico; vómitos; anorexia; estomatitis; sabor peculiar; Diarrea; hinchazón de la parótida; lengua negra.
Endocrino: Hinchazón testicular y ginecomastia en el varón; agrandamiento de los senos y galactorrea en la mujer; aumento o disminución de la libido; impotencia; elevación y disminución de los niveles de azúcar en la sangre.
Otro: Alopecia; edema; ganancia o pérdida de peso; frecuencia urinaria; aumento de la transpiración.
Síntomas de abstinencia: Después de una administración prolongada, la interrupción brusca del tratamiento puede producir náuseas, dolor de cabeza y malestar general. Se ha informado que las reducciones graduales de la dosis producen, dentro de dos semanas, síntomas transitorios que incluyen irritabilidad, inquietud y trastornos del sueño y del sueño.
Estos síntomas no son indicativos de adicción. Se han informado casos raros de manía o hipomanía que ocurren dentro de los 2 a 7 días posteriores al cese de la terapia crónica con antidepresivos tricíclicos.
Relación causal desconocida: Otras reacciones, notificadas en circunstancias en las que no se pudo establecer una relación causal, se enumeran para servir como información de alerta para los médicos.
Cuerpo como un todo: Síndrome tipo lupus (artritis migratoria, ANA positivo y factor reumatoide).
Digestivo: Insuficiencia hepática, ageusia.
Eventos adversos posteriores a la comercialización
Muy raramente se ha informado un síndrome similar al síndrome neuroléptico maligno (SNM) después de comenzar o aumentar la dosis de clorhidrato de amitriptilina, con y sin medicamentos concomitantes que se sabe que causan SNM. Los síntomas han incluido rigidez muscular, fiebre, cambios en el estado mental, diaforesis, taquicardia y temblor.
Se han notificado casos muy raros de síndrome serotoninérgico (SS) con clorhidrato de amitriptilina en combinación con otros fármacos que tienen una asociación reconocida con SS.
Se han notificado casos muy raros de cardiomiopatía con amitriptilina.
ADVERTENCIAS
Empeoramiento clínico y riesgo de suicidio
Los pacientes con trastorno depresivo mayor (MDD), tanto adultos como pediátricos, pueden experimentar un empeoramiento de su depresión y/o la aparición de ideación y comportamiento suicida (suicidalidad) o cambios inusuales en el comportamiento, estén o no tomando medicamentos antidepresivos, y esto el riesgo puede persistir hasta que ocurra una remisión significativa. El suicidio es un riesgo conocido de depresión y ciertos otros trastornos psiquiátricos, y estos trastornos en sí mismos son los predictores más fuertes de suicidio. Sin embargo, desde hace mucho tiempo existe la preocupación de que los antidepresivos puedan tener un papel en la inducción del empeoramiento de la depresión y la aparición de tendencias suicidas en ciertos pacientes durante las primeras fases del tratamiento. Los análisis combinados de ensayos controlados con placebo a corto plazo de medicamentos antidepresivos (ISRS y otros) mostraron que estos medicamentos aumentan el riesgo de pensamientos y conductas suicidas (tendencia al suicidio) en niños, adolescentes y adultos jóvenes (de 18 a 24 años) con trastorno depresivo mayor ( MDD) y otros trastornos psiquiátricos. Los estudios a corto plazo no mostraron un aumento en el riesgo de tendencias suicidas con antidepresivos en comparación con placebo en adultos mayores de 24 años; hubo una reducción con los antidepresivos en comparación con el placebo en adultos de 65 años o más.
Los análisis agrupados de ensayos controlados con placebo en niños y adolescentes con TDM, trastorno obsesivo compulsivo (TOC) u otros trastornos psiquiátricos incluyeron un total de 24 ensayos a corto plazo de 9 fármacos antidepresivos en más de 4400 pacientes. Los análisis agrupados de ensayos controlados con placebo en adultos con MDD u otros trastornos psiquiátricos incluyeron un total de 295 ensayos a corto plazo (duración media de 2 meses) de 11 fármacos antidepresivos en más de 77 000 pacientes. Hubo una variación considerable en el riesgo de suicidio entre los fármacos, pero una tendencia hacia un aumento en los pacientes más jóvenes para casi todos los fármacos estudiados. Hubo diferencias en el riesgo absoluto de suicidio entre las diferentes indicaciones, con la mayor incidencia en MDD. Sin embargo, las diferencias de riesgo (fármaco frente a placebo) fueron relativamente estables dentro de los estratos de edad y entre las indicaciones. Estas diferencias de riesgo (diferencia fármaco-placebo en el número de casos de tendencias suicidas por cada 1000 pacientes tratados) se proporcionan en la Tabla 1.
No se produjeron suicidios en ninguno de los ensayos pediátricos. Hubo suicidios en los ensayos con adultos, pero el número no fue suficiente para llegar a ninguna conclusión sobre el efecto del fármaco sobre el suicidio.
Se desconoce si el riesgo de suicidio se extiende al uso a largo plazo, es decir, más allá de varios meses. Sin embargo, existe evidencia sustancial de ensayos de mantenimiento controlados con placebo en adultos con depresión de que el uso de antidepresivos puede retrasar la recurrencia de la depresión.
Todos los pacientes que reciben tratamiento con antidepresivos por cualquier indicación deben ser monitoreados adecuadamente y observados de cerca por si empeoran clínicamente, tienen tendencias suicidas y cambios inusuales en el comportamiento, especialmente durante los meses iniciales de un ciclo de terapia con medicamentos, o en momentos de cambios de dosis, ya sea aumentos o disminuye.
Los siguientes síntomas, ansiedad, agitación, ataques de pánico, insomnio, irritabilidad, hostilidad, agresividad, impulsividad, acatisia (inquietud psicomotora), hipomanía y manía, se han informado en pacientes adultos y pediátricos que también reciben tratamiento con antidepresivos para el trastorno depresivo mayor como para otras indicaciones, tanto psiquiátricas como no psiquiátricas. Aunque no se ha establecido un vínculo causal entre la aparición de tales síntomas y el empeoramiento de la depresión y/o la aparición de impulsos suicidas, existe la preocupación de que tales síntomas puedan representar precursores de tendencias suicidas emergentes.
Se debe considerar cambiar el régimen terapéutico, incluida la posibilidad de suspender el medicamento, en pacientes cuya depresión empeora persistentemente, o que están experimentando tendencias suicidas emergentes o síntomas que podrían ser precursores de un empeoramiento de la depresión o tendencias suicidas, especialmente si estos síntomas son severos, abruptos. en el inicio, o no formaban parte de los síntomas de presentación del paciente.
Se debe alertar a las familias y cuidadores de pacientes en tratamiento con antidepresivos por trastorno depresivo mayor u otras indicaciones, tanto psiquiátricas como no psiquiátricas, sobre la necesidad de monitorear a los pacientes por la aparición de agitación, irritabilidad, cambios inusuales en el comportamiento y otros síntomas. descrito anteriormente, así como el surgimiento de tendencias suicidas, e informar dichos síntomas de inmediato a los proveedores de atención médica. Dicho seguimiento debe incluir la observación diaria por parte de las familias y los cuidadores. Las recetas de tabletas de clorhidrato de amitriptilina se deben escribir para la cantidad más pequeña de tabletas compatible con un buen manejo del paciente, a fin de reducir el riesgo de sobredosis.
Detección de pacientes para el trastorno bipolar
Un episodio depresivo mayor puede ser la presentación inicial del trastorno bipolar. En general, se cree (aunque no se ha establecido en ensayos controlados) que tratar un episodio de este tipo con un antidepresivo solo puede aumentar la probabilidad de precipitación de un episodio mixto/maníaco en pacientes con riesgo de trastorno bipolar. Se desconoce si alguno de los síntomas descritos anteriormente representa tal conversión. Sin embargo, antes de iniciar el tratamiento con un antidepresivo, los pacientes con síntomas depresivos deben someterse a un cribado adecuado para determinar si tienen riesgo de trastorno bipolar; dicha evaluación debe incluir un historial psiquiátrico detallado, incluidos antecedentes familiares de suicidio, trastorno bipolar y depresión. Cabe señalar que las tabletas de clorhidrato de amitriptilina no están aprobadas para su uso en el tratamiento de la depresión bipolar.
El clorhidrato de amitriptilina puede bloquear la acción antihipertensiva de la guanetidina o compuestos de acción similar.
Debe usarse con precaución en pacientes con antecedentes de convulsiones y, debido a su acción similar a la atropina, en pacientes con antecedentes de retención urinaria o glaucoma de ángulo cerrado. En pacientes con glaucoma de ángulo cerrado, incluso las dosis promedio pueden precipitar un ataque.
Los pacientes con trastornos cardiovasculares deben ser vigilados de cerca. Se ha informado que los fármacos antidepresivos tricíclicos, incluido el clorhidrato de amitriptilina, particularmente cuando se administran en dosis altas, producen arritmias, taquicardia sinusal y prolongación del tiempo de conducción. Se han notificado casos de infarto de miocardio y accidente cerebrovascular con fármacos de esta clase.
Se requiere una estrecha supervisión cuando se administra clorhidrato de amitriptilina a pacientes hipertiroideos o que reciben medicamentos para la tiroides.
El clorhidrato de amitriptilina puede aumentar la respuesta al alcohol y los efectos de los barbitúricos y otros depresores del SNC. En pacientes que puedan consumir alcohol en exceso, se debe tener en cuenta que la potenciación puede aumentar el peligro inherente a cualquier intento de suicidio o sobredosis. Se ha informado delirio con la administración concomitante de amitriptilina y disulfiram.
Glaucoma de ángulo cerrado
La dilatación pupilar que ocurre después del uso de muchos medicamentos antidepresivos, incluidas las tabletas de clorhidrato de amitriptilina, puede desencadenar un ataque de ángulo cerrado en un paciente con ángulos anatómicamente estrechos que no tienen una iridectomía permeable.
Uso en el embarazo
Embarazo Categoría C
No se observaron efectos teratogénicos en ratones, ratas o conejos cuando se administró amitriptilina por vía oral en dosis de 2 a 40 mg/kg/día (hasta 13 veces la dosis máxima recomendada en humanos*). Los estudios en la literatura han demostrado que la amitriptilina es teratogénica en ratones y hámsters cuando se administra por varias vías de administración en dosis de 28 a 100 mg/kg/día (9 a 33 veces la dosis máxima recomendada en humanos), produciendo múltiples malformaciones. Otro estudio en ratas informó que una dosis oral de 25 mg/kg/día (8 veces la dosis máxima recomendada en humanos) produjo retrasos en la osificación de los cuerpos vertebrales fetales sin otros signos de embriotoxicidad. En conejos, se informó que una dosis oral de 60 mg/kg/día (20 veces la dosis máxima recomendada en humanos) provocó una osificación incompleta de los huesos del cráneo.
Se ha demostrado que la amitriptilina atraviesa la placenta. Aunque no se ha establecido una relación causal, ha habido algunos informes de eventos adversos, incluidos efectos en el SNC, deformidades de las extremidades o retraso en el desarrollo, en bebés cuyas madres tomaron amitriptilina durante el embarazo. No existen estudios adecuados y bien controlados en mujeres embarazadas. El clorhidrato de amitriptilina debe usarse durante el embarazo solo si el beneficio potencial para la madre justifica el riesgo potencial para el feto.
Madres lactantes
La amitriptilina se excreta en la leche materna. En un informe en el que una paciente recibió 100 mg/día de amitriptilina mientras amamantaba a su bebé, se detectaron niveles de 83 a 141 ng/mL en el suero de la madre. Se encontraron niveles de 135 a 151 ng/mL en la leche materna, pero no se pudo detectar ningún rastro de la droga en el suero del bebé.
Debido a la posibilidad de que la amitriptilina produzca reacciones adversas graves en lactantes, se debe tomar la decisión de suspender la lactancia o suspender el fármaco, teniendo en cuenta la importancia del fármaco para la madre.
Uso en pacientes pediátricos
Dada la falta de experiencia en el uso de este fármaco en pacientes pediátricos, actualmente no se recomienda para pacientes menores de 12 años.
PRECAUCIONES
Los pacientes esquizofrénicos pueden desarrollar un aumento de los síntomas de psicosis; los pacientes con sintomatología paranoide pueden tener una exageración de tales síntomas. Los pacientes deprimidos, en particular aquellos con enfermedad maníaco-depresiva conocida, pueden experimentar un cambio a manía o hipomanía. En estas circunstancias, se puede reducir la dosis de amitriptilina o se puede administrar simultáneamente un tranquilizante importante como la perfenazina.
La posibilidad de suicidio en pacientes deprimidos permanece hasta que se produce una remisión significativa. Los pacientes potencialmente suicidas no deben tener acceso a grandes cantidades de este medicamento. Las recetas deben escribirse por la cantidad más pequeña posible.
La administración simultánea de clorhidrato de amitriptilina y terapia de electroshock puede aumentar los riesgos asociados con dicha terapia. Dicho tratamiento debe limitarse a los pacientes para los que es esencial.
Cuando sea posible, el medicamento debe suspenderse varios días antes de la cirugía electiva.
Se han informado tanto la elevación como la disminución de los niveles de azúcar en la sangre.
El clorhidrato de amitriptilina se debe utilizar con precaución en pacientes con insuficiencia hepática.
Información para pacientes
Los prescriptores u otros profesionales de la salud deben informar a los pacientes, sus familias y sus cuidadores sobre los beneficios y riesgos asociados con el tratamiento con tabletas de clorhidrato de amitriptilina y deben asesorarlos sobre su uso apropiado. Un paciente Guía de medicamentos sobre “Medicamentos antidepresivos, depresión y otras enfermedades mentales graves y pensamientos o acciones suicidas” está disponible para las tabletas de clorhidrato de amitriptilina. El prescriptor o el profesional de la salud debe instruir a los pacientes, sus familias y sus cuidadores para que lean el Guía de medicamentos y debe ayudarlos a comprender su contenido. Los pacientes deben tener la oportunidad de discutir el contenido de la Guía de medicamentos y para obtener respuestas a cualquier pregunta que puedan tener. El texto completo de la Guía de medicamentos se reproduce al final de este documento.
Se debe informar a los pacientes sobre los siguientes problemas y pedirles que alerten a su prescriptor si ocurren mientras toman tabletas de clorhidrato de amitriptilina.
Durante la terapia con clorhidrato de amitriptilina, se debe advertir a los pacientes sobre el posible deterioro de las capacidades mentales y/o físicas requeridas para realizar tareas peligrosas, como operar maquinaria o conducir un vehículo motorizado.
Se debe advertir a los pacientes que tomar tabletas de clorhidrato de amitriptilina puede causar dilatación papilar leve, lo que en individuos susceptibles puede conducir a un episodio de glaucoma de ángulo cerrado. El glaucoma preexistente casi siempre es glaucoma de ángulo abierto porque el glaucoma de ángulo cerrado, cuando se diagnostica, se puede tratar definitivamente con iridectomía. El glaucoma de ángulo abierto no es un factor de riesgo para el glaucoma de ángulo cerrado. Los pacientes pueden desear ser examinados para determinar si son susceptibles al cierre del ángulo y someterse a un procedimiento profiláctico (p. ej., iridectomía), si son susceptibles.
Empeoramiento clínico y riesgo de suicidio
Se debe alentar a los pacientes, sus familias y sus cuidadores a estar alerta ante la aparición de ansiedad, agitación, ataques de pánico, insomnio, irritabilidad, hostilidad, agresividad, impulsividad, acatisia (inquietud psicomotora), hipomanía, manía, otros cambios inusuales en el comportamiento. , empeoramiento de la depresión e ideación suicida, especialmente al principio del tratamiento con antidepresivos y cuando la dosis se ajusta hacia arriba o hacia abajo. Se debe recomendar a las familias y cuidadores de los pacientes que estén atentos a la aparición de dichos síntomas en el día a día, ya que los cambios pueden ser abruptos. Dichos síntomas deben informarse al médico o al profesional de la salud del paciente, especialmente si son graves, de inicio repentino o no formaban parte de los síntomas que presentaba el paciente. Síntomas como estos pueden estar asociados con un mayor riesgo de pensamientos y conductas suicidas e indican la necesidad de un control muy estricto y posiblemente cambios en la medicación.
Uso pediátrico
No se ha establecido la seguridad y eficacia en la población pediátrica (ver CUADRO DE ADVERTENCIA y ADVERTENCIAS - Empeoramiento clínico y riesgo de suicidio ). Cualquiera que esté considerando el uso de tabletas de clorhidrato de amitriptilina en un niño o adolescente debe sopesar los riesgos potenciales con la necesidad clínica.
Uso geriátrico
La experiencia clínica no ha identificado diferencias en las respuestas entre pacientes ancianos y jóvenes. En general, la selección de la dosis para un paciente de edad avanzada debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, enfermedad concomitante y otra terapia farmacológica en pacientes de edad avanzada.
Los pacientes geriátricos son particularmente sensibles a los efectos secundarios anticolinérgicos de los antidepresivos tricíclicos, incluido el clorhidrato de amitriptilina. Los efectos anticolinérgicos periféricos incluyen taquicardia, retención urinaria, estreñimiento, boca seca, visión borrosa y exacerbación del glaucoma de ángulo estrecho. Los efectos anticolinérgicos del sistema nervioso central incluyen deterioro cognitivo, enlentecimiento psicomotor, confusión, sedación y delirio. Los pacientes de edad avanzada que toman clorhidrato de amitriptilina pueden tener un mayor riesgo de caídas. Los pacientes de edad avanzada deben comenzar con dosis bajas de clorhidrato de amitriptilina y observarse de cerca (ver DOSIFICACIÓN Y ADMINISTRACIÓN ).
SOBREDOSIS
Pueden ocurrir muertes por sobredosis con esta clase de medicamentos. La ingestión de múltiples drogas (incluido el alcohol) es común en la sobredosis deliberada de antidepresivos tricíclicos. Como el manejo es complejo y cambiante, se recomienda que el médico se comunique con un centro de control de intoxicaciones para obtener información actualizada sobre el tratamiento. Los signos y síntomas de toxicidad se desarrollan rápidamente después de una sobredosis de antidepresivos tricíclicos; por lo tanto, se requiere vigilancia hospitalaria lo antes posible.
Manifestaciones
Las manifestaciones críticas de sobredosis incluyen: arritmias cardíacas, hipotensión grave, convulsiones y depresión del SNC, incluido el coma. Los cambios en el electrocardiograma, particularmente en el eje QRS o el ancho, son indicadores clínicamente significativos de toxicidad por antidepresivos tricíclicos. Además, un desplazamiento del eje hacia la derecha en el complejo QRS terminal junto con un intervalo QT prolongado y taquicardia sinusal son indicadores específicos y sensibles de sobredosis de tricíclicos de primera generación. La ausencia de estos hallazgos no es excluyente. También pueden ocurrir intervalo PR prolongado, cambios en la onda ST-T, taquicardia ventricular y fibrilación.
Otros signos de sobredosis pueden incluir: alteración de la contractilidad miocárdica, confusión, alteración de la concentración, alucinaciones visuales transitorias, pupilas dilatadas, trastornos de la motilidad ocular, agitación, reflejos hiperactivos, polirradiculoneuropatía, estupor, somnolencia, rigidez muscular, vómitos, hipotermia, hiperpirexia o cualquier de los síntomas enumerados en REACCIONES ADVERSAS.
administración
General
Obtenga un ECG e inicie inmediatamente la monitorización cardíaca. Proteja las vías respiratorias del paciente, establezca una vía intravenosa e inicie la descontaminación gástrica. Es necesario un mínimo de seis horas de observación con monitoreo cardíaco y observación de signos de depresión respiratoria o del SNC, hipotensión, arritmias cardíacas y/o bloqueos de conducción, y convulsiones. Si se presentan signos de toxicidad en cualquier momento durante el período, se requiere un seguimiento prolongado. Hay informes de casos de pacientes que sucumbieron a arritmias fatales después de una sobredosis; estos pacientes tenían evidencia clínica de envenenamiento significativo antes de la muerte y la mayoría recibió una descontaminación gastrointestinal inadecuada. La monitorización de los niveles plasmáticos del fármaco no debe guiar el tratamiento del paciente.
Descontaminación Gastrointestinal
Todos los pacientes con sospecha de sobredosis de antidepresivos tricíclicos deben recibir descontaminación gastrointestinal. Esto debe incluir un lavado gástrico de gran volumen seguido de carbón activado. Si la conciencia está alterada, se debe asegurar la vía aérea antes del lavado. LA ÉMESIS ESTÁ CONTRAINDICADA.
Cardiovascular
Una duración máxima de QRS de derivación de extremidades de ≥ 0,10 segundos puede ser la mejor indicación de la gravedad de la sobredosis. Se debe usar bicarbonato de sodio intravenoso para mantener el pH sérico en el rango de 7,45 a 7,55. Si la respuesta del pH es inadecuada, también se puede utilizar la hiperventilación. El uso concomitante de hiperventilación y bicarbonato de sodio debe hacerse con extrema precaución, con monitoreo frecuente de Ph. No es deseable un pH > 7,60 o una pCO2
En casos raros, la hemoperfusión puede ser beneficiosa en la inestabilidad cardiovascular refractaria aguda en pacientes con toxicidad aguda. Sin embargo, la hemodiálisis, la diálisis peritoneal, las exanguinotransfusiones y la diuresis forzada por lo general han sido reportadas como ineficaces en el envenenamiento por antidepresivos tricíclicos.
SNC
En pacientes con depresión del SNC, se recomienda la intubación temprana debido al potencial de deterioro abrupto. Las convulsiones deben controlarse con benzodiazepinas o, si no son eficaces, con otros anticonvulsivos (p. ej., fenobarbital, fenitoína).
No se recomienda la fisostigmina excepto para tratar síntomas potencialmente mortales que no han respondido a otras terapias, y solo en consulta con un centro de control de envenenamiento.
Seguimiento Psiquiátrico
Dado que la sobredosis suele ser deliberada, los pacientes pueden intentar suicidarse por otros medios durante la fase de recuperación. La derivación psiquiátrica puede ser apropiada.
Manejo pediátrico
Los principios de manejo de las sobredosis pediátricas y de adultos son similares. Se recomienda enfáticamente que el médico se comunique con el centro local de control de envenenamiento para un tratamiento pediátrico específico.
CONTRAINDICACIONES
El clorhidrato de amitriptilina está contraindicado en pacientes que hayan mostrado hipersensibilidad previa al mismo. No debe administrarse concomitantemente con inhibidores de la monoaminooxidasa. Se han producido crisis hiperpiréticas, convulsiones graves y muertes en pacientes que recibieron simultáneamente antidepresivos tricíclicos e inhibidores de la monoaminooxidasa. Cuando se desee sustituir un inhibidor de la monoaminooxidasa por clorhidrato de amitriptilina, se debe dejar transcurrir un mínimo de 14 días desde la suspensión del primero. El clorhidrato de amitriptilina debe entonces iniciarse con cautela con un aumento gradual de la dosis hasta lograr una respuesta óptima.
El clorhidrato de amitriptilina no debe administrarse con cisaprida debido a la posibilidad de que aumente el intervalo QT y aumente el riesgo de arritmia.
No se recomienda el uso de este medicamento durante la fase de recuperación aguda después de un infarto de miocardio.
FARMACOLOGÍA CLÍNICA
El clorhidrato de amitriptilina es un antidepresivo con efectos sedantes. Se desconoce su mecanismo de acción en el hombre. No es un inhibidor de la monoaminooxidasa y no actúa principalmente estimulando el sistema nervioso central.
La amitriptilina inhibe el mecanismo de bomba de membrana responsable de la captación de norepinefrina y serotonina en las neuronas adrenérgicas y serotoninérgicas. Farmacológicamente, esta acción puede potenciar o prolongar la actividad neuronal, ya que la recaptación de estas aminas biogénicas es fisiológicamente importante para terminar la actividad de transmisión. Algunos creen que esta interferencia con la recaptación de norepinefrina y/o serotonina es la base de la actividad antidepresiva de la amitriptilina.
Metabolismo
Los estudios en humanos después de la administración oral del fármaco marcado con 14C indicaron que la amitriptilina se absorbe y metaboliza rápidamente. La radiactividad del plasma fue prácticamente insignificante, aunque cantidades significativas de radiactividad aparecieron en la orina entre 4 y 6 horas y entre la mitad y un tercio del fármaco se excretó en 24 horas.
La amitriptilina se metaboliza por N-desmetilación e hidroxilación en puente en el hombre, el conejo y la rata. Prácticamente toda la dosis se excreta como glucurónido o sulfato conjugado de metabolitos, y aparece poco fármaco inalterado en la orina. Otras vías metabólicas pueden estar involucradas.
INFORMACIÓN DEL PACIENTE
Medicamentos antidepresivos, depresión y otras enfermedades mentales graves, y pensamientos o acciones suicidas
Lea la Guía del medicamento que viene con su medicamento antidepresivo o el de su familiar. Esta Guía del medicamento solo trata sobre el riesgo de pensamientos y acciones suicidas con medicamentos antidepresivos. Hable con su proveedor de atención médica o el de su familiar sobre:
- todos los riesgos y beneficios del tratamiento con medicamentos antidepresivos
- todas las opciones de tratamiento para la depresión u otra enfermedad mental grave
¿Cuál es la información más importante que debo saber sobre los medicamentos antidepresivos, la depresión y otras enfermedades mentales graves y los pensamientos o acciones suicidas?
- Preste mucha atención a cualquier cambio, especialmente a los repentinos, en el estado de ánimo, el comportamiento, los pensamientos o los sentimientos. Esto es muy importante cuando se inicia un medicamento antidepresivo o cuando se cambia la dosis.
- Llame al proveedor de atención médica de inmediato para informar cambios nuevos o repentinos en el estado de ánimo, el comportamiento, los pensamientos o los sentimientos.
- Mantenga todas las visitas de seguimiento con el proveedor de atención médica según lo programado. Llame al proveedor de atención médica entre visitas según sea necesario, especialmente si le preocupan los síntomas.
Llame a un proveedor de atención médica de inmediato si usted o un miembro de su familia tienen alguno de los siguientes síntomas, especialmente si son nuevos, empeoran o le preocupan:
- pensamientos sobre el suicidio o la muerte
- intentos de suicidio
- depresión nueva o peor
- ansiedad nueva o peor
- sentirse muy agitado o inquieto
- ataques de pánico
- dificultad para dormir (insomnio)
- irritabilidad nueva o peor
- Actuar agresivo, estar enojado o violento.
- actuando sobre impulsos peligrosos
- un aumento extremo en la actividad y el habla (manía)
- otros cambios inusuales en el comportamiento o el estado de ánimo
- Problemas visuales: dolor en los ojos, cambios en la visión, hinchazón o enrojecimiento en o alrededor del ojo
¿Qué más necesito saber sobre los medicamentos antidepresivos?
- Nunca deje de tomar un medicamento antidepresivo sin hablar primero con un proveedor de atención médica. Detener un medicamento antidepresivo repentinamente puede causar otros síntomas.
- Problemas visuales. Solo algunas personas corren el riesgo de tener estos problemas. Es posible que desee someterse a un examen de la vista para ver si está en riesgo y recibir tratamiento preventivo si lo está.
- Los antidepresivos son medicamentos que se usan para tratar la depresión y otras enfermedades. Es importante discutir todos los riesgos de tratar la depresión y también los riesgos de no tratarla. Los pacientes y sus familias u otros cuidadores deben analizar todas las opciones de tratamiento con el proveedor de atención médica, no solo el uso de antidepresivos.
- Las medicinas antidepresivas tienen otros efectos secundarios. Hable con el proveedor de atención médica sobre los efectos secundarios del medicamento recetado para usted o su familiar.
- Los medicamentos antidepresivos pueden interactuar con otros medicamentos . Conozca todos los medicamentos que toma usted o su familiar. Mantenga una lista de todos los medicamentos para mostrársela al proveedor de atención médica. No empiece a tomar nuevos medicamentos sin antes consultar con su proveedor de atención médica.
- No todos los medicamentos antidepresivos recetados para niños están aprobados por la FDA para su uso en niños. Hable con el proveedor de atención médica de su hijo para obtener más información.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
Esta Guía del medicamento ha sido aprobada por la Administración de Drogas y Alimentos de los EE. UU. para todos los antidepresivos.
