Xalatan 2.5ml Latanoprost Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
XALATAN® (latanoprost) solución oftálmica
DESCRIPCIÓN
Latanoprost es un análogo de la prostaglandina F2α. Su nombre químico es isopropil-(Z)-7[(1R,2R,3R,5S)3,5dihidroxi-2-[(3R)-3-hidroxi-5-fenilpentil]ciclopentil]-5-heptenoato. Su fórmula molecular es C26H40O5 y su estructura química es:
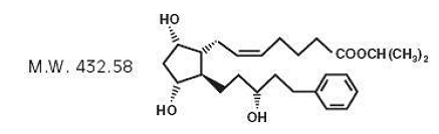
Latanoprost es un aceite incoloro a ligeramente amarillo que es muy soluble en acetonitrilo y fácilmente soluble en acetona, etanol, acetato de etilo, isopropanol, metanol y octanol. Es practicamente insoluble en agua.
XALATAN (solución oftálmica de latanoprost) 0,005 % se suministra como una solución acuosa estéril, isotónica y tamponada de latanoprost con un pH de aproximadamente 6,7 y una osmolalidad de aproximadamente 267 mOsmol/kg. Cada mL de XALATAN contiene 50 mcg de latanoprost. Se añade cloruro de benzalconio, 0,02% como conservante. Los ingredientes inactivos son: cloruro de sodio, dihidrogenofosfato de sodio monohidrato, hidrogenofosfato de disodio anhidro y agua para inyección. Una gota contiene aproximadamente 1,5 mcg de latanoprost.
INDICACIONES
XALATAN 2,5ml está indicado para la reducción de la presión intraocular elevada en pacientes con glaucoma de ángulo abierto o hipertensión ocular.
DOSIFICACIÓN Y ADMINISTRACIÓN
La dosis recomendada es de una gota en el(los) ojo(s) afectado(s) una vez al día por la noche. Si se olvida una dosis, el tratamiento debe continuar con la siguiente dosis de forma normal.
La dosis de XALATAN no debe exceder una vez al día; No se recomienda el uso combinado de dos o más prostaglandinas o análogos de prostaglandinas, incluido XALATAN 2,5 ml. Se ha demostrado que la administración de estos productos farmacéuticos de prostaglandina más de una vez al día puede disminuir el efecto de disminución de la presión intraocular (PIO) o causar elevaciones paradójicas de la PIO.
La reducción de la PIO comienza aproximadamente de 3 a 4 horas después de la administración y el efecto máximo se alcanza después de 8 a 12 horas.
XALATAN se puede usar junto con otros medicamentos oftálmicos tópicos para reducir la PIO. Si se usa más de un fármaco oftálmico tópico, los fármacos deben administrarse al menos con cinco (5) minutos de diferencia. Las lentes de contacto deben retirarse antes de la administración de XALATAN 2,5 ml y pueden volver a colocarse 15 minutos después de la administración.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
Solución oftálmica estéril que contiene 50 mcg/mL de latanoprost.
Almacenamiento y manipulación
XALATAN es una solución transparente, isotónica, tamponada e incolora conservada de latanoprost al 0,005 % (50 mcg/ml). Se suministra como una solución de 2,5 ml en un frasco transparente de polietileno de baja densidad de 5 ml con un cuentagotas de polietileno transparente, un tapón de rosca de polietileno de alta densidad color turquesa y una tapa superior de polietileno de baja densidad transparente a prueba de manipulaciones.
Llenado de 2,5 ml, 0,005 % (50 mcg/ml): Paquete de 1 botella: CDN 0013-8303-04 Llenado de 2,5 ml, 0,005 % (50 mcg/ml): paquete múltiple de 3 botellas: CDN 0013-8303-01
Almacenamiento
Proteger de la luz. Guarde la(s) botella(s) sin abrir en refrigeración a una temperatura de 2° a 8°C (36° a 46°F). Durante el envío al paciente, el frasco se puede mantener a temperaturas de hasta 40 °C (104 °F) durante un período que no exceda los 8 días. Una vez que se abre una botella para su uso, se puede almacenar a temperatura ambiente hasta 25 °C (77 °F) durante 6 semanas.
Distribuido por: Pharmacia & Upjohn Co., División de Pfizer Inc., NY, NY 10017. Pfizer Manufacturing Belgium NV Puurs, Bélgica. Revisado: n/a
EFECTOS SECUNDARIOS
Las siguientes reacciones adversas se informaron en la experiencia posterior a la comercialización y se analizan con mayor detalle en otras secciones de la etiqueta:
- Cambios en la pigmentación del iris [ver ADVERTENCIAS Y PRECAUCIONES ]
- Oscurecimiento de la piel de los párpados [ver ADVERTENCIAS Y PRECAUCIONES ]
- Cambios en las pestañas (aumento de la longitud, el grosor, la pigmentación y el número de pestañas) [ver ADVERTENCIAS Y PRECAUCIONES ]
- Inflamación intraocular (iritis/uveítis) [ver ADVERTENCIAS Y PRECAUCIONES ]
- Edema macular, incluido el edema macular cistoide [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se realizan en condiciones muy variables, las tasas de reacciones adversas observadas en los estudios clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica clínica.
XALATAN 2,5 ml se estudió en tres ensayos clínicos multicéntricos, aleatorizados y controlados. Los pacientes recibieron 50 mcg/ml de XALATAN una vez al día o 5 mg/ml del comparador activo (timolol) dos veces al día. La población de pacientes estudiada tenía una edad media de 65±10 años. El siete por ciento de los pacientes se retiró antes del punto final de 6 meses.
Menos del 1% de los pacientes tratados con XALATAN 2,5 ml requirieron la suspensión del tratamiento por intolerancia a la hiperemia conjuntival.
Los eventos/signos y síntomas oculares de la blefaritis se han identificado como “comúnmente observados” a través del análisis de datos de ensayos clínicos.
Experiencia posterior a la comercialización
Las siguientes reacciones se han identificado durante el uso posterior a la comercialización de XALATAN en la práctica clínica. Debido a que son informados voluntariamente por una población de tamaño desconocido, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco. Las reacciones, que se han elegido para su inclusión debido a su gravedad, frecuencia de notificación, posible conexión causal con XALATAN 2,5 ml o una combinación de estos factores, incluyen:
Trastornos del sistema nervioso: Mareo; dolor de cabeza; Necrolisis epidérmica toxica
Trastornos oculares: Cambios en las pestañas y el vello del párpado (aumento de la longitud, el grosor, la pigmentación y el número de pestañas); queratitis; edema corneal y erosiones; inflamación intraocular (iritis/uveítis); edema macular, incluido el edema macular cistoide; triquiasis; cambios periorbitarios y palpebrales que dan como resultado la profundización del surco palpebral; quiste de iris; oscurecimiento de la piel de los párpados; reacción cutánea localizada en los párpados; conjuntivitis; pseudopenfigoide de la conjuntiva ocular
Trastornos respiratorios, torácicos y mediastínicos: Asma y exacerbación del asma; disnea
Trastornos de la piel y del tejido subcutáneo: Prurito
Infecciones e infestaciones: queratitis por herpes
Trastornos cardíacos: Angina de pecho; palpitaciones; angina inestable
Desordenes generales y condiciones administrativas del sitio: Dolor de pecho
INTERACCIONES CON LA DROGAS
Los estudios in vitro han demostrado que se produce precipitación cuando se mezclan colirios que contienen timerosal con XALATAN. Si se utilizan tales medicamentos, deben administrarse con al menos cinco (5) minutos de diferencia.
No se recomienda el uso combinado de dos o más prostaglandinas o análogos de prostaglandinas, incluido XALATAN 2,5 ml. Se ha demostrado que la administración de estos productos farmacéuticos de prostaglandina más de una vez al día puede disminuir el efecto de disminución de la PIO o causar elevaciones paradójicas de la PIO.
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Pigmentación
Se ha informado que XALATAN causa cambios en los tejidos pigmentados. Los cambios informados con mayor frecuencia han sido el aumento de la pigmentación del iris, el tejido periorbitario (párpado) y las pestañas. Se espera que la pigmentación aumente mientras se administre latanoprost.
El cambio de pigmentación se debe a un mayor contenido de melanina en los melanocitos más que a un aumento en el número de melanocitos. Después de suspender el tratamiento con latanoprost, es probable que la pigmentación del iris sea permanente, mientras que se ha informado que la pigmentación del tejido periorbitario y los cambios en las pestañas son reversibles en algunos pacientes. Los pacientes que reciben tratamiento deben ser informados de la posibilidad de un aumento de la pigmentación. Más allá de los 5 años, se desconocen los efectos del aumento de la pigmentación [ver Estudios clínicos ].
Es posible que el cambio de color del iris no se note durante varios meses o años. Por lo general, la pigmentación marrón alrededor de la pupila se extiende concéntricamente hacia la periferia del iris y todo el iris o partes del iris se vuelven más marrones. Ni los nevos ni las pecas del iris parecen verse afectados por el tratamiento. Si bien el tratamiento con XALATAN 2,5 ml puede continuarse en pacientes que desarrollen un aumento notable de la pigmentación del iris, estos pacientes deben ser examinados con regularidad [ver INFORMACIÓN DEL PACIENTE ].
Cambios de pestañas
XALATAN 2,5 ml puede cambiar gradualmente las pestañas y el vello del ojo tratado; estos cambios incluyen mayor longitud, grosor, pigmentación, número de pestañas o pelos y crecimiento mal dirigido de las pestañas. Los cambios en las pestañas suelen ser reversibles al suspender el tratamiento [ver INFORMACIÓN DEL PACIENTE ].
Inflamación Intraocular
XALATAN 2,5 ml debe usarse con precaución en pacientes con antecedentes de inflamación intraocular (iritis/uveítis) y, en general, no debe usarse en pacientes con inflamación intraocular activa porque la inflamación puede exacerbarse.
Edema macular
Se ha informado edema macular, incluido edema macular cistoide, durante el tratamiento con XALATAN. XALATAN 2,5 ml debe usarse con precaución en pacientes afáquicos, en pacientes pseudofáquicos con una cápsula posterior del cristalino desgarrada o en pacientes con factores de riesgo conocidos de edema macular.
Queratitis herpética
Se ha informado la reactivación de la queratitis por herpes simplex durante el tratamiento con XALATAN. XALATAN 2,5 ml debe utilizarse con precaución en pacientes con antecedentes de queratitis herpética. Debe evitarse XALATAN 2,5 ml en casos de queratitis activa por herpes simple porque la inflamación puede exacerbarse.
queratitis bacteriana
Ha habido informes de queratitis bacteriana asociada con el uso de envases de dosis múltiples de productos oftálmicos tópicos. Estos envases habían sido contaminados inadvertidamente por pacientes que, en la mayoría de los casos, tenían una enfermedad corneal concurrente o una alteración de la superficie epitelial ocular [ver INFORMACIÓN DEL PACIENTE ].
Usar con lentes de contacto
Los lentes de contacto se deben quitar antes de la administración de XALATAN y se pueden volver a colocar 15 minutos después de la administración.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
Latanoprost no fue cancerígeno ni en ratones ni en ratas cuando se administró por sonda oral en dosis de hasta 170 mcg/kg/día (aproximadamente 2800 veces la dosis máxima recomendada en humanos) durante 20 y 24 meses, respectivamente.
Latanoprost no fue mutagénico en bacterias, en linfoma de ratón o en pruebas de micronúcleo de ratón. Se observaron aberraciones cromosómicas in vitro con linfocitos humanos. Los estudios adicionales in vitro e in vivo sobre la síntesis de ADN no programada en ratas fueron negativos.
No se ha encontrado que latanoprost tenga ningún efecto sobre la fertilidad masculina o femenina en estudios con animales.
Uso en poblaciones específicas
El embarazo
Efectos teratogénicos
Embarazo Categoría C.
Se han realizado estudios de reproducción en ratas y conejos. En conejos, una incidencia de 4 de 16 madres no tuvieron fetos viables a una dosis que fue aproximadamente 80 veces la dosis máxima en humanos, y la dosis no embriocida más alta en conejos fue aproximadamente 15 veces la dosis máxima en humanos.
No existen estudios adecuados y bien controlados en mujeres embarazadas. XALATAN 2,5 ml debe usarse durante el embarazo solo si el beneficio potencial justifica el riesgo potencial para el feto.
Madres lactantes
No se sabe si este fármaco o sus metabolitos se excretan en la leche humana. Debido a que muchos medicamentos se excretan en la leche humana, se debe tener precaución cuando se administre XALATAN 2,5 ml a mujeres lactantes.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos.
Uso geriátrico
No se han observado diferencias generales en la seguridad o la eficacia entre los pacientes de edad avanzada y los más jóvenes.
SOBREDOSIS
La infusión intravenosa de hasta 3 mcg/kg en voluntarios sanos produjo concentraciones plasmáticas medias 200 veces mayores que durante el tratamiento clínico y no se observaron reacciones adversas. Las dosis intravenosas de 5,5 a 10 mcg/kg causaron dolor abdominal, mareos, fatiga, sofocos, náuseas y sudoración. Si ocurre una sobredosis con XALATAN, el tratamiento debe ser sintomático.
CONTRAINDICACIONES
Hipersensibilidad conocida al latanoprost, al cloruro de benzalconio o a cualquier otro componente de este producto.
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
Latanoprost es un agonista del receptor FP selectivo de prostanoides que se cree que reduce la presión intraocular (PIO) al aumentar la salida del humor acuoso. Los estudios en animales y en el hombre sugieren que el principal mecanismo de acción es el aumento del flujo de salida uveoescleral. La PIO elevada representa un factor de riesgo importante para la pérdida del campo glaucomatoso. Cuanto mayor sea el nivel de PIO, mayor será la probabilidad de daño del nervio óptico y pérdida del campo visual.
Farmacodinámica
La reducción de la PIO en el hombre comienza alrededor de 3 a 4 horas después de la administración y el efecto máximo se alcanza después de 8 a 12 horas. La reducción de la PIO está presente durante al menos 24 horas.
Farmacocinética
Absorción
El latanoprost se absorbe a través de la córnea, donde el profármaco de éster isopropílico se hidroliza a la forma ácida para volverse biológicamente activo.
Distribución
El volumen de distribución en humanos es de 0,16 ± 0,02 L/kg. La acidez de latanoprost puede medirse en humor acuoso durante las primeras 4 horas, y en plasma sólo durante la primera hora después de la administración local. Los estudios en humanos indican que la concentración máxima en el humor acuoso se alcanza aproximadamente dos horas después de la administración tópica.
Metabolismo
Latanoprost, un profármaco de éster isopropílico, es hidrolizado por esterasas en la córnea al ácido biológicamente activo. El ácido activo de latanoprost que llega a la circulación sistémica se metaboliza principalmente en el hígado a los metabolitos 1,2-dinor y 1,2,3,4-tetranor a través de la β-oxidación de ácidos grasos.
Excreción
La eliminación del ácido de latanoprost del plasma humano es rápida (t½ = 17 min) después de la administración intravenosa y tópica. El aclaramiento sistémico es de aproximadamente 7 ml/min/kg. Tras la β-oxidación hepática, los metabolitos se eliminan principalmente por vía renal. Aproximadamente el 88 % y el 98 % de la dosis administrada se recupera en la orina después de la administración tópica e intravenosa, respectivamente.
Estudios clínicos
PIO basal elevada
Los pacientes con una PIO inicial media de 24 - 25 mmHg que fueron tratados durante 6 meses en ensayos multicéntricos, aleatorizados y controlados demostraron reducciones de la PIO de 6 - 8 mmHg. Esta reducción de la PIO con XALATAN 0,005 % administrado una vez al día fue equivalente al efecto de timolol al 0,5 % administrado dos veces al día.
Progresión del aumento de la pigmentación del iris
Se realizó un estudio de seguridad prospectivo abierto de 3 años con una fase de extensión de 2 años para evaluar la progresión del aumento de la pigmentación del iris con el uso continuo de XALATAN una vez al día como terapia adyuvante en 519 pacientes con glaucoma de ángulo abierto. El análisis se basó en la población de casos observados de los 380 pacientes que continuaban en la fase de extensión.
Los resultados mostraron que el inicio de un aumento notable de la pigmentación del iris ocurrió dentro del primer año de tratamiento para la mayoría de los pacientes que desarrollaron un aumento notable de la pigmentación del iris. Los pacientes continuaron mostrando signos de aumento de la pigmentación del iris durante los cinco años del estudio. La observación del aumento de la pigmentación del iris no afectó la incidencia, la naturaleza o la gravedad de los eventos adversos (aparte del aumento de la pigmentación del iris) registrados en el estudio. La reducción de la PIO fue similar independientemente del desarrollo de una mayor pigmentación del iris durante el estudio.
INFORMACIÓN DEL PACIENTE
Potencial de pigmentación
Advierta a los pacientes sobre la posibilidad de un aumento de la pigmentación marrón del iris, que puede ser permanente. Informar a los pacientes sobre la posibilidad de oscurecimiento de la piel de los párpados, que puede ser reversible después de la interrupción de XALATAN [ver ADVERTENCIAS Y PRECAUCIONES ].
Potencial de cambios en las pestañas
Informe a los pacientes sobre la posibilidad de cambios en las pestañas y el vello del ojo tratado durante el tratamiento con XALATAN. Estos cambios pueden resultar en una disparidad entre los ojos en cuanto a longitud, grosor, pigmentación, número de pestañas o vellos y/o dirección del crecimiento de las pestañas. Los cambios en las pestañas suelen ser reversibles al suspender el tratamiento.
Manejo del contenedor
Indique a los pacientes que eviten que la punta del recipiente dispensador entre en contacto con el ojo o las estructuras circundantes porque esto podría causar que la punta se contamine con bacterias comunes que se sabe que causan infecciones oculares. El uso de soluciones contaminadas puede ocasionar daños oculares graves y la subsiguiente pérdida de la visión [ver ADVERTENCIAS Y PRECAUCIONES ].
Cuándo buscar el consejo de un médico
Aconseje a los pacientes que si desarrollan una afección ocular intercurrente (p. ej., traumatismo o infección) o se someten a una cirugía ocular, o si desarrollan cualquier reacción ocular, en particular conjuntivitis y reacciones en los párpados, deben buscar de inmediato el consejo de su médico sobre el uso continuado de la dosis múltiple. envase.
Usar con lentes de contacto
Informe a los pacientes que XALATAN 2,5 ml contiene cloruro de benzalconio, que puede ser absorbido por lentes de contacto. Las lentes de contacto deben quitarse antes de la administración de la solución. Los lentes se pueden reinsertar 15 minutos después de la administración de XALATAN.
Uso con otras drogas oftálmicas
Si se usa más de un fármaco oftálmico tópico, los fármacos deben administrarse al menos con cinco (5) minutos de diferencia.
