Microzide 25mg Hydrochlorothiazide Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Microzide 25 mg y cómo se usa?
Microzide es un medicamento recetado que se usa para tratar los síntomas de la presión arterial alta (hipertensión) y la hinchazón (edema). Microzide se puede usar solo o con otros medicamentos.
Microzide pertenece a una clase de medicamentos llamados diuréticos, tiazida.
No se sabe si Microzide es seguro y eficaz en niños menores de 6 meses de edad.
¿Cuáles son los posibles efectos secundarios de Microzide?
Microzide puede causar efectos secundarios graves, que incluyen:
- aturdimiento,
- dolor de ojo,
- problemas de la vista,
- coloración amarillenta de la piel o los ojos (ictericia),
- piel pálida,
- moretones con facilidad,
- sangrado inusual (nariz, boca, vagina o recto),
- dificultad para respirar,
- sibilancias,
- tos con mucosidad espumosa,
- Dolor de pecho,
- boca seca,
- sed,
- somnolencia,
- falta de energía,
- inquietud,
- dolor o debilidad muscular,
- frecuencia cardíaca rápida,
- náuseas,
- vómitos,
- poca o ninguna orina,
- fiebre,
- dolor de garganta,
- hinchazón en la cara o la lengua,
- ardiendo en tus ojos, y
- dolor en la piel seguido de una erupción cutánea roja o morada que se extiende (especialmente en la cara o la parte superior del cuerpo) y causa ampollas y descamación
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Microzide incluyen:
- náuseas,
- vómitos,
- pérdida de apetito,
- Diarrea,
- estreñimiento,
- espasmo muscular,
- mareos, y
- dolor de cabeza
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Microzide. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
DESCRIPCIÓN
MICROZIDE® (hidroclorotiazida, USP 12,5 mg) es el derivado 3,4-dihidro de la clorotiazida. Su nombre químico es 6-cloro-3,4-dihidro-2H-1,2,4-benzotiadiazina-7-sulfonamida 1,1-dióxido. Su fórmula empírica es C7H8CIN304S2; su peso molecular es 297,74; y su fórmula estructural es:
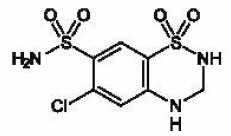
Es un polvo cristalino blanco o casi blanco que es ligeramente soluble en agua, pero muy soluble en solución de hidróxido de sodio.
MICROZIDE (cápsula de hidroclorotiazida) se suministra en cápsulas de 12,5 mg para uso oral.
Ingredientes inactivos : dióxido de silicio coloidal, almidón de maíz, lactosa monohidrato, estearato de magnesio. Las cápsulas de gelatina contienen D&C Red No. 28, D&C Yellow No. 10, FD&C Blue No. 1, gelatina, dióxido de titanio. Las cápsulas están impresas con tinta comestible que contiene óxido de hierro negro, D&C Yellow No. 10, FD&C Blue No. 1, FD&C Blue No. 2, FD&C Red No. 40.
INDICACIONES
MICROZIDE (cápsula de hidroclorotiazida) está indicado en el tratamiento de la hipertensión como agente terapéutico único o en combinación con otros antihipertensivos. A diferencia de los productos diuréticos combinados ahorradores de potasio, MICROZIDE (cápsula de hidroclorotiazida) se puede usar en aquellos pacientes en los que no se corre el riesgo de desarrollar hiperpotasemia, incluidos los pacientes que toman inhibidores de la ECA.
Uso en el embarazo
El uso rutinario de diuréticos en una mujer por lo demás sana es inapropiado y expone a la madre y al feto a peligros innecesarios. Los diuréticos no previenen el desarrollo de la toxemia del embarazo y no existe evidencia satisfactoria de que sean útiles en el tratamiento de la toxemia desarrollada.
El edema durante el embarazo puede surgir por causas patológicas o por las consecuencias fisiológicas y mecánicas del embarazo. Los diuréticos están indicados en el embarazo cuando el edema se debe a causas patológicas, al igual que en ausencia de embarazo. El edema dependiente en el embarazo que resulta de la restricción del retorno venoso por el útero expandido se trata adecuadamente mediante la elevación de las extremidades inferiores y el uso de medias de soporte; el uso de diuréticos para disminuir el volumen intravascular en este caso es ilógico e innecesario. Hay hipervolemia durante el embarazo normal que no es perjudicial ni para el feto ni para la madre (en ausencia de enfermedad cardiovascular), pero que se asocia con edema, incluido el edema generalizado en la mayoría de las mujeres embarazadas. Si este edema produce incomodidad, una mayor decúbito a menudo proporcionará alivio. En casos raros, este edema puede causar una incomodidad extrema que no se alivia con el descanso. En estos casos, un curso corto de diuréticos puede proporcionar alivio y puede ser apropiado.
DOSIFICACIÓN Y ADMINISTRACIÓN
Para el Control de la Hipertensión : La dosis inicial para adultos de MICROZIDE (cápsula de hidroclorotiazida) es una cápsula administrada una vez al día, ya sea que se administre sola o en combinación con otros antihipertensivos. No se recomiendan dosis diarias totales superiores a 50 mg.
CÓMO SUMINISTRADO
MICROZIDE (cápsula de hidroclorotiazida) Cápsulas son cápsulas de gelatina dura de dos piezas #4 verde azulado opaco/verde azulado opaco impresas con MICROZIDE (cápsula de hidroclorotiazida) y 12,5 mg en tinta negra. Se suministran en botes de 100 con cierre de seguridad para niños ( CDN 52544-622-01).
Dispense en un recipiente hermético resistente a la luz como se define en la USP.
Mantener fuera del alcance de los niños.
Almacenar a 20°-25°C (68°-77°F). [Consulte Temperatura ambiente controlada por la USP.] Proteger de la luz, la humedad, el congelamiento, -20 °C (-4 °F). Mantener el contenedor bien cerrado.
Dirija las consultas médicas a: WATSON., Medical Communications PO Box 1953, Morristown, NJ 07962-1953. 800-272-5525. Fabricado por: Watson Pharma Private Limited. Verna, Salcette, Goa 403 722 INDIA. Distribuido por: Watson Pharma, Inc. Morristown, NJ 07962 EE. UU. Revisado: febrero de 2011EFECTOS SECUNDARIOS
Se ha demostrado que las reacciones adversas asociadas con hidroclorotiazida están relacionadas con la dosis. En ensayos clínicos controlados, los eventos adversos informados con dosis de 12,5 mg de hidroclorotiazida una vez al día fueron comparables a los del placebo. Se informaron las siguientes reacciones adversas para dosis de hidroclorotiazida de 25 mg y mayores y, dentro de cada categoría, se enumeran en orden decreciente de gravedad.
cuerpo como un todo : Debilidad.
Cardiovascular : Hipotensión, incluida la hipotensión ortostática (puede agravarse con el alcohol, los barbitúricos, los narcóticos o los fármacos antihipertensivos).
Digestivo Pancreatitis, ictericia (ictericia colestática intrahepática), diarrea, vómitos, sialoadenitis, calambres, estreñimiento, irritación gástrica, náuseas, anorexia.
hematológico : anemia aplásica, agranulocitosis, leucopenia, anemia hemolítica, trombocitopenia.
Hipersensibilidad : Reacciones anafilácticas, vasculitis necrosante (vasculitis y vasculitis cutánea), dificultad respiratoria incluyendo neumonitis y edema pulmonar, fotosensibilidad, fiebre, urticaria, erupción, púrpura.
Metabólico : Desequilibrio electrolítico (ver PRECAUCIONES ), hiperglucemia, glucosuria, hiperuricemia.
musculoesquelético : Espasmo muscular.
Sistema Nervioso/Psiquiátrico : Vértigo, parestesia, mareo, dolor de cabeza, inquietud.
Renal : Insuficiencia renal, disfunción renal, nefritis intersticial (ver ADVERTENCIAS ).
Piel : Eritema multiforme, incluido el síndrome de Stevens-Johnson, dermatitis exfoliativa, incluida la necrólisis epidérmica tóxica, alopecia.
Sentidos especiales Visión borrosa transitoria, xantopsia.
urogenital : Impotencia.
Siempre que las reacciones adversas sean moderadas o graves, se debe reducir la dosis de tiazida o suspender el tratamiento.
INTERACCIONES CON LA DROGAS
Cuando se administran al mismo tiempo, los siguientes medicamentos pueden interactuar con los diuréticos tiazídicos:
Alcohol, barbitúricos o narcóticos - Puede producirse una potenciación de la hipotensión ortostática.
Medicamentos antidiabéticos - (agentes orales e insulina) puede ser necesario ajustar la dosis del fármaco antidiabético.
Otros medicamentos antihipertensivos - efecto aditivo o potenciación.
Resinas de colestiramina y colestipol - Las resinas de colestiramina y colestipol se unen a la hidroclorotiazida y reducen su absorción en el tracto gastrointestinal hasta en un 85 y un 43 por ciento, respectivamente.
Corticosteroide, ACTH - Depleción intensificada de electrolitos, en particular hipopotasemia.
Aminas presoras (p. ej., norepinefrina) - Posible disminución de la respuesta a las aminas presoras, pero no suficiente para descartar su uso.
Relajantes del músculo esquelético, no despolarizantes (p. ej., tubocurarina) posible aumento de la capacidad de respuesta al relajante muscular.
Litio - generalmente no debe administrarse con diuréticos. Los agentes diuréticos reducen el aclaramiento renal de litio y aumentan en gran medida el riesgo de toxicidad por litio. Consulte el prospecto de las preparaciones de litio antes de usar dichas preparaciones con MICROZIDE (cápsula de hidroclorotiazida) .
Fármacos anti-inflamatorios no esteroideos - En algunos pacientes, la administración de un agente antiinflamatorio no esteroideo puede reducir los efectos diuréticos, natriuréticos y antihipertensivos de los diuréticos de asa, ahorradores de potasio y tiazídicos. Cuando MICROZIDE (cápsula de hidroclorotiazida) y agentes antiinflamatorios no esteroideos se usan concomitantemente, se debe observar de cerca a los pacientes para determinar si se obtiene el efecto deseado del diurético.
Interacciones entre medicamentos y pruebas de laboratorio
Las tiazidas deben interrumpirse antes de realizar pruebas de función paratiroidea (ver PRECAUCIONES Generales ).
ADVERTENCIAS
Diabetes e hipoglucemia: La diabetes mellitus latente puede manifestarse y los pacientes diabéticos que reciben tiazidas pueden requerir un ajuste de la dosis de insulina.
Enfermedad renal: Los efectos acumulativos de las tiazidas pueden desarrollarse en pacientes con insuficiencia renal. En tales pacientes, las tiazidas pueden precipitar azotemia.
PRECAUCIONES
Estado de equilibrio de líquidos y electrolitos
En estudios publicados, la hipopotasemia clínicamente significativa ha sido consistentemente menos común en pacientes que recibieron 12,5 mg de hidroclorotiazida que en pacientes que recibieron dosis más altas. No obstante, se debe realizar una determinación periódica de electrolitos séricos en pacientes que puedan estar en riesgo de desarrollar hipopotasemia. Se debe observar a los pacientes en busca de signos de alteraciones de líquidos o electrolitos, es decir, hiponatremia, alcalosis hipoclorémica, hipopotasemia e hipomagnesemia.
Los signos o síntomas de advertencia de desequilibrio de líquidos y electrolitos incluyen sequedad de boca, sed, debilidad, letargo, somnolencia, inquietud, dolores o calambres musculares, fatiga muscular, hipotensión, oliguria, taquicardia y trastornos gastrointestinales como náuseas y vómitos.
Puede desarrollarse hipopotasemia, especialmente con diuresis intensa cuando hay cirrosis severa, durante el uso concomitante de corticosteroides u hormona adrenocorticotrópica (ACTH) o después de una terapia prolongada. La interferencia con la ingesta adecuada de electrolitos por vía oral también contribuirá a la hipopotasemia. La hipopotasemia y la hipomagnesemia pueden provocar arritmias ventriculares o sensibilizar o exagerar la respuesta del corazón a los efectos tóxicos de los digitálicos. La hipopotasemia se puede evitar o tratar con suplementos de potasio o una mayor ingesta de alimentos ricos en potasio.
La hiponatremia por dilución pone en riesgo la vida y puede ocurrir en pacientes edematosos cuando hace calor; el tratamiento apropiado es la restricción de agua en lugar de la administración de sal, excepto en raras ocasiones cuando la hiponatremia pone en peligro la vida. En la depleción real de sal, el reemplazo apropiado es la terapia de elección.
Hiperuricemia
La hiperuricemia o la gota aguda pueden precipitarse en ciertos pacientes que reciben diuréticos tiazídicos.
Función hepática deteriorada
Las tiazidas deben utilizarse con precaución en pacientes con insuficiencia hepática. Pueden precipitar coma hepático en pacientes con enfermedad hepática grave.
Enfermedad paratiroidea
Las tiazidas disminuyen la excreción de calcio y se han observado cambios patológicos en las glándulas paratiroides, con hipercalcemia e hipofosfatemia, en algunos pacientes que reciben tratamiento prolongado con tiazidas.
Carcinogénesis, mutagénesis, deterioro de la fertilidad
Los estudios de alimentación de dos años en ratones y ratas realizados bajo los auspicios del Programa Nacional de Toxicología (NTP) no revelaron evidencia de un potencial carcinogénico de hidroclorotiazida en ratones hembra (en dosis de hasta aproximadamente 600 mg/kg/día) o en machos. y ratas hembra (a dosis de aproximadamente 100 mg/kg/día). El NTP, sin embargo, encontró evidencia equívoca de hepatocarcinogenicidad en ratones macho. La hidroclorotiazida no fue genotóxica in vitro en el ensayo de mutagenicidad de Ames de las cepas TA 98, TA 100, TA 1535, TA 1537 y TA 1538 de Salmonella typhimurium y en la prueba de ovario de hámster chino (CHO) para aberraciones cromosómicas, ni en ensayos in vivo utilizando cromosomas de células germinales de ratón, cromosomas de médula ósea de hámster chino y el gen de rasgo letal recesivo ligado al sexo de Drosophila. Solo se obtuvieron resultados positivos en los ensayos in vitro de intercambio de cromátidas hermanas CHO (clastogenicidad) y en células de linfoma de ratón (mutagenicidad), usando concentraciones de hidroclorotiazida de 43 a 1300 mcg/mL, y en el ensayo de no disyunción de Aspergillus nidulans en una concentración no especificada.
La hidroclorotiazida no tuvo efectos adversos sobre la fertilidad de ratones y ratas de ambos sexos en estudios en los que estas especies fueron expuestas, a través de su dieta, a dosis de hasta 100 y 4 mg/kg, respectivamente, antes de la concepción y durante la gestación.
El embarazo
Efectos teratogénicos
Embarazo Categoría B: Los estudios en los que se administró hidroclorotiazida por vía oral a ratas y ratones preñados durante sus respectivos períodos de mayor organogénesis en dosis de hasta 3000 y 1000 mg de hidroclorotiazida/kg, respectivamente, no proporcionaron evidencia de daño al feto.
Sin embargo, no existen estudios adecuados y bien controlados en mujeres embarazadas. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, este medicamento debe usarse durante el embarazo solo si es claramente necesario.
Efectos no teratogénicos
Las tiazidas atraviesan la barrera placentaria y aparecen en la sangre del cordón umbilical. Existe el riesgo de ictericia fetal o neonatal, trombocitopenia y posiblemente otras reacciones adversas que han ocurrido en adultos.
Madres lactantes
Las tiazidas se excretan en la leche materna. Debido al potencial de reacciones adversas graves en los lactantes, se debe tomar la decisión de suspender la lactancia o suspender la hidroclorotiazida, teniendo en cuenta la importancia del fármaco para la madre.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos.
Uso de ancianos
Se puede observar una mayor reducción de la presión arterial y un aumento de los efectos secundarios en pacientes de edad avanzada (es decir, mayores de 65 años) con hidroclorotiazida. Por lo tanto, se recomienda iniciar el tratamiento con la dosis más baja disponible de hidroclorotiazida (12,5 mg). Si se requiere una titulación adicional, se deben utilizar incrementos de 12,5 mg.
SOBREDOSIS
Los signos y síntomas más comunes observados son los causados por la depleción de electrolitos (hipopotasemia, hipocloremia, hiponatremia) y la deshidratación resultante de una diuresis excesiva. Si también se ha administrado digitálicos, la hipopotasemia puede acentuar las arritmias cardíacas.
En caso de sobredosis, se deben emplear medidas sintomáticas y de apoyo. Debe inducirse la emesis o realizarse un lavado gástrico. Corregir la deshidratación, el desequilibrio electrolítico, el coma hepático y la hipotensión mediante los procedimientos establecidos. Si es necesario, administre oxígeno o respiración artificial para la insuficiencia respiratoria. No se ha establecido el grado en que la hidroclorotiazida se elimina por hemodiálisis.
La DL50 oral de hidroclorotiazida es superior a 10 g/kg en ratones y ratas.
CONTRAINDICACIONES
La hidroclorotiazida está contraindicada en pacientes con anuria. También está contraindicada la hipersensibilidad a este producto oa otros fármacos derivados de las sulfonamidas.
FARMACOLOGÍA CLÍNICA
La hidroclorotiazida bloquea la reabsorción de iones de sodio y cloruro y, por lo tanto, aumenta la cantidad de sodio que atraviesa el túbulo distal y el volumen de agua excretado. Una porción del sodio adicional presentado al túbulo distal se intercambia allí por iones de potasio e hidrógeno. Con el uso continuado de hidroclorotiazida y la depleción de sodio, los mecanismos compensatorios tienden a aumentar este intercambio y pueden producir una pérdida excesiva de iones de potasio, hidrógeno y cloruro. La hidroclorotiazida también disminuye la excreción de calcio y ácido úrico, puede aumentar la excreción de yoduro y puede reducir la tasa de filtración glomerular. Se ha demostrado que las toxicidades metabólicas asociadas con cambios electrolíticos excesivos causados por hidroclorotiazida están relacionadas con la dosis.
Farmacocinética y Metabolismo
La hidroclorotiazida se absorbe bien (65% a 75%) luego de la administración oral. La absorción de hidroclorotiazida se reduce en pacientes con insuficiencia cardíaca congestiva.
Las concentraciones plasmáticas máximas se observan entre 1 y 5 horas después de la dosificación y oscilan entre 70 y 490 ng/ml después de dosis orales de 12,5 a 100 mg. Las concentraciones plasmáticas están linealmente relacionadas con la dosis administrada. Las concentraciones de hidroclorotiazida son de 1,6 a 1,8 veces mayores en sangre total que en plasma. Se ha informado que la unión a proteínas séricas es de aproximadamente 40% a 68%. Se ha informado que la vida media de eliminación plasmática es de 6 a 15 horas. La hidroclorotiazida se elimina principalmente por vía renal. Después de dosis orales de 12,5 a 100 mg, del 55 % al 77 % de la dosis administrada aparece en la orina y más del 95 % de la dosis absorbida se excreta en la orina como fármaco inalterado. En pacientes con enfermedad renal, las concentraciones plasmáticas de hidroclorotiazida aumentan y la vida media de eliminación se prolonga.
Cuando MICROZIDE (cápsula de hidroclorotiazida) se administra con alimentos, su biodisponibilidad se reduce en un 10 %, la concentración plasmática máxima se reduce en un 20 % y el tiempo hasta la concentración máxima aumenta de 1,6 a 2,9 horas.
Farmacodinámica
Se cree que los efectos antihipertensivos agudos de las tiazidas se deben a una reducción del volumen sanguíneo y del gasto cardíaco, secundaria a un efecto natriurético, aunque también se ha propuesto un mecanismo vasodilatador directo. Con la administración crónica, el volumen plasmático vuelve a la normalidad, pero disminuye la resistencia vascular periférica. Se desconoce el mecanismo exacto del efecto antihipertensivo de la hidroclorotiazida.
Las tiazidas no afectan la presión arterial normal. El inicio de la acción ocurre dentro de las 2 horas posteriores a la dosificación, el efecto máximo se observa alrededor de las 4 horas y la actividad persiste hasta por 24 horas.
Estudios clínicos
En un ensayo de grupos paralelos, doble ciego, controlado con placebo, de 87 pacientes, de 4 semanas de duración, los pacientes que recibieron MICROZIDE (cápsula de hidroclorotiazida) tuvieron reducciones en la presión arterial sistólica y diastólica sentados que fueron significativamente mayores que las observadas en los pacientes que recibieron placebo. En ensayos controlados con placebo publicados que compararon 12,5 mg de hidroclorotiazida con 25 mg, la dosis de 12,5 mg conservó la mayor parte de la reducción de la presión arterial corregida con placebo observada con 25 mg.
INFORMACIÓN DEL PACIENTE
No se proporcionó información. por favor refiérase a ADVERTENCIAS y PRECAUCIONES secciones.
