Mircette 0.15/0.02 mg Desogestrel Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Mircette 0,15 mg y cómo se usa?
Mircette es un medicamento recetado que se usa como método anticonceptivo para prevenir el embarazo. Mircette se puede usar solo o con otros medicamentos.
Mircette pertenece a una clase de medicamentos llamados estrógenos/progestágenos; Anticonceptivos Orales.
No se sabe si Mircette es seguro y efectivo en niños antes de la menarquia.
¿Cuáles son los posibles efectos secundarios de Mircette?
Mircette puede causar efectos secundarios graves que incluyen:
- urticaria,
- respiración dificultosa,
- hinchazón de la cara, los labios, la lengua o la garganta,
- entumecimiento o debilidad repentinos (especialmente en un lado del cuerpo),
- dolor de cabeza intenso y repentino,
- dificultad para hablar,
- problemas con la visión o el equilibrio,
- pérdida repentina de la visión,
- dolor punzante en el pecho,
- dificultad para respirar,
- tosiendo sangre,
- dolor o calor en una o ambas piernas,
- dolor o presión en el pecho,
- dolor que se extiende a la mandíbula o al hombro,
- náuseas,
- transpiración,
- pérdida de apetito,
- dolor de estómago superior,
- cansancio,
- fiebre,
- orina oscura,
- heces de color arcilla,
- coloración amarillenta de la piel o los ojos (ictericia),
- dolor de cabeza intenso,
- visión borrosa,
- latidos en el cuello o las orejas,
- hinchazón en las manos, los tobillos o los pies,
- cambios en el patrón o la gravedad de las migrañas,
- bulto en el pecho,
- problemas para dormir,
- debilidad,
- sensación de cansancio y
- cambios de humor
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Mircette incluyen:
- náuseas,
- vómitos (especialmente cuando empiece a tomar este medicamento por primera vez),
- sensibilidad en los senos,
- sangrado por disrupción,
- acné,
- oscurecimiento de la piel del rostro,
- aumento de peso, y
- problemas con lentes de contacto
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Mircette. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
Se debe advertir a los pacientes que este producto no protege contra la infección por VIH (SIDA) y otras enfermedades de transmisión sexual.
DESCRIPCIÓN
Las tabletas Mircette® (desogestrel/etinilestradiol y etinilestradiol) brindan un régimen anticonceptivo oral de 21 tabletas blancas y redondas, cada una de las cuales contiene 0.15 mg de desogestrel (13-etil11-metileno-18,19-dinor-17 alfa-preg-4-en-20). -yn-17-ol), 0,02 mg de etinilestradiol (19-nor17 alfa-pregna-1,3,5 (10)-trien-20-yne-3,17-diol) e ingredientes inactivos que incluyen dióxido de silicio coloidal , hipromelosa, lactosa monohidrato, polietilenglicol, povidona, almidón pregelatinizado, ácido esteárico y vitamina E, seguido de 2 comprimidos redondos inertes de color verde claro con los siguientes ingredientes inactivos: FD&C azul no. 1 laca de aluminio, FD &C amarillo no. 6 lago de aluminio, D&C amarillo no. 10 laca de aluminio, lactosa monohidrato, estearato de magnesio, celulosa microcristalina y almidón pregelatinizado. Mircette® también contiene 5 comprimidos redondos amarillos que contienen 0,01 mg de etinilestradiol (19-nor-17 alfa-pregna-1,3,5 (10)-trien-20-yne3,17-diol) e ingredientes inactivos que incluyen dióxido de silicio coloidal , D&C amarillo no. 10, lago de aluminio, FD&C amarillo no. 6 laca de aluminio, hipromelosa, lactosa monohidrato, polietilenglicol, povidona, polisorbato 80, almidón pregelatinizado, ácido esteárico, dióxido de titanio y vitamina E. Los pesos moleculares de desogestrel y etinilestradiol son 310,48 y 296,40 respectivamente. Las fórmulas estructurales son las siguientes:
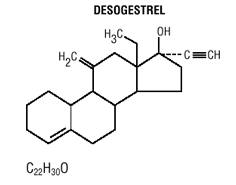
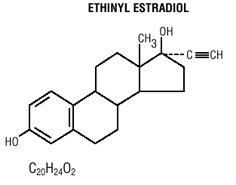
INDICACIONES
Mircette® (desogestrel/etinilestradiol y etinilestradiol) Las tabletas están indicadas para la prevención del embarazo en mujeres que eligen usar este producto como método anticonceptivo.
Los anticonceptivos orales son muy eficaces. La Tabla II enumera las tasas típicas de embarazos accidentales para las usuarias de anticonceptivos orales combinados y otros métodos anticonceptivos. La eficacia de estos métodos anticonceptivos, excepto la esterilización, depende de la fiabilidad con la que se utilicen. El uso correcto y consistente de estos métodos puede resultar en tasas de falla más bajas.
TABLA II: Porcentaje de mujeres que experimentan un embarazo no deseado durante el primer año de uso típico y el primer año de uso perfecto de la anticoncepción y el porcentaje que continúa usando al final del primer año, Estados Unidos.
DOSIFICACIÓN Y ADMINISTRACIÓN
Para lograr la máxima eficacia anticonceptiva, las tabletas de Mircette® (desogestrel/etinilestradiol y etinilestradiol) deben tomarse exactamente como se indica ya intervalos que no excedan las 24 horas. Mircette® se puede iniciar usando un inicio de domingo o un inicio del día 1.
NOTA: Cada dispensador de paquetes de ciclo está preimpreso con los días de la semana, comenzando con el domingo, para facilitar un régimen de inicio en domingo. Se proporcionan seis "tiras de etiquetas de días" diferentes con cada dispensador de paquetes de ciclo para adaptarse a un régimen de inicio del Día 1. En este caso, la paciente debe colocar sobre los días preimpresos la “tira de etiqueta del día” autoadhesiva que corresponde a su día de inicio.
IMPORTANTE: Se debe considerar la posibilidad de ovulación y concepción antes de iniciar el uso de Mircette®.
El uso de Mircette® para la anticoncepción puede iniciarse 4 semanas después del parto en mujeres que eligen no amamantar. Cuando los comprimidos se administran durante el puerperio, debe tenerse en cuenta el aumento del riesgo de enfermedad tromboembólica asociada con el puerperio (ver CONTRAINDICACIONES y ADVERTENCIAS sobre la enfermedad tromboembólica. Ver también PRECAUCIONES por Madres lactantes ).
Si la paciente comienza con Mircette® después del parto y aún no ha tenido un período, se le debe indicar que use otro método anticonceptivo hasta que haya tomado una tableta blanca diariamente durante 7 días.
Inicio Domingo
Al iniciar un régimen de inicio dominical, se debe utilizar otro método anticonceptivo hasta después de los primeros 7 días consecutivos de administración.
Si se comienza el domingo, los comprimidos se toman diariamente sin interrupción de la siguiente manera: El primer comprimido blanco debe tomarse el primer domingo después del comienzo de la menstruación (si la menstruación comienza el domingo, el primer comprimido blanco se toma ese día). Se toma un comprimido blanco al día durante 21 días, seguido de 1 comprimido verde claro (inerte) al día durante 2 días y 1 comprimido amarillo (activo) al día durante 5 días. Para todos los ciclos subsiguientes, el paciente comienza un nuevo régimen de 28 tabletas al día siguiente (domingo) después de tomar la última tableta amarilla. [Si cambia de un anticonceptivo oral de inicio dominical, la primera tableta de Mircette® (desogestrel/etinilestradiol y etinilestradiol) debe tomarse el segundo domingo después de la última tableta de un régimen de 21 días o debe tomarse el primer domingo después de la último comprimido inactivo de un régimen de 28 días.]
Si un paciente olvida 1 tableta blanca, debe tomar la tableta olvidada tan pronto como lo recuerde. Si la paciente olvida 2 tabletas blancas consecutivas en la Semana 1 o la Semana 2, la paciente debe tomar 2 tabletas el día que se acuerde y 2 tabletas al día siguiente; a partir de entonces, la paciente debe reanudar la toma de 1 comprimido al día hasta que finalice el paquete del ciclo. Se debe indicar a la paciente que use un método anticonceptivo de respaldo si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras. Si el paciente olvida 2 comprimidos blancos consecutivos en la tercera semana o 3 o más comprimidos blancos seguidos en cualquier momento durante el ciclo, el paciente debe seguir tomando 1 comprimido blanco al día hasta el próximo domingo. El domingo, el paciente debe tirar el resto de ese paquete de ciclo y comenzar un nuevo paquete de ciclo ese mismo día. Se debe indicar a la paciente que use un método anticonceptivo de respaldo si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras.
Inicio del día 1
Contando el primer día de la menstruación como “Día 1”, las tabletas se toman sin interrupción de la siguiente manera: una tableta blanca al día durante 21 días, una tableta verde claro (inerte) al día durante 2 días seguida de 1 tableta amarilla (etinilestradiol) al día durante 5 días. Para todos los ciclos subsiguientes, el paciente comienza un nuevo régimen de 28 tabletas al día siguiente de tomar la última tableta amarilla. [Si se cambia directamente de otro anticonceptivo oral, la primera tableta blanca debe tomarse el primer día de la menstruación que comienza después de la última tableta ACTIVA del producto anterior.]
Si un paciente olvida 1 tableta blanca, debe tomar la tableta olvidada tan pronto como lo recuerde. Si la paciente olvida 2 tabletas blancas consecutivas en la Semana 1 o la Semana 2, la paciente debe tomar 2 tabletas el día que se acuerde y 2 tabletas al día siguiente; a partir de entonces, la paciente debe reanudar la toma de 1 comprimido al día hasta que finalice el paquete del ciclo. Se debe indicar a la paciente que use un método anticonceptivo de respaldo si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras. Si el paciente olvida 2 tabletas blancas consecutivas en la tercera semana o si el paciente olvida 3 o más tabletas blancas seguidas en cualquier momento durante el ciclo, el paciente debe desechar el resto del paquete del ciclo y comenzar un nuevo paquete del ciclo que mismo día. Se debe indicar a la paciente que use un método anticonceptivo de respaldo si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras.
Todos los anticonceptivos orales
El sangrado intermenstrual, el manchado y la amenorrea son motivos frecuentes por los que las pacientes dejan de tomar anticonceptivos orales. En el sangrado intermenstrual, como en todos los casos de sangrado vaginal irregular, hay que tener en cuenta las causas no funcionales. En el sangrado anormal persistente o recurrente de la vagina no diagnosticado, están indicadas medidas diagnósticas adecuadas para descartar embarazo o malignidad. Si se han excluido tanto el embarazo como la patología, el tiempo o el cambio a otra preparación pueden resolver el problema. El cambio a un anticonceptivo oral con un mayor contenido de estrógeno, si bien es potencialmente útil para minimizar la irregularidad menstrual, debe hacerse solo si es necesario, ya que esto puede aumentar el riesgo de enfermedad tromboembólica.
Uso de anticonceptivos orales en caso de ausencia del período menstrual:
CÓMO SUMINISTRADO
Mircette ® (desogestrel/etinilestradiol y etinilestradiol) Las tabletas contienen 21 tabletas blancas redondas, 2 tabletas verdes redondas y 5 tabletas amarillas redondas en un blíster dentro de un dispensador de plástico reciclable. Cada comprimido blanco (grabado con "dp" en un lado y "021" en el otro lado) contiene 0,15 mg de desogestrel y 0,02 mg de etinilestradiol. Cada tableta verde (grabada con "dp" en un lado y "331" en el otro lado) contiene ingredientes inertes. Cada comprimido amarillo (grabado con "dp" en un lado y "457" en el otro lado) contiene 0,01 mg de etinilestradiol.
Cajas de 6 CDN 51285-114-58
Almacenar a 20° a 25°C (68° a 77°F) [Ver Temperatura ambiente controlada por USP ].
REFERENCIAS @sesenta y cinco. Hatcher RA, Trussell J, Stewart F et al. Tecnología anticonceptiva: decimoséptima edición revisada, Nueva York: Irvington Publishers, 1998, en prensa. @sesenta y cinco. Stadel BV. Anticonceptivos orales y enfermedades cardiovasculares. (Pt. 1). N Engl J Med 1981; 305:612–618. @sesenta y cinco. Stadel BV. Anticonceptivos orales y enfermedades cardiovasculares. (Pt. 2). N Engl J Med 1981; 305:672–677. @sesenta y cinco. Shapiro S. Anticonceptivos orales: es hora de hacer un balance. N Engl J Med 1987; 315:450–451. @sesenta y cinco. El estudio sobre el cáncer y las hormonas esteroides de los Centros para el Control de Enfermedades y el Instituto Nacional de Salud Infantil y Desarrollo Humano: uso de anticonceptivos orales y riesgo de cáncer de ovario. JAMA 1983; 249:1596–1599. @sesenta y cinco. El estudio sobre el cáncer y las hormonas esteroides de los Centros para el Control de Enfermedades y el Instituto Nacional de Salud Infantil y Desarrollo Humano: el uso de anticonceptivos orales combinados y el riesgo de cáncer de endometrio. JAMA 1987; 257:796–800. @sesenta y cinco. Ory HW. Quistes ováricos funcionales y anticonceptivos orales: asociación negativa confirmada quirúrgicamente. JAMA 1974; 228:68–69. @sesenta y cinco. Ory HW, Cole P, Macmahon B, Hoover R. Anticonceptivos orales y riesgo reducido de enfermedad mamaria benigna. N Engl J Med 1976; 294:419–422. @sesenta y cinco. Ory HW. La salud no anticonceptiva se beneficia del uso de anticonceptivos orales. Fam Plann Perspect 1982; 14:182–184. @sesenta y cinco. Ory HW, Forrest JD, Lincoln R. Tomando decisiones: Evaluación de los riesgos y beneficios para la salud de los métodos anticonceptivos. Nueva York, Instituto Alan Guttmacher, 1983; pags. 1. @sesenta y cinco. Godsland, I et al. Los efectos de diferentes formulaciones de agentes anticonceptivos orales sobre el metabolismo de lípidos y carbohidratos. N Engl J Med 1990; 323:1375–81. @sesenta y cinco. Kloosterboer, HJ et al. Selectividad en la unión de los receptores de progesterona y andrógenos de los progestágenos utilizados en la anticoncepción oral. Anticoncepción, 1988; 38:325–32. @sesenta y cinco. Van der Vies, J y de Visser, J. Estudios endocrinológicos con desogestrel. Arzneim. Forsch./Drug Res., 1983; 33(l),2:231–6. @sesenta y cinco. Datos en archivo, Organon Inc. @sesenta y cinco. Fotherby, K. Anticonceptivos orales, lípidos y enfermedades cardiovasculares. Anticoncepción, 1985; vol. 31; 4:367–94. @sesenta y cinco. Lawrence, DM et al. Reducción de los niveles de globulina transportadora de hormonas sexuales y testosterona libre derivada en mujeres con acné severo. Endocrinología Clínica, 1981; 15:87–91. @sesenta y cinco. Cullberg, G et al. Efectos de una combinación de dosis bajas de desogestrel y etinilestradiol sobre el hirsutismo, los andrógenos y la globulina transportadora de hormonas sexuales en mujeres con síndrome de ovario poliquístico. Acta Obstet Gynecol Scand, 1985; 64:195–202. @sesenta y cinco. Jung-Hoffmann, C y Kuhl, H. Efectos divergentes de dos anticonceptivos orales de dosis baja sobre la globulina transportadora de hormonas sexuales y la testosterona libre. AJOG, 1987; 156:199–203. @sesenta y cinco. Hammond, G et al. Concentraciones séricas de proteína fijadora de esteroides, distribución de progestágenos y biodisponibilidad de testosterona durante el tratamiento con anticonceptivos que contienen desogestrel o levonorgestrel. fértil. Esteril., 1984; 42:44–51. @sesenta y cinco. Palatsi, R et al. Testosterona sérica total y libre y globulina fijadora de hormonas sexuales (SHBG) en pacientes con acné tratadas con dos anticonceptivos orales diferentes. Acta Derm Venereol, 1984; 64:517–23.Teva Women'S Health, Inc., subsidiaria de Teva Pharmaceuticals USA, Inc. Sellersville, PA 18960. Rev. 06/2012
EFECTOS SECUNDARIOS
Se ha asociado un mayor riesgo de las siguientes reacciones adversas graves con el uso de anticonceptivos orales (ver ADVERTENCIAS sección):
- Tromboflebitis y trombosis venosa con o sin embolia
- Tromboembolismo arterial
- Embolia pulmonar
- Infarto de miocardio
- Hemorragia cerebral
- Trombosis cerebral
- Hipertensión
- Enfermedad de la vesícula
- Adenomas hepáticos o tumores hepáticos benignos
Existe evidencia de una asociación entre las siguientes condiciones y el uso de anticonceptivos orales:
- Trombosis mesentérica
- Trombosis de retina
Se han notificado las siguientes reacciones adversas en pacientes que reciben anticonceptivos orales y se cree que están relacionadas con el medicamento:
- Náuseas
- vómitos
- Síntomas gastrointestinales (como calambres abdominales e hinchazón)
- Sangrado por disrupción
- Punteo
- Cambio en el flujo menstrual
- amenorrea
- Infertilidad temporal tras la suspensión del tratamiento
- Edema
- Melasma que puede persistir
- Cambios en los senos: sensibilidad, agrandamiento, secreción
- Cambio de peso (aumento o disminución)
- Cambio en la erosión y secreción cervical
- Disminución en la lactancia cuando se administra inmediatamente después del parto
- ictericia colestásica
- Migraña
- Erupción (alérgica)
- Depresión mental
- Tolerancia reducida a los carbohidratos.
- candidiasis vaginal
- Cambio en la curvatura de la córnea (empinamiento)
- Intolerancia a las lentes de contacto
Se han notificado las siguientes reacciones adversas en usuarias de anticonceptivos orales y la asociación no se ha confirmado ni refutado:
- Síndrome premenstrual
- cataratas
- Cambios en el apetito
- Síndrome similar a la cistitis
- Dolor de cabeza
- Nerviosismo
- Mareo
- hirsutismo
- Pérdida de cabello del cuero cabelludo
- Eritema multiforme
- Eritema nodoso
- erupción hemorrágica
- vaginitis
- porfiria
- Insuficiencia renal
- Síndrome urémico hemolítico
- Acné
- Cambios en la libido
- Colitis
- Síndrome de Budd-Chiari
INTERACCIONES CON LA DROGAS
La reducción de la eficacia y el aumento de la incidencia de sangrado intermenstrual e irregularidades menstruales se han asociado con el uso concomitante de rifampicina. Se ha sugerido una asociación similar, aunque menos marcada, con barbitúricos, fenilbutazona, fenitoína sódica, carbamazepina y posiblemente con griseofulvina, ampicilina y tetraciclinas (72).
Se ha demostrado que los anticonceptivos hormonales combinados reducen significativamente las concentraciones plasmáticas de lamotrigina cuando se administran conjuntamente, probablemente debido a la inducción de la glucuronidación de lamotrigina. Esto puede reducir el control de las convulsiones; por lo tanto, pueden ser necesarios ajustes de dosis de lamotrigina.
Consulte la etiqueta del fármaco utilizado simultáneamente para obtener más información sobre las interacciones con los anticonceptivos hormonales o la posibilidad de alteraciones enzimáticas.
Interacciones con pruebas de laboratorio
Ciertas pruebas de función endocrina y hepática y componentes sanguíneos pueden verse afectados por los anticonceptivos orales:
ADVERTENCIAS
Fumar cigarrillos aumenta el riesgo de efectos secundarios cardiovasculares graves por el uso de anticonceptivos orales. Este riesgo aumenta con la edad y con el tabaquismo intenso (15 o más cigarrillos al día) y es bastante marcado en mujeres mayores de 35 años. Se debe recomendar enfáticamente a las mujeres que usan anticonceptivos orales que no fumen.
El uso de anticonceptivos orales se asocia con un mayor riesgo de varias afecciones graves, como infarto de miocardio, tromboembolismo, accidente cerebrovascular, neoplasia hepática y enfermedad de la vesícula biliar, aunque el riesgo de morbilidad o mortalidad grave es muy pequeño en mujeres sanas sin factores de riesgo subyacentes. El riesgo de morbilidad y mortalidad aumenta significativamente en presencia de otros factores de riesgo subyacentes, como hipertensión, hiperlipidemias, obesidad y diabetes.
Los profesionales que prescriben anticonceptivos orales deben estar familiarizados con la siguiente información relacionada con estos riesgos.
La información contenida en este prospecto se basa principalmente en estudios realizados en pacientes que usaron anticonceptivos orales con formulaciones de dosis más altas de estrógenos y progestágenos que las de uso común en la actualidad. Queda por determinar el efecto del uso a largo plazo de anticonceptivos orales con formulaciones de dosis más bajas de estrógenos y progestágenos.
lo largo de este etiquetado, los estudios epidemiológicos informados son de dos tipos: estudios retrospectivos o de casos y controles y estudios prospectivos o de cohortes. Los estudios de casos y controles proporcionan una medida del riesgo relativo de una enfermedad, es decir, una relación entre la incidencia de una enfermedad entre las usuarias de anticonceptivos orales y entre las no usuarias. El riesgo relativo no proporciona información sobre la aparición clínica real de una enfermedad. Los estudios de cohortes proporcionan una medida del riesgo atribuible, que es la diferencia en la incidencia de la enfermedad entre usuarias y no usuarias de anticonceptivos orales. El riesgo atribuible proporciona información sobre la ocurrencia real de una enfermedad en la población (Adaptado de las referencias 2 y 3 con el permiso del autor). Para más información, se remite al lector a un texto sobre métodos epidemiológicos.
Trastornos tromboembólicos y otros problemas vasculares
Tromboembolismo
Está bien establecido un mayor riesgo de enfermedad tromboembólica y trombótica asociada con el uso de anticonceptivos orales. Los estudios de casos y controles han encontrado que el riesgo relativo de las usuarias en comparación con las no usuarias es de 3 para el primer episodio de enfermedad tromboembólica venosa superficial, de 4 a 11 para la trombosis venosa profunda o embolia pulmonar, y de 1,5 a 6 para las mujeres con condiciones predisponentes para la enfermedad venosa venosa. enfermedad tromboembólica (2,3,19–24). Los estudios de cohortes han demostrado que el riesgo relativo es algo menor, alrededor de 3 para casos nuevos y alrededor de 4,5 para casos nuevos que requieren hospitalización (25). El riesgo de enfermedad tromboembólica asociada con los anticonceptivos orales no está relacionado con la duración del uso y desaparece una vez que se suspende el uso de la píldora (2).
Varios estudios epidemiológicos indican que los anticonceptivos orales de tercera generación, incluidos los que contienen desogestrel, están asociados con un mayor riesgo de tromboembolismo venoso que ciertos anticonceptivos orales de segunda generación (102–104). En general, estos estudios indican un riesgo aproximadamente dos veces mayor, lo que corresponde a 1 o 2 casos adicionales de tromboembolismo venoso por 10 000 mujeres-año de uso. Sin embargo, los datos de estudios adicionales no han mostrado este doble aumento en el riesgo.
Se ha informado un aumento de dos a cuatro veces en el riesgo relativo de complicaciones tromboembólicas posoperatorias con el uso de anticonceptivos orales (9,26). El riesgo relativo de trombosis venosa en mujeres que tienen condiciones predisponentes es el doble que en mujeres sin tales condiciones médicas (9,26). Si es factible, los anticonceptivos orales deben suspenderse al menos cuatro semanas antes y durante dos semanas después de una cirugía electiva de un tipo asociado con un aumento en el riesgo de tromboembolismo y durante y después de una inmovilización prolongada. Dado que el período posparto inmediato también se asocia con un mayor riesgo de tromboembolismo, los anticonceptivos orales no deben comenzar antes de las cuatro semanas posteriores al parto en mujeres que eligen no amamantar.
Infarto de miocardio
Se ha atribuido un mayor riesgo de infarto de miocardio al uso de anticonceptivos orales. Este riesgo se presenta principalmente en fumadores o mujeres con otros factores de riesgo subyacentes de enfermedad de las arterias coronarias, como hipertensión, hipercolesterolemia, obesidad mórbida y diabetes. Se ha estimado que el riesgo relativo de ataque cardíaco para las usuarias actuales de anticonceptivos orales es de dos a seis (4–10). El riesgo es muy bajo en mujeres menores de 30 años.
Se ha demostrado que fumar en combinación con el uso de anticonceptivos orales contribuye sustancialmente a la incidencia de infarto de miocardio en mujeres de treinta y tantos años o más, y el tabaquismo representa la mayoría de los casos en exceso (11). Se ha demostrado que las tasas de mortalidad asociadas con la enfermedad circulatoria aumentan sustancialmente en las fumadoras mayores de 35 años y las no fumadoras mayores de 40 años (Tabla III) entre las mujeres que usan anticonceptivos orales.
TABLA III: TASAS DE MORTALIDAD POR ENFERMEDADES CIRCULATORIAS POR 100.000 MUJER AÑOS POR EDAD, TABAQUISMO Y USO DE ANTICONCEPTIVOS ORALES
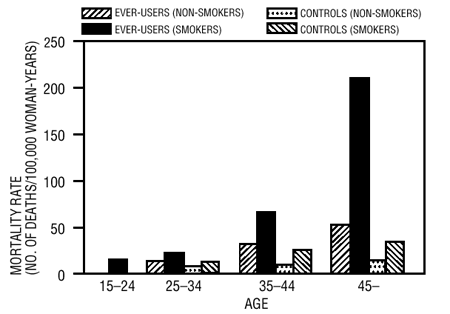
Los anticonceptivos orales pueden agravar los efectos de factores de riesgo bien conocidos, como la hipertensión, la diabetes, las hiperlipidemias, la edad y la obesidad (13). En particular, se sabe que algunos progestágenos reducen el colesterol HDL y causan intolerancia a la glucosa, mientras que los estrógenos pueden crear un estado de hiperinsulinismo (14–18). Se ha demostrado que los anticonceptivos orales aumentan la presión arterial entre las usuarias (ver ADVERTENCIAS ). Se han asociado efectos similares sobre los factores de riesgo con un mayor riesgo de enfermedad cardíaca. Los anticonceptivos orales deben usarse con precaución en mujeres con factores de riesgo de enfermedades cardiovasculares.
Enfermedades cerebrovasculares
Se ha demostrado que los anticonceptivos orales aumentan los riesgos relativos y atribuibles de eventos cerebrovasculares (accidente cerebrovascular trombótico y hemorrágico), aunque, en general, el riesgo es mayor entre las mujeres mayores (>35 años), hipertensas que también fuman. Se encontró que la hipertensión era un factor de riesgo tanto para usuarios como para no usuarios, para ambos tipos de accidentes cerebrovasculares, mientras que fumar interactuaba para aumentar el riesgo de accidentes cerebrovasculares hemorrágicos (27–29).
En un gran estudio, se demostró que el riesgo relativo de accidentes cerebrovasculares trombóticos oscila entre 3 para usuarios normotensos y 14 para usuarios con hipertensión grave (30). Se informa que el riesgo relativo de accidente cerebrovascular hemorrágico es de 1,2 para no fumadoras que usaron anticonceptivos orales, 2,6 para fumadoras que no usaron anticonceptivos orales, 7,6 para fumadoras que usaron anticonceptivos orales, 1,8 para usuarias normotensas y 25,7 para usuarias con hipertensión severa ( 30). El riesgo atribuible también es mayor en mujeres mayores (3).
Riesgo relacionado con la dosis de enfermedad vascular de los anticonceptivos orales
Se ha observado una asociación positiva entre la cantidad de estrógeno y progestágeno en los anticonceptivos orales y el riesgo de enfermedad vascular (31–33). Se ha informado una disminución de las lipoproteínas de alta densidad (HDL) séricas con muchos agentes progestágenos (14–16). Una disminución de las lipoproteínas de alta densidad séricas se ha asociado con una mayor incidencia de cardiopatía isquémica. Debido a que los estrógenos aumentan el colesterol HDL, el efecto neto de un anticonceptivo oral depende del equilibrio logrado entre las dosis de estrógeno y progestágeno y la naturaleza y cantidad absoluta de progestágenos utilizados en los anticonceptivos. La cantidad de ambas hormonas debe ser considerada en la elección de un anticonceptivo oral.
Minimizar la exposición a los estrógenos y progestágenos está en consonancia con los buenos principios terapéuticos. Para cualquier combinación particular de estrógeno/progestágeno, el régimen de dosificación prescrito debe ser uno que contenga la menor cantidad de estrógeno y progestágeno que sea compatible con una baja tasa de fracaso y las necesidades del paciente individual. Las nuevas aceptantes de agentes anticonceptivos orales deben comenzar con preparaciones que contengan 0,035 mg o menos de estrógeno.
Persistencia del riesgo de enfermedad vascular
Hay dos estudios que han demostrado la persistencia del riesgo de enfermedad vascular para las usuarias de anticonceptivos orales. En un estudio en los Estados Unidos, el riesgo de desarrollar infarto de miocardio después de suspender los anticonceptivos orales persiste durante al menos 9 años para mujeres de 40 a 49 años que habían usado anticonceptivos orales durante cinco años o más, pero este aumento del riesgo no se demostró en otros grupos de edad (8). En otro estudio realizado en Gran Bretaña, el riesgo de desarrollar enfermedad cerebrovascular persistió durante al menos 6 años después de suspender los anticonceptivos orales, aunque el exceso de riesgo fue muy pequeño (34). Sin embargo, ambos estudios se realizaron con formulaciones anticonceptivas orales que contenían 50 microgramos o más de estrógeno.
Estimaciones de mortalidad por uso de anticonceptivos
Un estudio reunió datos de una variedad de fuentes que han estimado la tasa de mortalidad asociada con diferentes métodos anticonceptivos a diferentes edades (Tabla IV). Estas estimaciones incluyen el riesgo combinado de muerte asociado con los métodos anticonceptivos más el riesgo atribuible al embarazo en caso de falla del método. Cada método anticonceptivo tiene sus beneficios y riesgos específicos. El estudio concluyó que, con la excepción de las usuarias de anticonceptivos orales de 35 años o más que fuman y de 40 años o más que no fuman, la mortalidad asociada con todos los métodos anticonceptivos es baja e inferior a la asociada con el parto.
La observación de un posible aumento del riesgo de mortalidad con la edad para las usuarias de anticonceptivos orales se basa en datos recopilados en la década de 1970, pero no informados hasta 1983 (35). Sin embargo, la práctica clínica actual implica el uso de formulaciones bajas en estrógeno combinadas con una cuidadosa consideración de los factores de riesgo.
Debido a estos cambios en la práctica y, también, debido a algunos datos nuevos limitados que sugieren que el riesgo de enfermedad cardiovascular con el uso de anticonceptivos orales ahora puede ser menor que el observado anteriormente (100,101), el Comité Asesor de Medicamentos para la Fertilidad y la Salud Materna se mostró pidió revisar el tema en 1989. El Comité concluyó que, aunque los riesgos de enfermedades cardiovasculares pueden aumentar con el uso de anticonceptivos orales después de los 40 años en mujeres sanas que no fuman (incluso con las formulaciones más nuevas de dosis bajas), también existen mayores riesgos potenciales para la salud asociados con el embarazo en mujeres mayores y con los procedimientos quirúrgicos y médicos alternativos que pueden ser necesarios si dichas mujeres no tienen acceso a medios anticonceptivos eficaces y aceptables.
Por lo tanto, el Comité recomendó que los beneficios del uso de anticonceptivos orales en dosis bajas por parte de mujeres sanas mayores de 40 años que no fuman pueden superar los posibles riesgos. Por supuesto, las mujeres mayores, como todas las mujeres que toman anticonceptivos orales, deben tomar la formulación de dosis más baja posible que sea efectiva.
TABLA IV: NÚMERO ANUAL DE MUERTES RELACIONADAS CON EL NACIMIENTO O EL MÉTODO ASOCIADAS AL CONTROL DE LA FERTILIDAD POR CADA 100.000 MUJERES NO ESTÉRILES, POR EL MÉTODO DE CONTROL DE LA FERTILIDAD SEGÚN LA EDAD
Carcinoma de los órganos reproductores y de las mamas
Se han realizado numerosos estudios epidemiológicos sobre la incidencia de cáncer de mama, de endometrio, de ovario y de cuello uterino en mujeres que utilizan anticonceptivos orales. Si bien existen informes contradictorios, la mayoría de los estudios sugieren que el uso de anticonceptivos orales no está asociado con un aumento general del riesgo de desarrollar cáncer de mama. Algunos estudios han informado un mayor riesgo relativo de desarrollar cáncer de mama, particularmente a una edad más temprana. Este aumento del riesgo relativo parece estar relacionado con la duración del uso (36–43, 79–89).
Algunos estudios sugieren que el uso de anticonceptivos orales se ha asociado con un aumento del riesgo de neoplasia intraepitelial cervical en algunas poblaciones de mujeres (45–48). Sin embargo, continúa existiendo controversia sobre hasta qué punto estos hallazgos pueden deberse a diferencias en el comportamiento sexual y otros factores.
neoplasia hepática
Los adenomas hepáticos benignos se asocian con el uso de anticonceptivos orales, aunque la incidencia de tumores benignos es rara en los Estados Unidos. Cálculos indirectos han estimado que el riesgo atribuible está en el rango de 3,3 casos/100.000 para usuarias, riesgo que aumenta después de cuatro o más años de uso, especialmente con anticonceptivos orales de dosis más altas (49). La rotura de adenomas hepáticos benignos poco frecuentes puede causar la muerte por hemorragia intraabdominal (50,51).
Los estudios realizados en Gran Bretaña han demostrado un mayor riesgo de desarrollar carcinoma hepatocelular (52–54) en usuarias de anticonceptivos orales a largo plazo (>8 años). Sin embargo, estos cánceres son extremadamente raros en los EE. UU. y el riesgo atribuible (el exceso de incidencia) de cánceres de hígado en usuarias de anticonceptivos orales se acerca a menos de uno por millón de usuarias.
lesiones oculares
Ha habido informes de casos clínicos de trombosis retiniana asociados con el uso de anticonceptivos orales. Los anticonceptivos orales deben suspenderse si hay una pérdida de visión parcial o completa inexplicable; aparición de proptosis o diplopía; papiledema; o lesiones vasculares retinales. Se deben tomar inmediatamente las medidas diagnósticas y terapéuticas apropiadas.
Uso de anticonceptivos orales antes o durante el embarazo temprano
Amplios estudios epidemiológicos no han revelado un mayor riesgo de defectos congénitos en mujeres que han usado anticonceptivos orales antes del embarazo (55–57). Los estudios tampoco sugieren un efecto teratogénico, particularmente en lo que se refiere a anomalías cardíacas y defectos de reducción de extremidades (55,56,58,59), cuando los anticonceptivos orales se toman sin darse cuenta durante el embarazo temprano.
La administración de anticonceptivos orales para inducir el sangrado por deprivación no debe utilizarse como prueba de embarazo. Los anticonceptivos orales no deben usarse durante el embarazo para tratar la amenaza o el aborto habitual. Se recomienda que para cualquier paciente que haya perdido dos períodos consecutivos, se descarte el embarazo antes de continuar con el uso de anticonceptivos orales. Si la paciente no se ha adherido al programa prescrito, se debe considerar la posibilidad de embarazo en el primer período perdido. Se debe suspender el uso de anticonceptivos orales hasta que se descarte el embarazo.
Enfermedad de la vesícula
Estudios anteriores informaron un mayor riesgo relativo de por vida de cirugía de vesícula biliar en usuarias de anticonceptivos orales y estrógenos (60,61). Sin embargo, estudios más recientes han demostrado que el riesgo relativo de desarrollar enfermedad de la vesícula biliar entre las usuarias de anticonceptivos orales puede ser mínimo (62–64). Los hallazgos recientes de riesgo mínimo pueden estar relacionados con el uso de formulaciones anticonceptivas orales que contienen dosis hormonales más bajas de estrógenos y progestágenos.
Efectos metabólicos de carbohidratos y lípidos
Se ha demostrado que los anticonceptivos orales provocan una disminución de la tolerancia a la glucosa en un porcentaje importante de usuarias (17). Los anticonceptivos orales que contienen más de 75 microgramos de estrógenos causan hiperinsulinismo, mientras que las dosis más bajas de estrógeno causan menos intolerancia a la glucosa (65). Los progestágenos aumentan la secreción de insulina y crean resistencia a la insulina, este efecto varía con diferentes agentes progestágenos (17,66). Sin embargo, en la mujer no diabética, los anticonceptivos orales parecen no tener efecto sobre la glucemia en ayunas (67). Debido a estos efectos demostrados, las mujeres prediabéticas y diabéticas deben ser monitoreadas cuidadosamente mientras toman anticonceptivos orales.
Una pequeña proporción de mujeres tendrá hipertrigliceridemia persistente mientras toman la píldora. Como se discutió anteriormente (ver ADVERTENCIAS ), se han informado cambios en los niveles séricos de triglicéridos y lipoproteínas en usuarias de anticonceptivos orales.
Presión sanguínea elevada
Se ha informado un aumento de la presión arterial en mujeres que toman anticonceptivos orales (68) y este aumento es más probable en usuarias mayores de anticonceptivos orales (69) y con el uso continuado (61). Los datos del Royal College of General Practitioners (12) y los ensayos aleatorios posteriores han demostrado que la incidencia de hipertensión aumenta con cantidades crecientes de progestágenos.
Se debe alentar a las mujeres con antecedentes de hipertensión o enfermedades relacionadas con la hipertensión, o enfermedad renal (70) a usar otro método anticonceptivo. Si las mujeres eligen usar anticonceptivos orales, deben ser monitoreadas de cerca y si ocurre una elevación significativa de la presión arterial, se deben suspender los anticonceptivos orales. Para la mayoría de las mujeres, la presión arterial elevada volverá a la normalidad después de suspender los anticonceptivos orales (69), y no hay diferencia en la aparición de hipertensión entre los que alguna vez los usaron y los que nunca los usaron (68,70,71).
Dolor de cabeza
La aparición o exacerbación de la migraña o el desarrollo de dolor de cabeza con un nuevo patrón que es recurrente, persistente o grave requiere la interrupción de los anticonceptivos orales y la evaluación de la causa.
irregularidades en el sangrado
A veces se encuentran sangrado intermenstrual y manchado en pacientes que toman anticonceptivos orales, especialmente durante los primeros tres meses de uso. Se deben considerar las causas no hormonales y tomar las medidas diagnósticas adecuadas para descartar malignidad o embarazo en caso de sangrado intermenstrual, como en el caso de cualquier sangrado vaginal anormal. Si se ha excluido la patología, el tiempo o un cambio a otra formulación pueden resolver el problema. En caso de amenorrea, se debe descartar el embarazo.
Algunas mujeres pueden experimentar amenorrea u oligomenorrea después de tomar la píldora, especialmente cuando tal condición ya existía.
Embarazo ectópico
El embarazo ectópico así como el intrauterino pueden ocurrir en fallas anticonceptivas.
PRECAUCIONES
General
Se debe advertir a los pacientes que este producto no protege contra la infección por VIH (SIDA) y otras enfermedades de transmisión sexual.
Exploración física y seguimiento
Es una buena práctica médica que todas las mujeres se realicen una historia clínica y exámenes físicos anuales, incluidas las mujeres que usan anticonceptivos orales. Sin embargo, el examen físico puede posponerse hasta después del inicio de los anticonceptivos orales si la mujer lo solicita y el médico lo considera apropiado. El examen físico debe incluir especial referencia a la presión arterial, mamas, abdomen y órganos pélvicos, incluida la citología cervical y las pruebas de laboratorio pertinentes. En caso de sangrado vaginal anormal persistente o recurrente no diagnosticado, se deben tomar las medidas apropiadas para descartar malignidad. Las mujeres con un fuerte historial familiar de cáncer de mama o que tienen nódulos mamarios deben ser monitoreadas con especial cuidado.
Trastornos de lípidos
Las mujeres que están siendo tratadas por hiperlipidemias deben ser seguidas de cerca si eligen usar anticonceptivos orales. Algunos progestágenos pueden elevar los niveles de LDL y dificultar el control de las hiperlipidemias.
Función del hígado
Si se desarrolla ictericia en una mujer que recibe tales medicamentos, se debe suspender el medicamento. Las hormonas esteroides pueden metabolizarse deficientemente en pacientes con insuficiencia hepática.
Retención de líquidos
Los anticonceptivos orales pueden causar cierto grado de retención de líquidos. Deben ser prescritos con precaución, y solo con un control cuidadoso, en pacientes con condiciones que puedan agravarse por la retención de líquidos.
Trastornos emocionales
Las mujeres con antecedentes de depresión deben ser cuidadosamente observadas y el medicamento debe suspenderse si la depresión reaparece en un grado grave.
Lentes de contacto
Los usuarios de lentes de contacto que desarrollen cambios visuales o cambios en la tolerancia a los lentes deben ser evaluados por un oftalmólogo.
Carcinogénesis
Ver ADVERTENCIAS sección.
El embarazo
Embarazo Categoría X (ver CONTRAINDICACIONES y ADVERTENCIAS secciones).
Madres lactantes
Se han identificado pequeñas cantidades de esteroides anticonceptivos orales en la leche de madres lactantes y se han informado algunos efectos adversos en el niño, que incluyen ictericia y agrandamiento de los senos. Además, los anticonceptivos orales administrados en el posparto pueden interferir con la lactancia al disminuir la cantidad y calidad de la leche materna. Si es posible, se debe aconsejar a la madre que amamanta que no use anticonceptivos orales sino que use otras formas de anticoncepción hasta que haya destetado completamente a su hijo.
uso pediátrico
Se ha establecido la seguridad y la eficacia de las tabletas de Mircette® (desogestrel/etinilestradiol y etinilestradiol) en mujeres en edad reproductiva. Se espera que la seguridad y la eficacia sean las mismas para adolescentes pospuberales menores de 16 años y para usuarios de 16 años o más. El uso de este producto antes de la menarquia no está indicado.
Información para el paciente
Ver Etiquetado de pacientes
REFERENCIAS @sesenta y cinco. Hatcher RA, Trussell J, Stewart F et al. Tecnología anticonceptiva: decimoséptima edición revisada, Nueva York: Irvington Publishers, 1998, en prensa. @sesenta y cinco. Stadel BV. Anticonceptivos orales y enfermedades cardiovasculares. (Pt. 1). N Engl J Med 1981; 305:612–618. @sesenta y cinco. Stadel BV. Anticonceptivos orales y enfermedades cardiovasculares. (Pt. 2). N Engl J Med 1981; 305:672–677. @sesenta y cinco. Adam SA, Thorogood M. La anticoncepción oral y el infarto de miocardio revisados: los efectos de las nuevas preparaciones y los patrones de prescripción. Br J Obstet y Gynecol 1981; 88:838–845. @sesenta y cinco. Mann JI, Inman WH. Anticonceptivos orales y muerte por infarto de miocardio. Br Med J 1975; 2(5965):245–248. @sesenta y cinco. Mann JI, Vessey MP, Thorogood M, Doll R. Infarto de miocardio en mujeres jóvenes con especial referencia a la práctica de anticonceptivos orales. Br Med J 1975; 2(5956):241–245. @sesenta y cinco. Estudio de anticoncepción oral del Royal College of General Practitioners: Análisis adicionales de la mortalidad en usuarias de anticonceptivos orales. Lancet 1981; 1: 541–546. @sesenta y cinco. Slone D, Shapiro S, Kaufman DW, Rosenberg L, Miettinen OS, Stolley PD. Riesgo de infarto de miocardio en relación con el uso actual y discontinuado de anticonceptivos orales. N Engl J Med 1981; 305:420–424. @sesenta y cinco. Vessey MP. Hormonas femeninas y enfermedad vascular: una descripción epidemiológica. Br J Fam Plann 1980; 6:1–12. @sesenta y cinco. Russell-Briefel RG, Ezzati TM, Fulwood R, Perlman JA, Murphy RS. Estado de riesgo cardiovascular y uso de anticonceptivos orales, Estados Unidos, 1976–80. Prevenir Med 1986; 15:352–362. @sesenta y cinco. Goldbaum GM, Kendrick JS, Hogelin GC, Gentry EM. El impacto relativo del tabaquismo y el uso de anticonceptivos orales en las mujeres en los Estados Unidos. JAMA 1987; 258:1339–1342. @sesenta y cinco. Layde PM, Beral V. Análisis adicionales de la mortalidad en usuarias de anticonceptivos orales: estudio de anticoncepción oral de médicos generales del Royal College. (Cuadro 5) Lancet 1981; 1: 541–546. @sesenta y cinco. Knopp RH. Riesgo de arteriosclerosis: las funciones de los anticonceptivos orales y los estrógenos posmenopáusicos. J Reprod Med 1986; 31(9) (Suplemento): 913–921. @sesenta y cinco. Krauss RM, Roy S, Mishell DR, Casagrande J, Pike MC. Efectos de dos anticonceptivos orales en dosis bajas sobre los lípidos y las lipoproteínas séricas: Cambios diferenciales en las subclases de lipoproteínas de alta densidad. Am J Obstet 1983; 145:446–452. @sesenta y cinco. Wahl P, Walden C, Knopp R, Hoover J, Wallace R, Heiss G, Rifkind B. Efecto de la potencia de estrógeno/progestina sobre el colesterol de lípidos/lipoproteínas. N Engl J Med 1983; 308:862–867. @sesenta y cinco. Wynn V, Niththyananthan R. El efecto de la progestina en los anticonceptivos orales combinados sobre los lípidos séricos con especial referencia a las lipoproteínas de alta densidad. Am J Obstet Gynecol 1982; 142:766–771. @sesenta y cinco. Wynn V, Godsland I. Efectos de los anticonceptivos orales y el metabolismo de los carbohidratos. J Reprod Med 1986; 31 (9) (Suplemento): 892–897. @sesenta y cinco. La Rosa JC. Factores de riesgo ateroscleróticos en la enfermedad cardiovascular. J Reprod Med 1986; 31 (9) (Suplemento): 906–912. @sesenta y cinco. Inman WH, Vessey MP. Investigación de la muerte por trombosis y embolia pulmonar, coronaria y cerebral en mujeres en edad fértil. Br Med J 1968; 2 (5599): 193–199. @sesenta y cinco. Maguire MG, Tonascia J, Sartwell PE, Stolley PD, Tockman MS. Mayor riesgo de trombosis debido a los anticonceptivos orales: un informe adicional. Am J Epidemiol 1979; 110 (2):188–195. @sesenta y cinco. Pettiti DB, Wingerd J, Pellegrin F, Ramacharan S. Riesgo de enfermedad vascular en mujeres: tabaquismo, anticonceptivos orales, estrógenos no anticonceptivos y otros factores. JAMA 1979; 242:1150–1154. @sesenta y cinco. Vessey MP, Doll R. Investigación de la relación entre el uso de anticonceptivos orales y la enfermedad tromboembólica. Br Med J 1968; 2 (5599): 199–205. @sesenta y cinco. Vessey MP, Doll R. Investigación de la relación entre el uso de anticonceptivos orales y la enfermedad tromboembólica. Un informe más. Br Med J 1969; 2 (5658):651–657. @sesenta y cinco. Porter JB, Hunter JR, Danielson DA, Jick H, Stergachis A. Anticonceptivos orales y enfermedad vascular no fatal: experiencia reciente. Obstet Gynecol 1982; 59 (3):299–302. @sesenta y cinco. Vessey M, Doll R, Peto R, Johnson B, Wiggins P. Un estudio de seguimiento a largo plazo de mujeres que usan diferentes métodos anticonceptivos: un informe provisional. Ciencias Biosociales 1976; 8:375–427. @sesenta y cinco. Royal College of General Practitioners: Anticonceptivos orales, trombosis venosa y venas varicosas. J Royal Coll Gen Pract 1978; 28:393–399. @sesenta y cinco. Grupo Colaborativo para el Estudio del Accidente Cerebrovascular en Mujeres Jóvenes: Anticoncepción oral y mayor riesgo de isquemia cerebral o trombosis. N Engl J Med 1973; 288:871–878. @sesenta y cinco. Petitti DB, Wingerd J. Uso de anticonceptivos orales, tabaquismo y riesgo de hemorragia subaracnoidea. Lancet 1978; 2:234–236. @sesenta y cinco. Inman WH. Anticonceptivos orales y hemorragia subaracnoidea fatal. Br Med J 1979; 2 (6203): 1468–70. @sesenta y cinco. Grupo Colaborativo para el Estudio del Accidente Cerebrovascular en Mujeres Jóvenes: Anticonceptivos orales y accidente cerebrovascular en mujeres jóvenes: factores de riesgo asociados. JAMA 1975; 231:718–722. @sesenta y cinco. Inman WH, Vessey MP, Westerholm B, Engelund A. Enfermedad tromboembólica y el contenido de esteroides de los anticonceptivos orales. Un informe para el Comité de Seguridad de Medicamentos. Br Med J 1970; 2:203–209. @sesenta y cinco. Meade TW, Greenberg G, Thompson SG. Progestágenos y reacciones cardiovasculares asociadas con los anticonceptivos orales y una comparación de la seguridad de las preparaciones de estrógeno de 50 y 35 mcg. Br Med J 1980; 280 (6224): 1157–1161. @sesenta y cinco. Kay CR. Progestágenos y enfermedad arterial: evidencia del estudio del Royal College of General Practitioners. Am J Obstet Gynecol 1982; 142:762–765. @sesenta y cinco. Royal College of General Practitioners: Incidencia de enfermedad arterial entre usuarias de anticonceptivos orales. J Royal Coll Gen Pract 1983; 33:75–82. @sesenta y cinco. Ory HW. Mortalidad asociada con la fecundidad y el control de la fecundidad: 1983. Family Planning Perspectives 1983; 15:50–56. @sesenta y cinco. El estudio sobre el cáncer y las hormonas esteroides de los Centros para el Control de Enfermedades y el Instituto Nacional de Salud Infantil y Desarrollo Humano: uso de anticonceptivos orales y riesgo de cáncer de mama. N Engl J Med 1986; 315:405–411. @sesenta y cinco. Pike MC, Henderson BE, Krailo MD, Duke A, Roy S. Riesgo de cáncer de mama en mujeres jóvenes y uso de anticonceptivos orales: posible efecto modificador de la formulación y edad de uso. Lancet 1983; 2:926–929. @sesenta y cinco. Paul C, Skegg DG, Spears GFS, Kaldor JM. Anticonceptivos orales y cáncer de mama: un estudio nacional. Br Med J 1986; 293:723–725. @sesenta y cinco. Miller DR, Rosenberg L, Kaufman DW, Schottenfeld D, Stolley PD, Shapiro S. Riesgo de cáncer de mama en relación con el uso temprano de anticonceptivos orales. Obstet Gynecol 1986; 68:863–868. @sesenta y cinco. Olson H, Olson KL, Moller TR, Ranstam J, Holm P. Uso de anticonceptivos orales y cáncer de mama en mujeres jóvenes en Suecia (carta). Lancet 1985; 2:748–749. @sesenta y cinco. McPherson K, Vessey M, Neil A, Doll R, Jones L, Roberts M. Uso temprano de anticonceptivos y cáncer de mama: resultados de otro estudio de casos y controles. Br J Cancer 1987; 56: 653–660 @sesenta y cinco. Huggins GR, Zucker PF. Anticonceptivos orales y neoplasia: actualización de 1987. Fértil Steril 1987; 47:733–761. @sesenta y cinco. McPherson K, Drife JO. La píldora y el cáncer de mama: ¿por qué la incertidumbre? Br Med J 1986; 293:709–710. @sesenta y cinco. Ory H, Naib Z, Conger SB, Hatcher RA, Tyler CW. Elección anticonceptiva y prevalencia de displasia cervical y carcinoma in situ. Am J Obstet Gynecol 1976; 124:573–577. @sesenta y cinco. Vessey MP, Lawless M, McPherson K, Yeates D. Neoplasia del cuello uterino y anticoncepción: un posible efecto adverso de la píldora. Lancet 1983; 2:930. @sesenta y cinco. Brinton LA, Huggins GR, Lehman HF, Malli K, Savitz DA, Trapido E, Rosenthal J, Hoover R. Uso a largo plazo de anticonceptivos orales y riesgo de cáncer de cuello uterino invasivo. Int J Cancer 1986; 38:339–344. @sesenta y cinco. Estudio colaborativo de la OMS sobre neoplasias y anticonceptivos esteroides: cáncer de cuello uterino invasivo y anticonceptivos orales combinados. Br Med J 1985; 209:961–965. @sesenta y cinco. Rooks JB, Ory HW, Ishak KG, Strauss LT, Greenspan JR, Hill AP, Tyler CW. Epidemiología del adenoma hepatocelular: el papel del uso de anticonceptivos orales. JAMA 1979; 242:644–648. @sesenta y cinco. Bein NN, Goldsmith SA. Hemorragia masiva recurrente por tumores hepáticos benignos secundaria a anticonceptivos orales. Br J Surg 1977; 64:433–435. @sesenta y cinco. Klatskin G. Tumores hepáticos: posible relación con el uso de anticonceptivos orales. Gastroenterología 1977; 73:386–394. @sesenta y cinco. Henderson BE, Preston-Martin S, Edmondson HA, Peters RL, Pike MC. Carcinoma hepatocelular y anticonceptivos orales. Br J Cancer 1983; 48:437–440. @sesenta y cinco. Neuberger J, Forman D, Doll R, Williams R. Anticonceptivos orales y carcinoma hepatocelular. Br Med J 1986; 292:1355–1357. @sesenta y cinco. Forman D, Vincent TJ, Doll R. Cáncer del hígado y anticonceptivos orales. Br Med J 1986; 292:1357–1361. @sesenta y cinco. Harlap S, Eldor J. Nacimientos después de fallas en los anticonceptivos orales. Obstet Gynecol 1980; 55:447–452. @sesenta y cinco. Savolainen E, Saksela E, Saxen L. Peligros teratógenos de los anticonceptivos orales analizados en un registro nacional de malformaciones. Am J Obstet Gynecol 1981; 140:521–524. @sesenta y cinco. Janerich DT, Piper JM, Glebatis DM. Anticonceptivos orales y defectos de nacimiento. Am J Epidemiol 1980; 112:73–79. @sesenta y cinco. Ferencz C, Matanoski GM, Wilson PD, Rubin JD, Neill CA, Gutberlet R. Terapia hormonal materna y cardiopatía congénita. Teratología 1980; 21:225–239. @sesenta y cinco. Rothman KJ, Fyler DC, Goldbatt A, Kreidberg MB. Hormonas exógenas y otras exposiciones a fármacos de niños con cardiopatías congénitas. Am J Epidemiol 1979; 109:433–439. @sesenta y cinco. Programa Colaborativo de Vigilancia de Drogas de Boston: Anticonceptivos orales y enfermedad tromboembólica venosa, enfermedad de la vesícula biliar confirmada quirúrgicamente y tumores de mama. Lancet 1973; 1:1399–1404. @sesenta y cinco. Real Colegio de Médicos Generales: Anticonceptivos orales y salud. Nueva York, Pittman, 1974. @sesenta y cinco. Layde PM, Vessey MP, Yeates D. Riesgo de enfermedad de la vesícula biliar: un estudio de cohorte de mujeres jóvenes que asisten a clínicas de planificación familiar. J Epidemiol Salud Comunitaria 1982; 36:274–278. @sesenta y cinco. Grupo de Roma para la Epidemiología y Prevención de la Colelitiasis (GREPCO): Prevalencia de la enfermedad de cálculos biliares en una población femenina adulta italiana. Am J Epidemiol 1984; 119:796–805. @sesenta y cinco. Strom BL, Tamragouri RT, Morse ML, Lazar EL, West SL, Stolley PD, Jones JK. Anticonceptivos orales y otros factores de riesgo para la enfermedad de la vesícula biliar. Clin Pharmacol Ther 1986; 39:335–341. @sesenta y cinco. Wynn V, Adams PW, Godsland IF, Melrose J, Niththyananthan R, Oakley NW, Seedj A. Comparación de los efectos de diferentes formulaciones de anticonceptivos orales combinados sobre el metabolismo de carbohidratos y lípidos. Lancet 1979; 1:1045–1049. @sesenta y cinco. Wynn V. Efecto de la progesterona y las progestinas sobre el metabolismo de los carbohidratos. En Progesterona y Progestina. Editado por Bardin CW, Milgrom E, Mauvis-Jarvis P. Nueva York, Raven Press, 1983 págs. 395–410. @sesenta y cinco. Perlman JA, Roussell-Briefel RG, Ezzati TM, Lieberknecht G. Tolerancia a la glucosa oral y la potencia de los progestágenos anticonceptivos orales. J Chronic Dis 1985; 38:857–864. @sesenta y cinco. Estudio de anticoncepción oral del Royal College of General Practitioners: efecto sobre la hipertensión y la enfermedad mamaria benigna del componente de progestágeno en anticonceptivos orales combinados. Lancet 1977; @sesenta y cinco. Fisch IR, Frank J. Anticonceptivos orales y presión arterial. JAMA 1977; 237:2499–2503. @sesenta y cinco. Laragh AJ. Hipertensión inducida por anticonceptivos orales: nueve años después. Am J Obstet Gynecol 1976; 126:141–147. @sesenta y cinco. Ramcharan S, Peritz E, Pellegrin FA, Williams WT. Incidencia de hipertensión en la cohorte del estudio de fármacos anticonceptivos de Walnut Creek. En Farmacología de los Medicamentos Anticonceptivos Esteroideos. Garattini S, Berendes HW. Eds. Nueva York, Raven Press, 1977 págs. 277–288. (Monografías del Instituto Mario Negri de Investigaciones Farmacológicas, Milán). @sesenta y cinco. El estudio sobre el cáncer y las hormonas esteroides de los Centros para el Control de Enfermedades y el Instituto Nacional de Salud Infantil y Desarrollo Humano: uso de anticonceptivos orales y riesgo de cáncer de ovario. JAMA 1983; 249:1596–1599. @sesenta y cinco. Schlesselman J, Stadel BV, Murray P, Lai S. Breast Cancer en relación con el uso temprano de anticonceptivos orales 1988; 259:1828–1833. @sesenta y cinco. Hennekens CH, Speizer FE, Lipnick RJ, Rosner B, Bain C, Belanger C, Stampfer MJ, Willett W, Peto R. Un estudio de casos y controles sobre el uso de anticonceptivos orales y el cáncer de mama. JNCI 1984; 72:39–42. @sesenta y cinco. LaVecchia C, Decarli A, Fasoli M, Franceschi S, Gentile A, Negri E, Parazzini F, Tognoni G. Anticonceptivos orales y cánceres de mama y del tracto genital femenino. Resultados provisionales de un estudio de casos y controles. Hermano J. Cáncer 1986; 54:311–317. @sesenta y cinco. Meirik O, Lund E, Adami H, Bergstrom R, Christoffersen T, Bergsjo P. Uso de anticonceptivos orales en el cáncer de mama en mujeres jóvenes. Un estudio nacional conjunto de casos y controles en Suecia y Noruega. Lancet 1986; 11:650–654. @sesenta y cinco. Kay CR, Hannaford PC. El cáncer de mama y la píldora: otro informe del estudio sobre anticoncepción oral del Royal College of General Practitioners. Hermano J. Cáncer 1988; 58:675–680. @sesenta y cinco. Stadel BV, Lai S, Schlesselman JJ, Murray P. Anticonceptivos orales y cáncer de mama premenopáusico en mujeres nulíparas. Anticoncepción 1988; 38:287–299. @sesenta y cinco. Miller DR, Rosenberg L, Kaufman DW, Stolley P, Warshauer ME, Shapiro S. Cáncer de mama antes de los 45 años y uso de anticonceptivos orales: Nuevos hallazgos. Soy. J. Epidemiol 1989; 129:269–280. @sesenta y cinco. Grupo Nacional de Estudio de Casos y Controles del Reino Unido, Uso de anticonceptivos orales y riesgo de cáncer de mama en mujeres jóvenes. Lancet 1989; 1:973–982. @sesenta y cinco. Schlesselman JJ. Cáncer de mama y aparato reproductor en relación con el uso de anticonceptivos orales. Anticoncepción 1989; 40:1–38. @sesenta y cinco. Vessey MP, McPherson K, Villard-Mackintosh L, Yeates D. Anticonceptivos orales y cáncer de mama: últimos hallazgos en un gran estudio de cohortes. Hermano J. Cáncer 1989; 59:613–617. @sesenta y cinco. Jick SS, Walker AM, Stergachis A, Jick H. Anticonceptivos orales y cáncer de mama. Hermano J. Cáncer 1989; 59:618–621. @sesenta y cinco. Porter JB, Hunter J, Jick H et al. Anticonceptivos orales y enfermedad vascular no fatal. Obstet Gynecol 1985; 66:1–4. @sesenta y cinco. Porter JB, Jick H, Walker AM. Mortalidad entre usuarias de anticonceptivos orales. Obstet Gynecol 1987; 7029–32. @sesenta y cinco. Jick H, Jick SS, Gurewich V, Myers MW, Vasilakis C. Riesgo de muerte cardiovascular idiopática y tromboembolismo venoso no fatal en mujeres que usan anticonceptivos orales con diferentes componentes de progestágeno. Lanceta, 1995; 346:1589–93. @sesenta y cinco. Estudio colaborativo de la Organización Mundial de la Salud sobre enfermedades cardiovasculares y anticoncepción con hormonas esteroides. Efecto de diferentes progestágenos en anticonceptivos orales bajos en estrógenos sobre la enfermedad tromboembólica venosa. Lanceta, 1995; 346:1582–88. @sesenta y cinco. Spitzer WO, Lewis MA, Heinemann LAJ, Thorogood M, MacRae KD en nombre del Grupo de Investigación Transnacional sobre Anticonceptivos Orales y Salud de Mujeres Jóvenes. Anticonceptivos orales de tercera generación y riesgo de trastornos tromboembólicos venosos: un estudio internacional de casos y controles. Br Med J, 1996; 312:83–88. @sesenta y cinco. Christensen J, Petrenaite V, Atterman J, et al. Los anticonceptivos orales inducen el metabolismo de lamotrigina: evidencia de un ensayo doble ciego controlado con placebo. Epilepsia 2007;48(3):484-489.SOBREDOSIS
No se han informado efectos nocivos graves después de la ingestión aguda de grandes dosis de anticonceptivos orales por parte de niños pequeños. La sobredosis puede causar náuseas y puede ocurrir sangrado por deprivación en las mujeres.
Beneficios de salud no anticonceptivos
Los siguientes beneficios para la salud no anticonceptivos relacionados con el uso de anticonceptivos orales están respaldados por estudios epidemiológicos que utilizaron en gran medida formulaciones de anticonceptivos orales que contenían dosis de estrógeno superiores a 0,035 mg de etinilestradiol o 0,05 mg de mestranol (73–78).
Efectos sobre la menstruación
- aumento de la regularidad del ciclo menstrual
- disminución de la pérdida de sangre y disminución de la incidencia de anemia por deficiencia de hierro
- disminución de la incidencia de dismenorrea
Efectos relacionados con la inhibición de la ovulación
- disminución de la incidencia de quistes ováricos funcionales
- disminución de la incidencia de embarazos ectópicos
Efectos del uso a largo plazo
- disminución de la incidencia de fibroadenomas y enfermedad fibroquística de la mama
- disminución de la incidencia de enfermedad inflamatoria pélvica aguda
- disminución de la incidencia de cáncer de endometrio
- disminución de la incidencia de cáncer de ovario
CONTRAINDICACIONES
Los anticonceptivos orales no deben usarse en mujeres que actualmente tienen las siguientes condiciones:
- Tromboflebitis o trastornos tromboembólicos
- Antecedentes de tromboflebitis venosa profunda o trastornos tromboembólicos.
- Enfermedad vascular cerebral o de las arterias coronarias
- Carcinoma de mama conocido o sospechado
- Carcinoma de endometrio u otra neoplasia dependiente de estrógeno conocida o sospechada
- Sangrado genital anormal no diagnosticado
- Ictericia colestática del embarazo o ictericia con uso previo de píldoras
- Adenomas o carcinomas hepáticos
- Embarazo conocido o sospechado
FARMACOLOGÍA CLÍNICA
Los anticonceptivos orales combinados actúan mediante la supresión de las gonadotropinas. Aunque el mecanismo principal de esta acción es la inhibición de la ovulación, otras alteraciones incluyen cambios en el moco cervical (que aumentan la dificultad de entrada de los espermatozoides en el útero) y el endometrio (que reducen la probabilidad de implantación).
Los estudios de unión al receptor, así como los estudios en animales, han demostrado que el etonogestrel, el metabolito biológicamente activo del desogestrel, combina una alta actividad progestacional con una androgenicidad intrínseca mínima (91,92). Se desconoce la relevancia de este último hallazgo en humanos.
Farmacocinética
Absorción
El desogestrel se absorbe rápida y casi por completo y se convierte en etonogestrel, su metabolito biológicamente activo. Después de la administración oral, la biodisponibilidad relativa de desogestrel en comparación con una solución, medida por los niveles séricos de etonogestrel, es de aproximadamente 100%. Las tabletas Mircette® (desogestrel/etinilestradiol y etinilestradiol) proporcionan dos regímenes diferentes de etinilestradiol; 0,02 mg en el comprimido combinado [blanco] y 0,01 mg en el comprimido amarillo. El etinilestradiol se absorbe rápida y casi completamente. Después de una dosis única de la tableta combinada Mircette® [blanca], la biodisponibilidad relativa del etinilestradiol es de aproximadamente el 93 %, mientras que la biodisponibilidad relativa de la tableta de 0,01 mg [amarilla] es del 99 %. No se ha evaluado el efecto de los alimentos sobre la biodisponibilidad de los comprimidos de Mircette® después de la administración oral.
La farmacocinética de etonogestrel y etinilestradiol luego de la administración de dosis múltiples de tabletas de Mircette® se determinó durante el tercer ciclo en 17 sujetos. Las concentraciones plasmáticas de etonogestrel y etinilestradiol alcanzaron el estado estacionario el día 21. El AUC(0–24) del etonogestrel en el estado estacionario el día 21 fue aproximadamente 2,2 veces mayor que el AUC(0–24) del día 1 del tercer ciclo . Los parámetros farmacocinéticos de etonogestrel y etinilestradiol durante el tercer ciclo después de la administración de dosis múltiples de comprimidos de Mircette® se resumen en la Tabla I.
TABLA I: PARÁMETROS FARMACOCINÉTICOS MEDIOS (DE) DE Mircette® DURANTE UN PERÍODO DE DOSIFICACIÓN DE 28 DÍAS EN EL TERCER CICLO (n=17).
Distribución
Se encontró que el etonogestrel, el metabolito activo del desogestrel, se une a las proteínas en un 99 %, principalmente a la globulina fijadora de hormonas sexuales (SHBG). El etinilestradiol se une aproximadamente en un 98,3 %, principalmente a la albúmina plasmática. El etinilestradiol no se une a SHBG, pero induce la síntesis de SHBG. El desogestrel, en combinación con etinilestradiol, no contrarresta el aumento de SHBG inducido por los estrógenos, lo que resulta en niveles séricos más bajos de testosterona libre (96–99).
Metabolismo
Desogestrel:
El desogestrel se metaboliza rápida y completamente por hidroxilación en la mucosa intestinal y en el primer paso por el hígado a etonogestrel. También se han identificado otros metabolitos (es decir, 3α-OH-desogestrel, 3β-OHdesogestrel y 3α-OH-5α-H-desogestrel) sin acciones farmacológicas y estos metabolitos pueden sufrir conjugación de glucurónido y sulfato.
Etinilestradiol:
El etinilestradiol está sujeto a un grado significativo de conjugación presistémica (metabolismo de fase II). El etinilestradiol que escapa de la conjugación de la pared intestinal sufre un metabolismo de fase I y una conjugación hepática (metabolismo de fase II). Los principales metabolitos de la fase I son 2-OH-etinilestradiol y 2-metoxi-etinilestradiol. Los conjugados de sulfato y glucurónido tanto del etinilestradiol como de los metabolitos de fase I, que se excretan en la bilis, pueden pasar por la circulación enterohepática.
Excreción
El etonogestrel y el etinilestradiol se excretan en la orina, la bilis y las heces. En el estado estacionario, el día 21, la vida media de eliminación de etonogestrel es de 27,8±7,2 horas y la vida media de eliminación de etinilestradiol para el comprimido combinado es de 23,9±25,5 horas. Para el comprimido de etinilestradiol de 0,01 mg [amarillo], la semivida de eliminación en estado estacionario, día 28, es de 18,9 ± 8,3 horas.
Poblaciones Especiales
La raza
No hay información para determinar el efecto de la raza en la farmacocinética de las tabletas de Mircette® (desogestrel/etinilestradiol y etinilestradiol).
insuficiencia hepática
No se realizaron estudios formales para evaluar el efecto de la enfermedad hepática en la disposición de Mircette®.
Insuficiencia renal
No se realizaron estudios formales para evaluar el efecto de la enfermedad renal en la disposición de Mircette®.
Interacciones fármaco-fármaco
En la literatura se han informado interacciones entre desogestrel/etinilestradiol y otros fármacos. No se realizaron estudios formales de interacciones farmacológicas (ver PRECAUCIONES sección).
REFERENCIAS @sesenta y cinco. Godsland, I et al. Los efectos de diferentes formulaciones de agentes anticonceptivos orales sobre el metabolismo de lípidos y carbohidratos. N Engl J Med 1990; 323:1375–81. @sesenta y cinco. Kloosterboer, HJ et al. Selectividad en la unión de los receptores de progesterona y andrógenos de los progestágenos utilizados en la anticoncepción oral. Anticoncepción, 1988; 38:325–32. @sesenta y cinco. Van der Vies, J y de Visser, J. Estudios endocrinológicos con desogestrel. Arzneim. Forsch./Drug Res., 1983; 33(l),2:231–6. @sesenta y cinco. Cullberg, G et al. Efectos de una combinación de dosis bajas de desogestrel y etinilestradiol sobre el hirsutismo, los andrógenos y la globulina transportadora de hormonas sexuales en mujeres con síndrome de ovario poliquístico. Acta Obstet Gynecol Scand, 1985; 64:195–202. @sesenta y cinco. Jung-Hoffmann, C y Kuhl, H. Efectos divergentes de dos anticonceptivos orales de dosis baja sobre la globulina transportadora de hormonas sexuales y la testosterona libre. AJOG, 1987; 156:199–203. @sesenta y cinco. Hammond, G et al. Concentraciones séricas de proteína fijadora de esteroides, distribución de progestágenos y biodisponibilidad de testosterona durante el tratamiento con anticonceptivos que contienen desogestrel o levonorgestrel. fértil. Esteril., 1984; 42:44–51. @sesenta y cinco. Palatsi, R et al. Testosterona sérica total y libre y globulina fijadora de hormonas sexuales (SHBG) en pacientes con acné tratadas con dos anticonceptivos orales diferentes. Acta Derm Venereol, 1984; 64:517–23.INFORMACIÓN DEL PACIENTE
Mircette ® (desogestrel/etinilestradiol y etinilestradiol) Comprimidos
Este producto (como todos los anticonceptivos orales) está destinado a prevenir el embarazo. No protege contra la infección por VIH (SIDA) y otras enfermedades de transmisión sexual.
TENGA EN CUENTA: Esta etiqueta se revisa periódicamente a medida que se dispone de nueva información médica importante. Por lo tanto, revise cuidadosamente este etiquetado.
DESCRIPCIÓN
El siguiente producto anticonceptivo oral contiene una combinación de progestina y estrógeno, los dos tipos de hormonas femeninas:
Cada comprimido blanco contiene 0,15 mg de desogestrel y 0,02 mg de etinilestradiol. Cada comprimido verde claro contiene ingredientes inertes y cada comprimido amarillo contiene 0,01 mg de etinilestradiol.
INTRODUCCIÓN
Cualquier mujer que considere usar anticonceptivos orales (la píldora anticonceptiva o la píldora) debe comprender los beneficios y riesgos de usar esta forma de control de la natalidad. Este folleto le dará gran parte de la información que necesitará para tomar esta decisión y también le ayudará a determinar si corre el riesgo de desarrollar alguno de los efectos secundarios graves de la píldora. Le dirá cómo usar la píldora correctamente para que sea lo más eficaz posible. Sin embargo, este prospecto no reemplaza una discusión cuidadosa entre usted y su médico o proveedor de atención médica. Debe analizar la información proporcionada en este prospecto con él o ella, tanto cuando comience a tomar la píldora como durante sus visitas posteriores. También debe seguir los consejos de su médico o proveedor de atención médica con respecto a los controles regulares mientras toma la píldora.
EFICACIA DE LOS ANTICONCEPTIVOS ORALES
Los anticonceptivos orales o “píldoras anticonceptivas” o “la píldora” se utilizan para prevenir el embarazo y son más efectivos que otros métodos anticonceptivos no quirúrgicos. Cuando se toman correctamente, la probabilidad de quedar embarazada es inferior al 1% (1 embarazo por cada 100 mujeres por año de uso) cuando se usan perfectamente, sin omitir ninguna pastilla. Las tasas de falla típicas son en realidad del 5% por año. La posibilidad de quedar embarazada aumenta con cada píldora olvidada durante un ciclo menstrual.
En comparación, las tasas típicas de fracaso de otros métodos anticonceptivos durante el primer año de uso son las siguientes:
QUIÉN NO DEBE TOMAR ANTICONCEPTIVOS ORALES
Fumar cigarrillos aumenta el riesgo de efectos secundarios cardiovasculares graves por el uso de anticonceptivos orales. Este riesgo aumenta con la edad y con el tabaquismo intenso (15 o más cigarrillos al día) y es bastante marcado en mujeres mayores de 35 años. Se recomienda enfáticamente a las mujeres que usan anticonceptivos orales que no fumen.
Algunas mujeres no deberían usar la píldora. Por ejemplo, no debe tomar la píldora si está embarazada o cree que puede estarlo. Tampoco debe usar la píldora si tiene alguna de las siguientes condiciones:
- Antecedentes de ataque cardíaco o accidente cerebrovascular
- Coágulos de sangre en las piernas (tromboflebitis), los pulmones (embolia pulmonar) o los ojos
- Antecedentes de coágulos de sangre en las venas profundas de las piernas.
- Dolor torácico (angina de pecho)
- Cáncer de mama conocido o sospechado o cáncer del revestimiento del útero, el cuello uterino o la vagina
- Sangrado vaginal inexplicable (hasta que su médico llegue a un diagnóstico)
- Coloración amarillenta del blanco de los ojos o de la piel (ictericia) durante el embarazo o durante el uso previo de la píldora
- Tumor hepático (benigno o canceroso)
- Embarazo conocido o sospechado.
Informe a su médico o proveedor de atención médica si alguna vez ha tenido alguna de estas afecciones. Su médico o proveedor de atención médica puede recomendarle otro método anticonceptivo.
OTRAS CONSIDERACIONES ANTES DE TOMAR ANTICONCEPTIVOS ORALES
Informe a su médico o proveedor de atención médica si tiene:
- Nódulos mamarios, enfermedad fibroquística de la mama, una radiografía o mamografía de mama anormal
- Diabetes
- Colesterol o triglicéridos elevados
- Alta presión sanguínea
- Migraña u otros dolores de cabeza o epilepsia
- Depresión mental
- Enfermedad de la vesícula biliar, el corazón o los riñones
- Antecedentes de períodos menstruales escasos o irregulares.
Las mujeres con cualquiera de estas condiciones deben ser revisadas con frecuencia por su médico o proveedor de atención médica si deciden usar anticonceptivos orales.
Además, asegúrese de informar a su médico o proveedor de atención médica si fuma o toma algún medicamento.
RIESGOS DE TOMAR ANTICONCEPTIVOS ORALES
1. Riesgo de desarrollar coágulos de sangre
Los coágulos de sangre y la obstrucción de los vasos sanguíneos son uno de los efectos secundarios más graves de tomar anticonceptivos orales y pueden causar la muerte o una discapacidad grave. En particular, un coágulo en la pierna puede causar tromboflebitis y un coágulo que viaja a los pulmones puede causar un bloqueo repentino del vaso que lleva sangre a los pulmones. Los riesgos de estos efectos secundarios pueden ser mayores con los anticonceptivos orales que contienen desogestrel como Mircette® que con otras píldoras de dosis baja. En raras ocasiones, se forman coágulos en los vasos sanguíneos del ojo y pueden causar ceguera, visión doble o problemas de visión.
Si toma anticonceptivos orales y necesita una cirugía electiva, debe permanecer en cama por una enfermedad prolongada o ha dado a luz recientemente, puede correr el riesgo de desarrollar coágulos sanguíneos. Debe consultar a su médico o proveedor de atención médica acerca de suspender los anticonceptivos orales tres o cuatro semanas antes de la cirugía y no tomar anticonceptivos orales durante dos semanas después de la cirugía o durante el reposo en cama. Tampoco debe tomar anticonceptivos orales poco después del parto. Es recomendable esperar al menos cuatro semanas después del parto si no está amamantando o cuatro semanas después de un aborto en el segundo trimestre. Si está amamantando, debe esperar hasta que haya destetado a su hijo antes de usar la píldora (ver Lactancia materna en PRECAUCIONES GENERALES ).
El riesgo de enfermedad circulatoria en usuarias de anticonceptivos orales puede ser mayor en usuarias de píldoras de dosis alta y puede ser mayor con una duración más prolongada del uso de anticonceptivos orales. Además, algunos de estos mayores riesgos pueden continuar durante varios años después de suspender los anticonceptivos orales. El riesgo de enfermedad tromboembólica venosa asociada con los anticonceptivos orales no aumenta con la duración del uso y desaparece una vez que se suspende el uso de la píldora. El riesgo de coagulación sanguínea anormal aumenta con la edad tanto en las usuarias como en las no usuarias de anticonceptivos orales, pero el mayor riesgo de los anticonceptivos orales parece estar presente en todas las edades. Para las mujeres de 20 a 44 años, se estima que aproximadamente 1 de cada 2000 que usan anticonceptivos orales será hospitalizada cada año debido a una coagulación anormal. Entre los no usuarios del mismo grupo de edad, aproximadamente 1 de cada 20 000 sería hospitalizado cada año. Para las usuarias de anticonceptivos orales en general, se ha estimado que en mujeres entre 15 y 34 años el riesgo de muerte por un trastorno circulatorio es de aproximadamente 1 en 12.000 por año, mientras que para las no usuarias la tasa es de aproximadamente 1 en 50.000 por año. En el grupo de edad de 35 a 44 años, se estima que el riesgo es de 1 en 2500 por año para las usuarias de anticonceptivos orales y de 1 en 10 000 por año para las no usuarias.
2. Ataques cardíacos y accidentes cerebrovasculares
Los anticonceptivos orales pueden aumentar la tendencia a desarrollar accidentes cerebrovasculares (tapamiento o ruptura de los vasos sanguíneos en el cerebro) y angina de pecho y ataques cardíacos (obstrucción de los vasos sanguíneos en el corazón). Cualquiera de estas condiciones puede causar la muerte o una discapacidad grave.
Fumar aumenta mucho la posibilidad de sufrir infartos y accidentes cerebrovasculares. Además, fumar y el uso de anticonceptivos orales aumentan en gran medida las posibilidades de desarrollar y morir de enfermedades del corazón.
3. Enfermedad de la vesícula biliar
Las usuarias de anticonceptivos orales probablemente tengan un mayor riesgo que las no usuarias de tener enfermedad de la vesícula biliar, aunque este riesgo puede estar relacionado con las píldoras que contienen altas dosis de estrógenos.
4. Tumores hepáticos
En casos raros, los anticonceptivos orales pueden causar tumores hepáticos benignos pero peligrosos. Estos tumores hepáticos benignos pueden romperse y causar una hemorragia interna letal. Además, se encontró una asociación posible, pero no definitiva, con la píldora y los cánceres de hígado en dos estudios, en los que se encontró que algunas mujeres que desarrollaron estos cánceres muy raros habían usado anticonceptivos orales durante períodos prolongados. Sin embargo, los cánceres de hígado son extremadamente raros. La posibilidad de desarrollar cáncer de hígado por el uso de la píldora es aún más rara.
5. Cáncer de los órganos reproductores y de las mamas
Hay conflicto entre los estudios sobre el cáncer de mama y el uso de anticonceptivos orales. Algunos estudios han informado un aumento en el riesgo de desarrollar cáncer de mama, particularmente a una edad más temprana. Este aumento del riesgo parece estar relacionado con la duración del uso. La mayoría de los estudios no han encontrado un aumento general en el riesgo de desarrollar cáncer de mama.
Algunos estudios han encontrado un aumento en la incidencia de cáncer de cuello uterino en mujeres que usan anticonceptivos orales. Sin embargo, este hallazgo puede estar relacionado con otros factores además del uso de anticonceptivos orales. No hay evidencia suficiente para descartar la posibilidad de que las píldoras puedan causar tales tipos de cáncer.
RIESGO ESTIMADO DE MUERTE POR UN MÉTODO ANTICONCEPTIVO O EMBARAZO
Todos los métodos de control de la natalidad y el embarazo están asociados con el riesgo de desarrollar ciertas enfermedades que pueden conducir a la discapacidad o la muerte. Se ha calculado una estimación del número de muertes asociadas con diferentes métodos de control de la natalidad y el embarazo y se muestra en la siguiente tabla.
NÚMERO ANUAL DE MUERTES RELACIONADAS CON EL NACIMIENTO O EL MÉTODO ASOCIADAS AL CONTROL DE LA FERTILIDAD POR CADA 100.000 MUJERES NO ESTÉRILES, POR EL MÉTODO DE CONTROL DE LA FERTILIDAD SEGÚN LA EDAD
En la tabla anterior, el riesgo de muerte por cualquier método anticonceptivo es menor que el riesgo de parto, excepto para las usuarias de anticonceptivos orales mayores de 35 años que fuman y las usuarias de píldoras mayores de 40 años, incluso si no fuman. En la tabla se puede ver que para las mujeres de 15 a 39 años, el riesgo de muerte fue mayor con el embarazo (7 a 26 muertes por 100.000 mujeres, dependiendo de la edad). Entre las usuarias de píldoras que no fuman, el riesgo de muerte es siempre menor que el asociado al embarazo para cualquier grupo de edad, aunque a partir de los 40 años el riesgo aumenta a 32 muertes por cada 100.000 mujeres, frente a las 28 asociadas al embarazo en ese momento. años. Sin embargo, para las usuarias de píldoras que fuman y tienen más de 35 años, el número estimado de muertes supera las de otros métodos anticonceptivos. Si una mujer tiene más de 40 años y fuma, su riesgo estimado de muerte es cuatro veces mayor (117/100.000 mujeres) que el riesgo estimado asociado con el embarazo (28/100.000 mujeres) en ese grupo de edad.
La sugerencia de que las mujeres mayores de 40 años que no fuman no deben tomar anticonceptivos orales se basa en información de píldoras de dosis altas más antiguas y en un uso menos selectivo de las píldoras que el que se practica en la actualidad. Un comité asesor de la FDA discutió este tema en 1989 y recomendó que los beneficios del uso de anticonceptivos orales por parte de mujeres saludables mayores de 40 años que no fuman pueden superar los posibles riesgos. Sin embargo, se advierte a todas las mujeres, especialmente a las mujeres mayores, que usen la píldora de dosis más baja que sea efectiva.
SEÑALES DE ADVERTENCIA
Si cualquiera de estos efectos adversos ocurre mientras toma anticonceptivos orales, llame a su médico o proveedor de atención médica de inmediato:
- Dolor agudo en el pecho, tos con sangre o dificultad para respirar repentina (lo que indica un posible coágulo en el pulmón)
- Dolor en la pantorrilla (que indica un posible coágulo en la pierna)
- Dolor opresivo en el pecho o pesadez en el pecho (lo que indica un posible ataque al corazón)
- Dolor de cabeza intenso y repentino o vómitos, mareos o desmayos, alteraciones de la visión o del habla, debilidad o entumecimiento en un brazo o una pierna (que indican un posible derrame cerebral)
- Pérdida repentina parcial o completa de la visión (lo que indica un posible coágulo en el ojo)
- Bultos en los senos (que indican posible cáncer de seno o enfermedad fibroquística del seno; pídale a su médico o proveedor de atención médica que le muestre cómo examinar sus senos)
- Dolor intenso o sensibilidad en el área del estómago (lo que indica un tumor hepático posiblemente roto)
- Dificultad para dormir, debilidad, falta de energía, fatiga o cambios de humor (posiblemente indicando depresión severa)
- Ictericia o coloración amarillenta de la piel o los globos oculares, acompañada frecuentemente de fiebre, fatiga, pérdida de apetito, orina de color oscuro o heces de color claro (lo que indica posibles problemas hepáticos).
EFECTOS SECUNDARIOS DE LOS ANTICONCEPTIVOS ORALES
1. Sangrado vaginal
Puede ocurrir sangrado vaginal irregular o manchado mientras toma las píldoras. El sangrado irregular puede variar desde una ligera tinción entre períodos menstruales hasta un sangrado intermenstrual, que es un flujo muy parecido a un período regular. El sangrado irregular ocurre con mayor frecuencia durante los primeros meses de uso de anticonceptivos orales, pero también puede ocurrir después de haber estado tomando la píldora durante algún tiempo. Dicho sangrado puede ser temporal y por lo general no indica ningún problema grave. Es importante continuar tomando sus píldoras a tiempo. Si el sangrado ocurre en más de un ciclo o dura más de unos pocos días, hable con su médico o proveedor de atención médica.
2. Lentes de contacto
Si usa lentes de contacto y nota un cambio en la visión o una incapacidad para usar sus lentes, comuníquese con su médico o proveedor de atención médica.
3. Retención de líquidos
Los anticonceptivos orales pueden causar edema (retención de líquidos) con hinchazón de los dedos o los tobillos y pueden elevar la presión arterial. Si experimenta retención de líquidos, comuníquese con su médico o proveedor de atención médica.
4. Melasmas
Es posible un oscurecimiento irregular de la piel, particularmente de la cara.
5. Otros efectos secundarios
Otros efectos secundarios pueden incluir náuseas y vómitos, cambios en el apetito, dolor de cabeza, nerviosismo, depresión, mareos, pérdida del cabello del cuero cabelludo, sarpullido e infecciones vaginales.
Si alguno de estos efectos secundarios le molesta, llame a su médico o proveedor de atención médica.
PRECAUCIONES GENERALES
1. Períodos perdidos y uso de anticonceptivos orales antes o durante el embarazo temprano
Puede haber ocasiones en las que no menstrúe con regularidad después de haber terminado de tomar un ciclo de píldoras. Si ha tomado sus píldoras con regularidad y no tiene un período menstrual, continúe tomándolas durante el próximo ciclo, pero asegúrese de informar a su médico o proveedor de atención médica antes de hacerlo. Si no ha tomado las píldoras diariamente según las instrucciones y no tuvo un período menstrual, o si no tuvo dos períodos menstruales consecutivos, es posible que esté embarazada. Consulte con su médico o proveedor de atención médica de inmediato para determinar si está embarazada. No continúe tomando anticonceptivos orales hasta que esté segura de que no está embarazada, pero continúe usando otro método anticonceptivo.
No hay evidencia concluyente de que el uso de anticonceptivos orales se asocie con un aumento de defectos de nacimiento, cuando se toman inadvertidamente durante el embarazo temprano. Anteriormente, algunos estudios informaron que los anticonceptivos orales podrían estar asociados con defectos de nacimiento, pero estos estudios no han sido confirmados. Sin embargo, los anticonceptivos orales o cualquier otro medicamento no deben usarse durante el embarazo a menos que sea claramente necesario y lo haya recetado su médico o proveedor de atención médica. Debe consultar con su médico o proveedor de atención médica sobre los riesgos para su hijo por nacer de cualquier medicamento que tome durante el embarazo.
2. Durante la lactancia
Si está amamantando, consulte a su médico o proveedor de atención médica antes de comenzar a tomar anticonceptivos orales. Parte del medicamento pasará al niño a través de la leche. Se han informado algunos efectos adversos en el niño, que incluyen coloración amarillenta de la piel (ictericia) y agrandamiento de los senos. Además, los anticonceptivos orales pueden disminuir la cantidad y calidad de su leche. Si es posible, no use anticonceptivos orales durante la lactancia. Debe utilizar otro método anticonceptivo, ya que la lactancia materna solo proporciona una protección parcial contra el embarazo y esta protección parcial disminuye significativamente a medida que amamanta durante períodos más prolongados.
Debe considerar comenzar con los anticonceptivos orales solo después de haber destetado a su hijo por completo.
3. Pruebas de laboratorio
Si tiene programada alguna prueba de laboratorio, informe a su médico o proveedor de atención médica que está tomando píldoras anticonceptivas. Ciertos análisis de sangre pueden verse afectados por las píldoras anticonceptivas.
4. Interacciones medicamentosas
Ciertos medicamentos pueden interactuar con las píldoras anticonceptivas y hacerlas menos efectivas para prevenir el embarazo o causar un aumento en el sangrado intermenstrual. Dichos medicamentos incluyen rifampicina, medicamentos utilizados para la epilepsia como barbitúricos (por ejemplo, fenobarbital), fenitoína (Dilantin® es una marca de este medicamento), fenilbutazona (Butazolidin® es una marca) y posiblemente ciertos antibióticos. Es posible que necesite utilizar métodos anticonceptivos adicionales cuando tome medicamentos que pueden hacer que los anticonceptivos orales sean menos efectivos.
Las píldoras anticonceptivas pueden interactuar con lamotrigina, un anticonvulsivo que se usa para la epilepsia. Esto puede aumentar el riesgo de convulsiones, por lo que es posible que su médico deba ajustar la dosis de lamotrigina.
Algunos medicamentos pueden hacer que la píldora anticonceptiva sea menos efectiva, entre ellos:
- barbitúricos
- bosentán
- Carbamazepina
- Felbamato
- griseofulvina
- Oxcarbazepina
- fenitoína
- rifampicina
- Hierba de San Juan
- topiramato
Al igual que con todos los productos recetados, debe informar a su proveedor de atención médica sobre cualquier otro medicamento o producto a base de hierbas que esté tomando. Es posible que deba usar un anticonceptivo de barrera cuando tome medicamentos o productos que pueden hacer que las píldoras anticonceptivas sean menos efectivas.
5. Enfermedades de transmisión sexual
Este producto (como todos los anticonceptivos orales) está destinado a prevenir el embarazo. No protege contra la transmisión del VIH (SIDA) y otras enfermedades de transmisión sexual como la clamidia, el herpes genital, las verrugas genitales, la gonorrea, la hepatitis B y la sífilis.
COMO TOMAR LA PASTILLA
PUNTOS IMPORTANTES A RECORDAR
ANTES DE EMPEZAR A TOMAR SUS PASTILLAS:
1. ASEGÚRESE DE LEER ESTAS INSTRUCCIONES:
Antes de empezar a tomar sus pastillas.
En cualquier momento usted no está seguro de qué hacer.
2. LA FORMA CORRECTA DE TOMAR LA PASTILLA ES TOMAR UNA PASTILLA TODOS LOS DÍAS A LA MISMA HORA.
Si olvidas las pastillas podrías quedar embarazada. Esto incluye poner en marcha el paquete de tarde.
Cuantas más píldoras olvide, más probable es que quede embarazada.
3. MUCHAS MUJERES TIENEN MANCHADO O SANGRADO LIGERO, O PUEDEN SENTIR NEGOCIO DEL ESTÓMAGO DURANTE LOS PRIMEROS 1 A 3 PAQUETES DE PÍLDORAS.
Si se siente mal del estómago, no deje de tomar la píldora. El problema normalmente desaparecerá. Si no desaparece, consulte con su médico o proveedor de atención médica.
4. LAS PÍLDORAS FALTANTES TAMBIÉN PUEDEN PROVOCAR MANCHAS O SANGRADO LEVE, incluso cuando se reponga las píldoras olvidadas.
En los días que tome 2 píldoras para compensar las píldoras olvidadas, también podría sentirse un poco mal del estómago.
5. SI TIENE VÓMITOS O DIARREA, por cualquier motivo, o SI TOMA ALGUNOS MEDICAMENTOS, incluidos algunos antibióticos, es posible que sus pastillas no funcionen tan bien.
Use un método de respaldo (como condones, espuma o esponja) hasta que consulte con su médico o proveedor de atención médica.
6. SI TIENE PROBLEMAS PARA RECORDAR TOMAR LA PÍLDORA, hable con su médico o proveedor de atención médica sobre cómo hacer que tomar la píldora sea más fácil o sobre cómo usar otro método anticonceptivo.
7. SI TIENE ALGUNA PREGUNTA O NO ESTÁ SEGURO SOBRE LA INFORMACIÓN EN ESTE FOLLETO, llame a su médico o proveedor de atención médica.
ANTES DE EMPEZAR A TOMAR SUS PASTILLAS
8. DECIDA A QUÉ HORA DEL DÍA QUIERE TOMAR SU PASTILLA.
Es importante tomarlo aproximadamente a la misma hora todos los días.
8. MIRA TU PAQUETE DE PASTILLAS: TENDRÁ 28 PASTILLAS:
Este paquete de 28 píldoras contiene 26 píldoras “activas” [blancas y amarillas] (con hormonas) y 2 píldoras “inactivas” [verde claro] (sin hormonas).
10. ENCUENTRA TAMBIÉN:
1) en qué parte del paquete comenzar a tomar las píldoras,
2) en qué orden tomar las pastillas (siga las flechas) y
3) los números de semana como se muestra en la imagen de abajo.
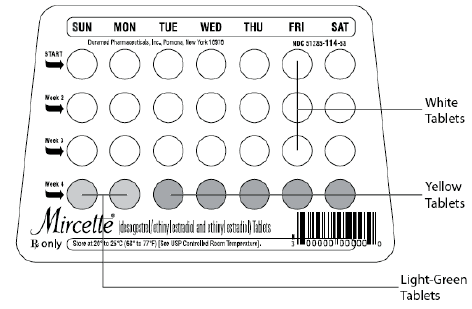
11. ASEGÚRESE DE TENER LISTO EN TODO MOMENTO:
OTRO TIPO DE CONTROL DE LA NATALIDAD (como condones, espuma o esponja) para usar como respaldo en caso de que olvide las píldoras.
UN PAQUETE DE PASTILLAS EXTRA COMPLETO.
CUANDO EMPEZAR EL PRIMER PAQUETE DE PASTILLAS
Puede elegir qué día empezar a tomar su primer paquete de píldoras. Decida con su médico o proveedor de atención médica cuál es el mejor día para usted. Elija una hora del día que sea fácil de recordar.
DÍA 1 INICIO
12. Elija la tira de la etiqueta del día que comienza con el primer día de su período (este es el día en que comienza a sangrar o manchar, incluso si es casi medianoche cuando comienza el sangrado).
13. Coloque esta tira de etiquetas de días en el dispensador de tabletas para ciclos sobre el área que tiene impresos los días de la semana (empezando por el domingo).
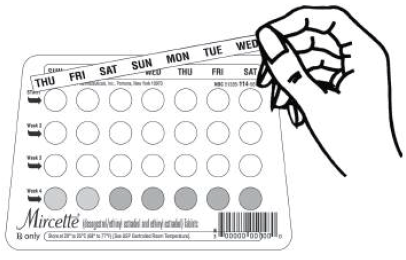
Nota: si el primer día de su período es domingo, puede omitir los pasos 1 y 2.
14. Tome la primera píldora “activa” [blanca] del primer paquete durante las primeras 24 horas de su período.
15. No necesitará usar un método anticonceptivo de respaldo, ya que comenzará a tomar la píldora al comienzo de su período.
DOMINGO INICIO
16. Tome la primera píldora “activa” [blanca] del primer paquete el domingo después de que comience su período, incluso si todavía está sangrando. Si tu regla comienza el domingo, comienza el paquete ese mismo día.
17. Use otro método anticonceptivo como método de respaldo si tiene relaciones sexuales en cualquier momento desde el domingo en que comienza su primer paquete hasta el próximo domingo (7 días). Los condones, la espuma o la esponja son buenos métodos anticonceptivos de respaldo.
QUÉ HACER DURANTE EL MES
18. TOME UNA PASTILLA A LA MISMA HORA TODOS LOS DÍAS HASTA QUE EL ENVASE ESTÉ VACÍO.
No omita las píldoras incluso si está manchando o sangrando entre períodos mensuales o si siente malestar estomacal (náuseas).
No se salte las píldoras, incluso si no tiene relaciones sexuales con mucha frecuencia.
19. CUANDO TERMINA UN PAQUETE O CAMBIA SU MARCA DE PÍLDORAS:
21 pastillas : Espere 7 días para comenzar el siguiente paquete. Probablemente tendrá su período durante esa semana. Asegúrese de que no pasen más de 7 días entre paquetes de 21 días.
28 pastillas : Comience el próximo paquete el día después de su última píldora. No espere ningún día entre paquetes.
QUÉ HACER SI DEJA DE TOMAR PASTILLAS
Si OLVIDA 1 pastilla “activa” [blanca]:
20. Tómelo tan pronto como lo recuerde. Tome la siguiente píldora a la hora habitual. Esto significa que toma 2 pastillas en 1 día.
21. No necesita usar un método anticonceptivo de respaldo si tiene relaciones sexuales. Si OLVIDA 2 píldoras “activas” [blancas] seguidas en la SEMANA 1 O LA SEMANA 2 de su paquete:
22. Tome 2 pastillas el día que se acuerde y 2 pastillas al día siguiente.
23. Luego tome 1 pastilla al día hasta terminar el paquete.
24. PUEDE QUEDAR EMBARAZADA si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras. DEBE usar otro método anticonceptivo (como condones, espuma o esponja) como método de respaldo durante esos 7 días.
Si OLVIDA 2 píldoras “activas” [blancas] seguidas en la SEMANA 3:
25. Si eres un principiante del día 1:
DESECHE el resto del paquete de píldoras y comience un nuevo paquete ese mismo día.
Si eres un Sunday Starter:
Siga tomando 1 pastilla todos los días hasta el domingo.
El domingo, BOTE el resto del paquete y comience un nuevo paquete de píldoras ese mismo día.
26. Es posible que no tenga su período este mes, pero es de esperar. Sin embargo, si pierde su período 2 meses seguidos, llame a su médico o proveedor de atención médica porque podría estar embarazada.
27. PUEDE QUEDAR EMBARAZADA si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras. DEBE usar otro método anticonceptivo (como condones, espuma o esponja) como método de respaldo durante esos 7 días.
Si usted PERDER 3 O MAS Píldoras “activas” [blancas] seguidas (durante las primeras 3 semanas):
28. Si eres un principiante del día 1:
DESECHE el resto del paquete de píldoras y comience un nuevo paquete ese mismo día.
Si eres un Sunday Starter:
Siga tomando 1 pastilla todos los días hasta el domingo.
El domingo, BOTE el resto del paquete y comience un nuevo paquete de píldoras ese mismo día.
29. Es posible que no tenga su período este mes, pero esto se espera. Sin embargo, si pierde su período 2 meses seguidos, llame a su médico o proveedor de atención médica porque podría estar embarazada.
30. PUEDE QUEDAR EMBARAZADA si tiene relaciones sexuales en los 7 días posteriores a la omisión de las píldoras. DEBE usar otro método anticonceptivo (como condones, espuma o esponja) como método de respaldo durante esos 7 días.
RECORDATORIO PARA AQUELLOS EN PAQUETES DE 28 DÍAS
Si olvida alguna de las 2 pastillas [verde claro] o 5 [amarillas] en la Semana 4:
DESECHE las píldoras que se olvidó.
Continúe tomando 1 pastilla cada día hasta que el paquete esté vacío.
No necesita un método de respaldo.
POR ÚLTIMO, SI AÚN NO ESTÁS SEGURO DE QUÉ HACER CON LAS PASTILLAS QUE TE HAS PERDIDO
Use un MÉTODO DE RESPALDO cada vez que tenga relaciones sexuales.
SIGA TOMANDO UNA PASTILLA “ACTIVA” [BLANCA] CADA DÍA hasta que pueda comunicarse con su médico o proveedor de atención médica.
EMBARAZO POR FALLA DE LA PÍLDORA
La incidencia de falla de la píldora que resulta en un embarazo es de aproximadamente uno por ciento (es decir, un embarazo por cada 100 mujeres por año) si se toma todos los días según las indicaciones, pero las tasas de falla más típicas son de alrededor del 5%. Si ocurre una falla, el riesgo para el feto es mínimo.
EMBARAZO DESPUÉS DE DEJAR LA PÍLDORA
Puede haber algún retraso en quedar embarazada después de dejar de usar anticonceptivos orales, especialmente si tenía ciclos menstruales irregulares antes de usar anticonceptivos orales. Puede ser recomendable posponer la concepción hasta que comience a menstruar regularmente una vez que haya dejado de tomar la píldora y desee quedar embarazada.
No parece haber ningún aumento en los defectos de nacimiento en los recién nacidos cuando el embarazo se produce poco después de dejar de tomar la píldora.
SOBREDOSIS
No se han informado efectos nocivos graves luego de la ingestión de grandes dosis de anticonceptivos orales por parte de niños pequeños. La sobredosis puede causar náuseas y sangrado por deprivación en las mujeres. En caso de sobredosis, comuníquese con su médico, proveedor de atención médica o farmacéutico.
OTRA INFORMACIÓN
Su médico o proveedor de atención médica tomará un historial médico y familiar antes de recetarle anticonceptivos orales y la examinará. El examen físico puede retrasarse para otro momento si usted lo solicita y su médico o el proveedor de atención médica cree que es una buena práctica médica posponerlo. Usted debe volver a examinarse al menos una vez al año. Asegúrese de informar a su médico o proveedor de atención médica si hay antecedentes familiares de cualquiera de las condiciones enumeradas anteriormente en este prospecto. Asegúrese de asistir a todas las citas con su médico o proveedor de atención médica, porque este es un momento para determinar si hay signos tempranos de efectos secundarios del uso de anticonceptivos orales.
No use el medicamento para ninguna condición que no sea para la que fue recetado. Este medicamento ha sido recetado específicamente para usted; no se la dé a otras personas que quieran píldoras anticonceptivas.
BENEFICIOS PARA LA SALUD DE LOS ANTICONCEPTIVOS ORALES
Además de prevenir el embarazo, el uso de anticonceptivos orales combinados puede brindar ciertos beneficios. Están:
- los ciclos menstruales pueden volverse más regulares.
- el flujo de sangre durante la menstruación puede ser más ligero y se puede perder menos hierro. Por lo tanto, es menos probable que ocurra anemia debido a la deficiencia de hierro.
- el dolor u otros síntomas durante la menstruación pueden encontrarse con menos frecuencia.
- el embarazo ectópico (tubárico) puede ocurrir con menos frecuencia.
- Los quistes o bultos no cancerosos en el seno pueden ocurrir con menos frecuencia.
- la enfermedad pélvica inflamatoria aguda puede ocurrir con menos frecuencia.
- el uso de anticonceptivos orales puede brindar cierta protección contra el desarrollo de dos formas de cáncer: cáncer de ovario y cáncer del revestimiento del útero.
Si desea obtener más información sobre las píldoras anticonceptivas, consulte a su médico, proveedor de atención médica o farmacéutico. Tienen un folleto más técnico llamado Información de prescripción que tal vez desee leer.
