Flonase Nasal Spray 50mcg Fluticasone Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Flonase y cómo se usa?
Flonase es un medicamento recetado que se usa para tratar los síntomas de la rinitis alérgica (estornudos, secreción nasal y ojos llorosos o con comezón) y los pólipos nasales. Flonase se puede usar solo o con otros medicamentos.
Flonase pertenece a una clase de medicamentos llamados corticosteroides, intranasales, inmunosupresores, PHD.
No se sabe si Flonase es seguro y eficaz en niños menores de 4 años.
¿Cuáles son los posibles efectos secundarios de Flonase?
Flonase puede causar efectos secundarios graves que incluyen:
- hemorragias nasales graves o continuas,
- respiración ruidosa,
- nariz que moquea,
- costras alrededor de tus fosas nasales,
- enrojecimiento, llagas o manchas blancas en la boca o la garganta,
- fiebre,
- escalofríos,
- dolor de cuerpo,
- visión borrosa,
- dolor de ojo,
- viendo halos alrededor de las luces,
- heridas que no cicatrizan,
- empeoramiento del cansancio,
- debilidad muscular,
- aturdimiento,
- náuseas, y
- vómitos
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Flonase incluyen:
- hemorragia nasal menor,
- ardor o picazón en la nariz,
- llagas o manchas blancas dentro o alrededor de la nariz,
- tos,
- dificultad para respirar,
- dolor de cabeza,
- dolor de espalda,
- dolor de sinusitis,
- dolor de garganta,
- fiebre,
- náuseas, y
- vómitos
DESCRIPCIÓN
El componente activo de FLONASE Nasal Spray 50mcg es propionato de fluticasona, un corticosteroide con el nombre químico S-(fluorometil) 6α,9-difluoro-11β,17-dihidroxi-16α-metil-3oxoandrosta-1,4-dieno-17β-carbotioato , 17-propionato y la siguiente estructura química:
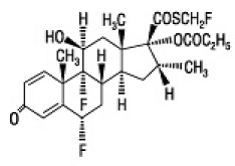
El propionato de fluticasona es un polvo blanco con un peso molecular de 500,6 y la fórmula empírica es C25H31F3O5S. Es prácticamente insoluble en agua, libremente soluble en dimetilsulfóxido y dimetilformamida, y ligeramente soluble en metanol y etanol al 95%.
FLONASE Aerosol Nasal, 50 mcg es una suspensión acuosa de propionato de fluticasona microfino para administración tópica en la mucosa nasal por medio de una bomba atomizadora dosificadora. El aerosol nasal FLONASE de 50 mcg también contiene celulosa microcristalina y carboximetilcelulosa sódica, dextrosa, cloruro de benzalconio al 0,02 % p/p, polisorbato 80 y alcohol feniletílico al 0,25 % p/p, y tiene un pH entre 5 y 7.
Después del cebado inicial, cada activación libera 50 mcg de propionato de fluticasona en 100 mg de formulación a través del adaptador nasal.
INDICACIONES
FLONASE® Nasal Spray está indicado para el tratamiento de los síntomas nasales de la rinitis no alérgica perenne en pacientes adultos y pediátricos a partir de los 4 años.
DOSIFICACIÓN Y ADMINISTRACIÓN
Administre el aerosol nasal FLONASE solo por vía intranasal. Prepare el aerosol nasal FLONASE antes de usarlo por primera vez o después de un período sin uso (1 semana o más) agitando bien el contenido y liberando 6 aerosoles en el aire lejos de la cara. Agite el aerosol nasal FLONASE suavemente antes de cada uso.
Los pacientes deben usar FLONASE Spray Nasal a intervalos regulares ya que su efectividad depende de su uso regular. El efecto máximo puede demorar varios días y los pacientes individuales experimentarán un tiempo variable hasta el inicio y un grado diferente de alivio de los síntomas.
Adultos
La dosis inicial recomendada en adultos es de 2 pulverizaciones (50 mcg de propionato de fluticasona cada una) en cada fosa nasal una vez al día (dosis diaria total, 200 mcg). La misma dosis diaria total, 1 pulverización en cada fosa nasal administrada dos veces al día (p. ej., 8 am y 8 pm) también es eficaz. Después de los primeros días, los pacientes pueden reducir su dosis a 1 pulverización en cada fosa nasal una vez al día para la terapia de mantenimiento.
Las dosis diarias totales máximas no deben exceder las 2 aplicaciones en cada fosa nasal (dosis total, 200 mcg/día). No hay evidencia de que exceder la dosis recomendada sea más efectivo.
Adolescentes y niños (mayores de 4 años)
La dosis inicial recomendada en adolescentes y niños mayores de 4 años es 1 pulverización en cada fosa nasal una vez al día (dosis diaria total, 100 mcg). Los pacientes que no respondan adecuadamente a 1 pulverización en cada fosa nasal pueden usar 2 pulverizaciones en cada fosa nasal una vez al día (dosis diaria total, 200 mcg). Una vez que se logra un control adecuado, la dosis debe reducirse a 1 pulverización en cada fosa nasal una vez al día.
La dosis máxima diaria total no debe exceder de 2 pulverizaciones en cada fosa nasal (200 mcg/día). No hay evidencia de que exceder la dosis recomendada sea más efectivo.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
FLONASE Aerosol Nasal es una suspensión de aerosol nasal. Cada spray de 100 mg proporciona 50 mcg de propionato de fluticasona.
Almacenamiento y manipulación
FLONAS El aerosol nasal, 50 mcg, se suministra en una botella de vidrio ámbar equipada con una bomba dosificadora atomizadora blanca, un adaptador nasal blanco y una cubierta antipolvo verde en una caja de 1 ( CDN 0173-0453-01) con aprobado por la FDA Etiquetado de pacientes (ver Instrucciones de uso para el paciente para la correcta actuación del dispositivo ). Cada botella contiene un peso neto de llenado de 16 g y proporcionará 120 actuaciones. Cada actuación libera 50 mcg de propionato de fluticasona en 100 mg de formulación a través del adaptador nasal. No se puede asegurar la cantidad correcta de medicamento en cada atomización después de 120 atomizaciones aunque la botella no esté completamente vacía. La botella debe desecharse cuando se haya utilizado el número de actuaciones indicado en la etiqueta.
Almacenar entre 4° y 30°C (39° y 86°F).
GlaxoSmithKline Research Triangle Park, NC 27709. Revisado: enero de 2015EFECTOS SECUNDARIOS
El uso de corticosteroides sistémicos y locales puede resultar en lo siguiente:
- Epistaxis, ulceración nasal, infección por Candida albicans, perforación del tabique nasal y alteración de la cicatrización de heridas [ver ADVERTENCIAS Y PRECAUCIONES ]
- Cataratas y glaucoma [ver ADVERTENCIAS Y PRECAUCIONES ]
- Inmunosupresión [ver ADVERTENCIAS Y PRECAUCIONES ]
- Hipercorticismo y supresión suprarrenal [ver ADVERTENCIAS Y PRECAUCIONES ]
- Efecto sobre el crecimiento [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variables, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica.
En ensayos clínicos controlados en los EE. UU., más de 3300 sujetos con rinitis alérgica y no alérgica recibieron tratamiento con propionato de fluticasona intranasal. En general, las reacciones adversas en los ensayos clínicos se han asociado principalmente con la irritación de las membranas mucosas nasales, y las reacciones adversas se informaron con aproximadamente la misma frecuencia en sujetos tratados con placebo. Menos del 2% de los sujetos en ensayos clínicos interrumpieron debido a reacciones adversas; esta tasa fue similar para el vehículo placebo y los comparadores activos.
Los datos de seguridad que se describen a continuación se basan en 7 ensayos clínicos controlados con placebo en sujetos con rinitis alérgica. Los 7 ensayos incluyeron 536 sujetos (57 niñas y 108 niños de 4 a 11 años, 137 mujeres y 234 hombres adolescentes y adultos) tratados con FLONASE 200 mcg una vez al día durante 2 a 4 semanas y 2 ensayos clínicos controlados con placebo que incluyeron 246 sujetos (119 mujeres y 127 hombres adolescentes y adultos) tratados con FLONASE 200 mcg una vez al día durante 6 meses (Tabla 1). En la Tabla 1 también se incluyen las reacciones adversas de 2 ensayos en los que 167 niños (45 niñas y 122 niños de 4 a 11 años) fueron tratados con 100 mcg de FLONASE una vez al día durante 2 a 4 semanas.
Otras reacciones adversas con FLONASE Aerosol Nasal 50 mcg observadas con una incidencia menor o igual al 3% pero mayor o igual al 1% y más comunes que con placebo incluyeron: sangre en la mucosidad nasal, secreción nasal, dolor abdominal, diarrea, fiebre, síntomas parecidos a la gripe, dolores y molestias, mareos y bronquitis.
Experiencia posterior a la comercialización
Además de los eventos adversos informados en los ensayos clínicos, se identificaron los siguientes eventos adversos durante el uso posterior a la aprobación del propionato de fluticasona intranasal. Debido a que estas reacciones son informadas voluntariamente por una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco. Estos eventos se eligieron para su inclusión debido a su gravedad, frecuencia de notificación o conexión causal con el propionato de fluticasona o una combinación de estos factores.
Desordenes generales y condiciones administrativas del sitio
Reacciones de hipersensibilidad, que incluyen angioedema, erupción cutánea, edema de la cara y la lengua, prurito, urticaria, broncoespasmo, sibilancias, disnea y anafilaxia/reacciones anafilactoides, que en raras ocasiones fueron graves.
Trastornos del oído y del laberinto
Alteración o pérdida del sentido del gusto y/u olfato y, raramente, perforación del tabique nasal, úlcera nasal, dolor de garganta, irritación y sequedad de garganta, tos, ronquera y cambios en la voz.
Trastornos oculares
Sequedad e irritación, conjuntivitis, visión borrosa, glaucoma, aumento de la presión intraocular y cataratas.
Se han notificado casos de supresión del crecimiento con los corticosteroides intranasales, incluido FLONASE [ver ADVERTENCIAS Y PRECAUCIONES ].
INTERACCIONES CON LA DROGAS
Inhibidores del citocromo P450 3A4
El propionato de fluticasona es un sustrato de CYP3A4. No se recomienda el uso de inhibidores potentes de CYP3A4 (p. ej., ritonavir, atazanavir, claritromicina, indinavir, itraconazol, nefazodona, nelfinavir, saquinavir, ketoconazol, telitromicina, conivaptán, lopinavir, nefazodona, voriconazol) con el aerosol nasal FLONASE porque aumentan los efectos adversos sistémicos de los corticosteroides. puede ocurrir.
ritonavir
Un ensayo de interacción farmacológica con el aerosol nasal acuoso de propionato de fluticasona en sujetos sanos ha demostrado que el ritonavir (un potente inhibidor de CYP3A4) puede aumentar significativamente la exposición plasmática del propionato de fluticasona, lo que da como resultado concentraciones séricas de cortisol significativamente reducidas [ver FARMACOLOGÍA CLÍNICA ]. Durante el uso posterior a la comercialización, hubo informes de interacciones farmacológicas clínicamente significativas en pacientes que recibieron productos de propionato de fluticasona, incluido FLONASE, con ritonavir, lo que resultó en efectos corticosteroides sistémicos, incluido el síndrome de Cushing y la supresión suprarrenal.
ketoconazol
La administración conjunta de propionato de fluticasona inhalado por vía oral (1000 mcg) y ketoconazol (200 mg una vez al día) resultó en un aumento de 1,9 veces en la exposición de propionato de fluticasona en plasma y una disminución del 45 % en el área bajo la curva (AUC) de cortisol en plasma, pero no tuvo ningún efecto. en la excreción urinaria de cortisol.
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Efectos nasales locales
Epistaxis
En ensayos clínicos de 2 a 26 semanas de duración, se observó epistaxis con mayor frecuencia en sujetos tratados con FLONASE Aerosol Nasal que en aquellos que recibieron placebo [ver REACCIONES ADVERSAS ].
Ulceración Nasal
Se han informado casos posteriores a la comercialización de ulceración nasal en pacientes tratados con FLONASE Aerosol Nasal [ver REACCIONES ADVERSAS ].
infección por cándida
En ensayos clínicos con propionato de fluticasona administrado por vía intranasal, se ha producido el desarrollo de infecciones localizadas de nariz y faringe por Candida albicans. Cuando se desarrolla una infección de este tipo, puede requerir tratamiento con la terapia local adecuada y la interrupción del aerosol nasal FLONASE. Los pacientes que usen el aerosol nasal FLONASE durante varios meses o más deben ser examinados periódicamente para detectar evidencia de infección por Candida u otros signos de efectos adversos en la mucosa nasal.
Perforación del tabique nasal
Se han informado casos posteriores a la comercialización de perforación del tabique nasal en pacientes tratados con FLONASE Aerosol Nasal [ver REACCIONES ADVERSAS ].
Deterioro de la cicatrización de heridas
Debido al efecto inhibitorio de los corticosteroides sobre la cicatrización de heridas, los pacientes que han experimentado úlceras nasales recientes, cirugía nasal o traumatismo nasal deben evitar el uso del aerosol nasal FLONASE hasta que se haya producido la cicatrización.
Glaucoma y Cataratas
El uso de corticosteroides intranasales e inhalados puede resultar en el desarrollo de glaucoma y/o cataratas. Por lo tanto, se justifica una estrecha vigilancia en pacientes con cambios en la visión o con antecedentes de aumento de la presión intraocular, glaucoma y/o cataratas.
Reacciones de hipersensibilidad, incluida la anafilaxia
Se han informado reacciones de hipersensibilidad (p. ej., anafilaxia, angioedema, urticaria, dermatitis de contacto y sarpullido) después de la administración de FLONASE en aerosol nasal. Suspender FLONASE
Aerosol nasal si ocurren tales reacciones [ver CONTRAINDICACIONES ]. En raras ocasiones, pueden ocurrir reacciones de hipersensibilidad inmediata después de la administración de FLONASE Spray Nasal.
Inmunosupresión
Las personas que consumen medicamentos que suprimen el sistema inmunitario son más susceptibles a las infecciones que las personas sanas. La varicela y el sarampión, por ejemplo, pueden tener un curso más grave o incluso fatal en niños o adultos susceptibles que usan corticosteroides. En tales niños o adultos que no han tenido estas enfermedades o no han sido inmunizados adecuadamente, se debe tener especial cuidado para evitar la exposición. Se desconoce cómo la dosis, la vía y la duración de la administración de corticosteroides afectan el riesgo de desarrollar una infección diseminada. Tampoco se conoce la contribución de la enfermedad subyacente y/o el tratamiento previo con corticosteroides al riesgo. Si un paciente está expuesto a la varicela, puede estar indicada la profilaxis con inmunoglobulina contra la varicela zoster (IGVZ). Si un paciente está expuesto al sarampión, puede estar indicada la profilaxis con inmunoglobulina (IG) intramuscular combinada. (Ver la información de prescripción completa para VZIG e IG. Si se desarrolla varicela, se puede considerar el tratamiento con agentes antivirales.
Los corticosteroides intranasales deben usarse con precaución, si es que se usan, en pacientes con infecciones tuberculosas activas o quiescentes de las vías respiratorias; infecciones sistémicas fúngicas, bacterianas, virales o parasitarias; o herpes simple ocular.
Hipercorticismo y supresión suprarrenal
Cuando los corticosteroides intranasales se usan en dosis superiores a las recomendadas o en individuos susceptibles a las dosis recomendadas, pueden aparecer efectos corticosteroides sistémicos como hipercorticismo y supresión suprarrenal. Si ocurren tales cambios, la dosificación de FLONASE Aerosol nasal debe suspenderse lentamente de acuerdo con los procedimientos aceptados para suspender la terapia con corticosteroides orales.
La sustitución de un corticosteroide sistémico por un corticosteroide tópico puede acompañarse de signos de insuficiencia suprarrenal. Además, algunos pacientes pueden experimentar síntomas de abstinencia de corticosteroides (p. ej., dolor articular y/o muscular, cansancio, depresión). Los pacientes previamente tratados durante períodos prolongados con corticosteroides sistémicos y transferidos a corticosteroides tópicos deben ser monitoreados cuidadosamente por insuficiencia suprarrenal aguda en respuesta al estrés. En pacientes que tienen asma u otras condiciones clínicas que requieren tratamiento con corticosteroides sistémicos a largo plazo, las disminuciones rápidas en las dosis de corticosteroides sistémicos pueden causar una exacerbación severa de sus síntomas.
Interacciones farmacológicas con inhibidores potentes del citocromo P450 3A4
No se recomienda el uso de inhibidores potentes del citocromo P450 3A4 (CYP3A4) (p. ej., ritonavir, atazanavir, claritromicina, indinavir, itraconazol, nefazodona, nelfinavir, saquinavir, ketoconazol, telitromicina, conivaptán, lopinavir, nefazodona, voriconazol) con el aerosol nasal FLONASE porque pueden ocurrir efectos adversos de corticosteroides sistémicos aumentados [ver INTERACCIONES CON LA DROGAS , FARMACOLOGÍA CLÍNICA ].
Efecto sobre el crecimiento
Los corticosteroides intranasales pueden causar una reducción en la velocidad de crecimiento cuando se administran a pacientes pediátricos [ver Uso en poblaciones específicas ]. Supervise el crecimiento de forma rutinaria de los pacientes pediátricos que reciben el aerosol nasal FLONASE. Para minimizar los efectos sistémicos de los corticosteroides intranasales, incluido el aerosol nasal FLONASE, ajuste la dosis de cada paciente a la dosis más baja que controle eficazmente sus síntomas [ver DOSIFICACIÓN Y ADMINISTRACIÓN , Uso en poblaciones específicas ].
Información de asesoramiento para pacientes
Aconseje al paciente que lea la etiqueta del paciente aprobada por la FDA ( INFORMACIÓN DEL PACIENTE e Instrucciones de uso ).
Efectos nasales locales
Informe a los pacientes que el tratamiento con FLONASE Aerosol nasal de 50 mcg puede provocar reacciones adversas, que incluyen epistaxis y ulceración nasal. La infección por Candida también puede ocurrir con el tratamiento con FLONASE Aerosol Nasal. Además, FLONASE Aerosol nasal de 50 mcg se ha asociado con perforación del tabique nasal y problemas de cicatrización de heridas. Los pacientes que han experimentado úlceras nasales recientes, cirugía nasal o traumatismo nasal no deben usar el aerosol nasal FLONASE de 50 mcg hasta que se haya curado [ver ADVERTENCIAS Y PRECAUCIONES ].
Glaucoma y Cataratas
Informe a los pacientes que el glaucoma y las cataratas están asociados con el uso de corticosteroides nasales e inhalados. Aconseje a los pacientes que notifiquen a sus proveedores de atención médica si observan un cambio en la visión mientras usan el aerosol nasal FLONASE [ver ADVERTENCIAS Y PRECAUCIONES ].
Reacciones de hipersensibilidad, incluida la anafilaxia
Informe a los pacientes que pueden ocurrir reacciones de hipersensibilidad, que incluyen anafilaxia, angioedema, urticaria, dermatitis de contacto y sarpullido, después de la administración de FLONASE en aerosol nasal. Si ocurren tales reacciones, los pacientes deben suspender el uso de FLONASE Aerosol Nasal [ver ADVERTENCIAS Y PRECAUCIONES ].
Inmunosupresión
Advierta a los pacientes que reciben dosis inmunosupresoras de corticosteroides para evitar la exposición a la varicela o el sarampión y, si están expuestos, consulten a su proveedor de atención médica sin demora. Informar a los pacientes del posible empeoramiento de la tuberculosis existente; infecciones fúngicas, bacterianas, virales o parasitarias; o herpes simple ocular [ver ADVERTENCIAS Y PRECAUCIONES ].
Velocidad de crecimiento reducida
Aconseje a los padres que el aerosol nasal FLONASE de 50 mcg puede causar una reducción en la velocidad de crecimiento cuando se administra a pacientes pediátricos. Los médicos deben seguir de cerca el crecimiento de los niños y adolescentes que toman corticosteroides por cualquier vía [ver ADVERTENCIAS Y PRECAUCIONES , Uso pediátrico ].
Úselo diariamente para obtener el mejor efecto
Informe a los pacientes que deben usar FLONASE Aerosol nasal de 50 mcg de manera regular. FLONASE Aerosol Nasal 50 mcg, al igual que otros corticosteroides, no tiene un efecto inmediato sobre los síntomas de la rinitis. Es posible que no se alcance el beneficio máximo durante varios días. Los pacientes no deben aumentar la dosis prescrita, pero deben comunicarse con sus proveedores de atención médica si los síntomas no mejoran o si la afección empeora.
Mantenga el aerosol fuera de los ojos y la boca
Informe a los pacientes que eviten rociar el aerosol nasal FLONASE en los ojos y la boca.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
El propionato de fluticasona no demostró potencial tumorigénico en ratones con dosis orales de hasta 1000 mcg/kg (aproximadamente 20 veces la MRHDID en adultos y aproximadamente 10 veces la MRHDID en niños sobre una base de mcg/m²) durante 78 semanas o en ratas con dosis de inhalación de hasta a 57 mcg/kg (aproximadamente 2 veces la MRHDID en adultos y aproximadamente equivalente a la MRHDID en niños sobre una base de mcg/m²) durante 104 semanas.
El propionato de fluticasona no indujo mutaciones genéticas en células procariotas o eucariotas in vitro. No se observó un efecto clastogénico significativo en linfocitos periféricos humanos cultivados in vitro o en la prueba de micronúcleos de ratón.
No se observó evidencia de deterioro de la fertilidad en ratas macho y hembra en dosis subcutáneas de hasta 50 mcg/kg (aproximadamente 2 veces la MRHDID en adultos sobre una base de mcg/m²). El peso de la próstata se redujo significativamente con una dosis subcutánea de 50 mcg/kg.
Estudios clínicos
Rinitis no alérgica perenne
Se realizaron tres ensayos aleatorizados, doble ciego, de grupos paralelos, controlados con placebo con vehículo en 1191 sujetos para investigar el uso regular de FLONASE en aerosol nasal de 50 mcg en sujetos con rinitis no alérgica perenne. Estos ensayos evaluaron las puntuaciones de síntomas nasales totales (TNSS) calificadas por el sujeto que incluyeron obstrucción nasal, goteo posnasal, rinorrea en sujetos tratados durante 28 días de terapia doble ciego y en 1 de los 3 ensayos durante 6 meses de tratamiento abierto. Dos de estos ensayos demostraron que los sujetos tratados con el aerosol nasal FLONASE (100 mcg dos veces al día) exhibieron disminuciones estadísticamente significativas en el TNSS en comparación con los sujetos tratados con el vehículo.
Uso en poblaciones específicas
El embarazo
Efectos teratogénicos
Embarazo Categoría C. No existen ensayos adecuados y bien controlados con el aerosol nasal FLONASE en mujeres embarazadas. Se ha demostrado que los corticosteroides son teratogénicos en animales de laboratorio cuando se administran sistémicamente en dosis relativamente bajas. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, el aerosol nasal FLONASE debe usarse durante el embarazo solo si el beneficio potencial justifica el riesgo potencial para el feto. Se debe recomendar a las mujeres que se comuniquen con sus médicos si quedan embarazadas mientras toman FLONASE en aerosol nasal.
Ratones y ratas en dosis de propionato de fluticasona de aproximadamente 1 y 4 veces, respectivamente, la dosis intranasal diaria máxima recomendada en humanos (MRHDID) para adultos (sobre una base de mg/m² en dosis subcutáneas maternas de 45 y 100 mcg/kg/día, respectivamente) mostró toxicidad fetal característica de los compuestos de corticosteroides potentes, incluido el retraso del crecimiento embrionario, el onfalocele, el paladar hendido y la osificación craneal retardada. No se observó teratogenicidad en ratas con dosis de hasta 3 veces la MRHDID (sobre una base de mg/m² en dosis de inhalación materna de hasta 68,7 mcg/kg/día).
En conejos, se observó reducción de peso fetal y paladar hendido con una dosis de propionato de fluticasona de aproximadamente 0,3 veces la MRHDID para adultos (sobre una base de mg/m² con una dosis subcutánea materna de 4 mcg/kg/día). Sin embargo, no se informaron efectos teratogénicos con dosis de propionato de fluticasona de hasta aproximadamente 20 veces la MRHDID para adultos (sobre una base de mg/m² en una dosis oral materna de hasta 300 mcg/kg/día). No se detectó propionato de fluticasona en el plasma en este estudio, lo que concuerda con la baja biodisponibilidad establecida después de la administración oral [ver FARMACOLOGÍA CLÍNICA ].
El propionato de fluticasona atravesó la placenta tras la administración subcutánea a ratones y ratas y la administración oral a conejos.
La experiencia con los corticosteroides orales desde su introducción en dosis farmacológicas, a diferencia de las fisiológicas, sugiere que los roedores son más propensos a los efectos teratogénicos de los corticosteroides que los humanos. Además, debido a que hay un aumento natural en la producción de corticosteroides durante el embarazo, la mayoría de las mujeres requerirán una dosis más baja de corticosteroides exógenos y muchas no necesitarán tratamiento con corticosteroides durante el embarazo.
Efectos no teratogénicos
El hipoadrenalismo puede ocurrir en bebés nacidos de madres que reciben corticosteroides durante el embarazo. Dichos bebés deben ser monitoreados cuidadosamente.
Madres lactantes
No se sabe si el propionato de fluticasona se excreta en la leche materna humana. Sin embargo, se han detectado otros corticosteroides en la leche humana. La administración subcutánea a ratas lactantes de propionato de fluticasona tritiado en una dosis de aproximadamente 0,4 veces la MRHDID para adultos en mg/m² resultó en una radioactividad medible en la leche.
Debido a que no existen datos de ensayos controlados sobre el uso intranasal de FLONASE en aerosol nasal de 50 mcg por parte de madres lactantes, se debe tener precaución cuando se administre FLONASE en aerosol nasal de 50 mcg a mujeres lactantes.
Uso pediátrico
Se ha establecido la seguridad y eficacia del aerosol nasal FLONASE en niños a partir de los 4 años [ver REACCIONES ADVERSAS , FARMACOLOGÍA CLÍNICA ].Seiscientos cincuenta (650) sujetos de 4 a 11 años y 440 sujetos de 12 a 17 años fueron estudiados en ensayos clínicos en EE. UU. con aerosol nasal de propionato de fluticasona. No se ha establecido la seguridad y eficacia de FLONASE Aerosol nasal de 50 mcg en niños menores de 4 años.
Efectos sobre el crecimiento
Los ensayos clínicos controlados han demostrado que los corticosteroides intranasales pueden causar una reducción en la velocidad de crecimiento cuando se administran a pacientes pediátricos. Este efecto se observó en ausencia de pruebas de laboratorio de supresión del eje hipotálamo-pituitario-suprarrenal (HPA), lo que sugiere que la velocidad de crecimiento es un indicador más sensible de la exposición sistémica a los corticosteroides en pacientes pediátricos que algunas pruebas de uso común de la función del eje HPA. Se desconocen los efectos a largo plazo de esta reducción en la velocidad de crecimiento asociada con los corticosteroides intranasales, incluido el impacto en la estatura adulta final. No se ha estudiado adecuadamente el potencial de "recuperación" del crecimiento después de la interrupción del tratamiento con corticosteroides intranasales. El crecimiento de los pacientes pediátricos que reciben corticosteroides intranasales, incluido el aerosol nasal FLONASE, debe controlarse de forma rutinaria (p. ej., mediante estadiometría). Los posibles efectos sobre el crecimiento del tratamiento prolongado deben sopesarse frente a los beneficios clínicos obtenidos y los riesgos asociados con las terapias alternativas. Para minimizar los efectos sistémicos de los corticosteroides intranasales, incluido el aerosol nasal FLONASE, la dosis de cada paciente debe ajustarse a la dosis más baja que controle efectivamente sus síntomas.
Se realizó un ensayo controlado con placebo de 1 año en 150 sujetos pediátricos (de 3 a 9 años de edad) para evaluar el efecto del aerosol nasal FLONASE (dosis única diaria de 200 mcg) sobre la velocidad de crecimiento. De la población primaria que recibió el aerosol nasal FLONASE (n = 56) y el placebo (n = 52), la estimación puntual de la velocidad de crecimiento con el aerosol nasal FLONASE de 50 mcg fue 0,14 cm/año más baja que el placebo (IC del 95 %: -0,54, 0,27 cm /año). Por lo tanto, no se observó ningún efecto estadísticamente significativo sobre el crecimiento en comparación con el placebo. No se observó evidencia de cambios clínicamente relevantes en la función del eje HPA o la densidad mineral ósea evaluada por excreción de cortisol urinario de 12 horas y absorciometría de rayos X de energía dual, respectivamente.
No se puede descartar la posibilidad de que FLONASE Aerosol nasal de 50 mcg provoque una inhibición del crecimiento en pacientes susceptibles o cuando se administre en dosis superiores a las recomendadas.
Uso geriátrico
Un número limitado de sujetos de 65 años o más (n = 129) o de 75 años o más (n = 11) han sido tratados con FLONASE en aerosol nasal en ensayos clínicos. Si bien el número de sujetos es demasiado pequeño para permitir un análisis separado de la eficacia y la seguridad, las reacciones adversas notificadas en esta población fueron similares a las notificadas por pacientes más jóvenes. En general, la selección de la dosis para un paciente de edad avanzada debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedades concomitantes u otra terapia con medicamentos.
Deterioro hepático
No se han realizado ensayos farmacocinéticos formales con FLONASE en aerosol nasal de 50 mcg en sujetos con insuficiencia hepática. Dado que el propionato de fluticasona se elimina predominantemente por el metabolismo hepático, el deterioro de la función hepática puede conducir a la acumulación de propionato de fluticasona en el plasma. Por lo tanto, los pacientes con enfermedad hepática deben ser monitoreados de cerca.

Insuficiencia renal
No se han realizado ensayos farmacocinéticos formales con FLONASE en aerosol nasal en sujetos con insuficiencia renal.
SOBREDOSIS
La sobredosis crónica puede provocar signos/síntomas de hipercorticismo (ver PRECAUCIONES ). La administración intranasal de 2 mg (10 veces la dosis recomendada) de propionato de fluticasona dos veces al día durante 7 días en voluntarios humanos sanos fue bien tolerada. Se han estudiado dosis orales únicas de hasta 16 mg en voluntarios humanos sin que se hayan informado efectos tóxicos agudos. Las dosis orales repetidas de hasta 80 mg diarios durante 10 días en voluntarios y las dosis orales repetidas de hasta 10 mg diarios durante 14 días en pacientes fueron bien toleradas. Las reacciones adversas fueron de gravedad leve o moderada, y las incidencias fueron similares en los grupos de tratamiento activo y placebo. Es poco probable que se produzca una sobredosis aguda con esta forma de dosificación, ya que 1 frasco de FLONASE (propionato de fluticasona) en aerosol nasal contiene aproximadamente 8 mg de propionato de fluticasona.
Las dosis letales medianas por vía oral y subcutánea en ratones y ratas fueron > 1000 mg/kg (> 20 000 y > 41 000 veces, respectivamente, la dosis intranasal diaria máxima recomendada en adultos y > 10 000 y > 20 000 veces, respectivamente, la dosis intranasal diaria máxima recomendada). dosis en niños sobre una base de mg/m2).
CONTRAINDICACIONES
El aerosol nasal FLONASE (propionato de fluticasona) está contraindicado en pacientes con hipersensibilidad a cualquiera de sus ingredientes.
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
El propionato de fluticasona es un corticosteroide trifluorado sintético con actividad antiinflamatoria. Se ha demostrado in vitro que el propionato de fluticasona muestra una afinidad de unión por el receptor de glucocorticoides humano que es 18 veces mayor que la de la dexametasona, casi el doble que la del monopropionato de beclometasona-17 (BMP), el metabolito activo del dipropionato de beclometasona, y más de 3 veces mayor que la de la dexametasona. de budesonida. Los datos del ensayo vasoconstrictor de McKenzie en el hombre son consistentes con estos resultados. Se desconoce el significado clínico de estos hallazgos.
Se desconoce el mecanismo preciso a través del cual el propionato de fluticasona afecta los síntomas de la rinitis. Se ha demostrado que los corticosteroides tienen una amplia gama de efectos sobre múltiples tipos de células (p. ej., mastocitos, eosinófilos, neutrófilos, macrófagos, linfocitos) y mediadores (p. ej., histamina, eicosanoides, leucotrienos, citocinas) implicados en la inflamación. En 7 ensayos en adultos, el aerosol nasal FLONASE redujo los eosinófilos de la mucosa nasal en el 66 % de los pacientes (35 % para el placebo) y los basófilos en el 39 % de los pacientes (28 % para el placebo). Se desconoce la relación directa de estos hallazgos con el alivio de los síntomas a largo plazo.
Farmacodinámica
Efecto del eje HPA
Se evaluaron los efectos sistémicos potenciales de FLONASE Aerosol nasal de 50 mcg en el eje HPA. El aerosol nasal FLONASE de 50 mcg administrado como 200 mcg una vez al día o 400 mcg dos veces al día se comparó con un placebo o prednisona oral de 7,5 o 15 mg administrados por la mañana. El aerosol nasal FLONASE en cualquiera de las dosis durante 4 semanas no afectó la respuesta suprarrenal a la estimulación con cosintropina durante 6 horas, mientras que ambas dosis de prednisona oral redujeron significativamente la respuesta a la cosintropina.
Electrofisiología cardíaca
No se ha realizado un estudio diseñado específicamente para evaluar el efecto de FLONASE en el intervalo QT.
Farmacocinética
La actividad de FLONASE Aerosol nasal de 50 mcg se debe al fármaco original, propionato de fluticasona. Debido a la baja biodisponibilidad por vía intranasal, la mayoría de los datos farmacocinéticos se obtuvieron por otras vías de administración.
Absorción
Los cálculos indirectos indican que el propionato de fluticasona administrado por vía intranasal tiene una biodisponibilidad absoluta que promedia menos del 2 %. Los ensayos que utilizan dosis orales de fármacos etiquetados y no etiquetados han demostrado que la biodisponibilidad sistémica oral del propionato de fluticasona es insignificante (
Distribución
Luego de la administración intravenosa, la fase de disposición inicial para el propionato de fluticasona fue rápida y consistente con su alta solubilidad en lípidos y unión a tejidos. El volumen de distribución promedió 4,2 L/kg.
El porcentaje de propionato de fluticasona unido a proteínas plasmáticas humanas promedió el 99 %. El propionato de fluticasona se une débil y reversiblemente a los eritrocitos y no se une significativamente a la transcortina humana.
Eliminación
Después de la dosificación intravenosa, el propionato de fluticasona mostró una cinética poliexponencial y tuvo una vida media de eliminación terminal de aproximadamente 7,8 horas. El aclaramiento sanguíneo total del propionato de fluticasona es elevado (promedio: 1.093 ml/min), y el aclaramiento renal representa menos del 0,02 % del total.
Metabolismo: El único metabolito circulante detectado en el hombre es el derivado del ácido 17β-carboxílico del propionato de fluticasona, que se forma a través de la vía CYP3A4. Este metabolito tenía menos afinidad (aproximadamente 1/2000) que el fármaco original por el receptor de glucocorticoides del citosol de pulmón humano in vitro y una actividad farmacológica insignificante en estudios con animales. Otros metabolitos detectados in vitro utilizando células de hepatoma humano cultivadas no se han detectado en el hombre.
Excreción: Menos del 5% de una dosis oral radiomarcada se excretó en la orina como metabolitos, y el resto se excretó en las heces como fármaco original y metabolitos.
Poblaciones Especiales
El aerosol nasal de propionato de fluticasona no se estudió en ninguna población especial y no se han obtenido datos farmacocinéticos específicos de género.
Interacciones con la drogas
Inhibidores del Citocromo P450 3A4: Ritonavir: El propionato de fluticasona es un sustrato de CYP3A4. No se recomienda la coadministración de propionato de fluticasona y el inhibidor potente de CYP3A4, ritonavir, en base a un ensayo cruzado de interacciones farmacológicas de dosis múltiples en 18 sujetos sanos. El aerosol nasal acuoso de propionato de fluticasona (200 mcg una vez al día) se coadministró durante 7 días con ritonavir (100 mg dos veces al día). Las concentraciones plasmáticas de propionato de fluticasona después del aerosol nasal acuoso de propionato de fluticasona solo fueron indetectables (
Ketoconazol: La coadministración de propionato de fluticasona inhalado por vía oral (1000 mcg) y ketoconazol (200 mg una vez al día) resultó en un aumento de 1,9 veces en la exposición de propionato de fluticasona en plasma y una disminución del 45 % en el AUC de cortisol en plasma, pero no tuvo ningún efecto sobre la excreción urinaria de cortisol.
Eritromicina: En un estudio de interacción farmacológica de dosis múltiples, la coadministración de propionato de fluticasona inhalado por vía oral (500 mcg dos veces al día) y eritromicina (333 mg 3 veces al día) no afectó la farmacocinética del propionato de fluticasona.
INFORMACIÓN DEL PACIENTE
FLONASE® [flow'naz] (propionato de fluticasona) Aerosol nasal, 50 mcg
Lea la información para el paciente que viene con el aerosol nasal FLONASE antes de comenzar a usarlo y cada vez que renueve su receta. Es posible que haya nueva información. Esta información del paciente no reemplaza la conversación con su proveedor de atención médica sobre su condición médica o tratamiento.
¿Qué es el aerosol nasal FLONASE?
FLONASE Nasal Spray 50mcg es un medicamento recetado que se usa para tratar los síntomas nasales no alérgicos, como secreción nasal, congestión nasal, estornudos y picazón nasal en adultos y niños a partir de los 4 años.
No se sabe si FLONASE Aerosol nasal de 50 mcg es seguro y efectivo en niños menores de 4 años.
¿Quién no debe usar FLONASE Aerosol Nasal 50mcg?
No use el aerosol nasal FLONASE de 50 mcg si es alérgico al propionato de fluticasona o a cualquiera de los ingredientes del aerosol nasal FLONASE. Consulte "¿Cuáles son los ingredientes del aerosol nasal FLONASE de 50 mcg?" a continuación para obtener una lista completa de ingredientes.
¿Qué debo decirle a mi proveedor de atención médica antes de usar FLONASE, aerosol nasal de 50 mcg?
Informe a su proveedor de atención médica sobre todas sus afecciones de salud, incluso si usted:
- tiene o ha tenido llagas nasales, cirugía nasal o lesión nasal.
- tiene problemas en los ojos, como cataratas o glaucoma.
- tiene un problema del sistema inmunológico.
- es alérgico a alguno de los ingredientes del aerosol nasal FLONASE, a cualquier otro medicamento o producto alimenticio. Ver “¿Cuáles son los ingredientes del aerosol nasal FLONASE?” a continuación para obtener una lista completa de ingredientes.
- tiene cualquier tipo de infección viral, bacteriana o fúngica.
- están expuestos a la varicela o al sarampión.
- tiene otras condiciones médicas.
- está embarazada o planea quedar embarazada. No se sabe si el aerosol nasal FLONASE puede dañar a su bebé por nacer.
- están amamantando o planean amamantar. No se sabe si FLONASE Aerosol Nasal 50 mcg pasa a la leche materna y si le puede hacer daño a su bebé.
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluyendo medicamentos recetados y de venta libre, vitaminas y suplementos a base de hierbas. El aerosol nasal FLONASE y otros medicamentos pueden interactuar entre sí. Esto puede causar efectos secundarios graves. Especialmente, informe a su proveedor de atención médica si toma medicamentos antimicóticos o anti-VIH.
Conozca los medicamentos que toma. Mantenga una lista de ellos para mostrársela a su proveedor de atención médica y farmacéutico cuando obtenga un nuevo medicamento.
¿Cómo debo usar el aerosol nasal FLONASE?
Lea las instrucciones paso a paso para usar el aerosol nasal FLONASE al final de esta información para el paciente.
- El aerosol nasal FLONASE es para uso exclusivo en la nariz. No lo rocíe en sus ojos o boca.
- Los niños deben usar el aerosol nasal FLONASE con la ayuda de un adulto, según las instrucciones del proveedor de atención médica del niño.
- Use el aerosol nasal FLONASE de 50 mcg exactamente como le indique su proveedor de atención médica. No use el aerosol nasal FLONASE con más frecuencia de lo recetado.
- El aerosol nasal FLONASE puede tomar varios días de uso regular para que los síntomas de la rinitis mejoren. Si sus síntomas no mejoran o empeoran, llame a su proveedor de atención médica.
- Obtendrá los mejores resultados si continúa usando el aerosol nasal FLONASE regularmente todos los días sin omitir una dosis. Después de que comience a sentirse mejor, su proveedor de atención médica puede disminuir su dosis. No haga deje de usar FLONASE Aerosol nasal de 50 mcg a menos que su proveedor de atención médica se lo indique.
¿Cuáles son los posibles efectos secundarios de FLONASE Aerosol Nasal 50mcg?
El aerosol nasal FLONASE de 50 mcg puede causar efectos secundarios graves, que incluyen:
- problemas de nariz Los problemas de la nariz pueden incluir:
- sangra la nariz
- llagas (úlceras) en la nariz.
- cierta infección fúngica en la nariz, la boca y/o la garganta (aftas).
- orificio en el cartílago de la nariz (perforación del tabique nasal). Los síntomas de la perforación del tabique nasal pueden incluir:
- costras en la nariz
- hemorragia nasal
- nariz que moquea
- silbido al respirar
- cicatrización lenta de heridas. No debe usar el aerosol nasal FLONASE hasta que su nariz haya sanado si tiene una llaga en la nariz, si se sometió a una cirugía en la nariz o si se lesionó la nariz.
- problemas oculares, incluyendo glaucoma y cataratas. Debe someterse a exámenes oculares regulares mientras usa el aerosol nasal FLONASE.
- reacciones alérgicas graves. Llame a su proveedor de atención médica o busque atención médica de emergencia si presenta alguno de los siguientes signos de una reacción alérgica grave:
- sarpullido
- urticaria
- hinchazón de la cara, la boca y la lengua
- problemas respiratorios
- sistema inmunitario debilitado y mayor probabilidad de contraer infecciones (inmunosupresión). Tomar medicamentos que debilitan su sistema inmunológico lo hace más propenso a contraer infecciones y puede empeorar ciertas infecciones. Estas infecciones pueden incluir tuberculosis (TB), infecciones oculares por herpes simple e infecciones causadas por hongos, bacterias, virus y parásitos. Evite el contacto con personas que tengan una enfermedad contagiosa como varicela o sarampión mientras usa FLONASE Aerosol Nasal. Si entra en contacto con alguien que tiene varicela o sarampión, llame a su proveedor de atención médica de inmediato. Los síntomas de una infección pueden incluir:
- fiebre
- sensación de cansancio
- dolor
- náuseas
- dolores
- vómitos
- escalofríos
- disminución de los niveles de hormonas esteroides (insuficiencia suprarrenal). La insuficiencia suprarrenal ocurre cuando las glándulas suprarrenales no producen suficientes hormonas esteroides. Esto puede suceder cuando deja de tomar medicamentos corticosteroides orales (como la prednisona) y comienza a tomar medicamentos que contienen un esteroide inhalado (como el aerosol nasal FLONASE). Los síntomas de insuficiencia suprarrenal pueden incluir:
- sensación de cansancio
- falta de energía
- debilidad
- náuseas y vómitos
- presión arterial baja
- crecimiento lento en los niños. El crecimiento de un niño debe controlarse con frecuencia.
Los efectos secundarios más comunes de FLONASE Nasal Spray 50mcg incluyen:
- dolor de cabeza
- náuseas y vómitos
- dolor de garganta
- dificultad para respirar
- hemorragia nasal
- tos
- ardor o picazón en la nariz
Informe a su proveedor de atención médica sobre cualquier efecto secundario que le moleste o que no desaparezca.
Estos no son todos los efectos secundarios de FLONASE Aerosol Nasal. Consulte a su proveedor de atención médica o farmacéutico para obtener más información.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
¿Cómo conservo FLONASE Aerosol Nasal 50mcg?
- Almacene FLONASE entre 39 °F y 86 °F (4 °C y 30 °C).
Mantenga el aerosol nasal FLONASE de 50 mcg y todos los medicamentos fuera del alcance de los niños.
Información general sobre el uso seguro y eficaz de FLONASE Aerosol Nasal.
A veces, los medicamentos se recetan para fines no mencionados en el folleto de información para el paciente. No use el aerosol nasal FLONASE para una condición para la cual no fue recetado. No le dé su Aerosol Nasal FLONASE a otras personas, incluso si tienen la misma condición que usted tiene. Puede que les haga daño.
Este folleto de información para el paciente resume la información más importante sobre el aerosol nasal FLONASE. Si desea obtener más información, hable con su proveedor de atención médica. Puede pedirle a su farmacéutico o proveedor de atención médica información sobre el aerosol nasal FLONASE que fue escrito para profesionales de la salud.
Para obtener más información sobre el aerosol nasal FLONASE, llame al 1-888-825-5249.
¿Cuáles son los ingredientes de FLONASE Spray Nasal 50mcg?
Principio activo: propionato de fluticasona.
Ingredientes inactivos: celulosa microcristalina, carboximetilcelulosa sódica, dextrosa, cloruro de benzalconio al 0,02 % p/p, polisorbato 80 y alcohol feniletílico al 0,25 % p/p.
Instrucciones de uso
FLONASE® [flow'naz] (propionato de fluticasona) Aerosol nasal, 50 mcg
FLONASE Aerosol nasal 50 mcg es solo para uso en la nariz.
Lea esta información antes de comenzar a usar su aerosol nasal FLONASE.
Partes de su aerosol nasal FLONASE (Ver Figura A)
Figura A 
Su aerosol nasal FLONASE de 50 mcg debe prepararse antes de usarlo por primera vez y cuando no lo haya usado durante una semana o más.
Cómo preparar su spray nasal FLONASE
- Agite la botella suavemente y luego retire la cubierta antipolvo (vea la Figura B).
Figura B 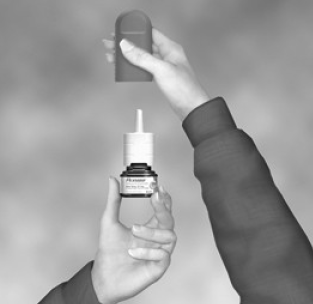
- Sostenga el frasco como se muestra (vea la figura C) con el aplicador nasal apuntando hacia afuera y con los dedos índice y medio a ambos lados del aplicador nasal y el pulgar debajo del frasco.
- Presione hacia abajo y suelte 6 veces hasta que aparezca un rocío fino (vea la figura C). La bomba ya está lista para su uso.
Figura C 
Uso de su aerosol nasal FLONASE:
Paso 1 . Suénate la nariz para limpiar tus fosas nasales.
Paso 2 . Cierra 1 fosa nasal. Incline la cabeza ligeramente hacia adelante y, manteniendo la botella en posición vertical, inserte con cuidado el aplicador nasal en la otra fosa nasal (consulte la Figura D).
Figura D 
Paso 3 Comience a inhalar por la nariz y, mientras inhala, presione firme y rápidamente el aplicador una vez para liberar el aerosol. Para obtener una dosis completa, use su dedo índice y medio para rociar mientras sostiene la base de la botella con su pulgar. Evite rociar en sus ojos. Inhale suavemente por la fosa nasal (vea la figura E).
Figura E 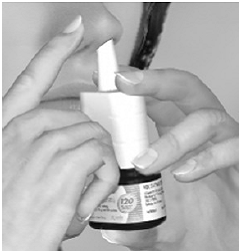
Paso 4 . Exhala por la boca.
Paso 5 . Si se requiere una segunda aplicación en esa fosa nasal, repita los pasos 2 a 4.
Paso 6 . Repita los pasos 2 a 5 en la otra fosa nasal.
Paso 7 . Limpie el aplicador nasal con un pañuelo limpio y vuelva a colocar la cubierta antipolvo (vea la figura F).
Figura F 
No use esta botella por más de la cantidad indicada en la etiqueta, aunque la botella no esté completamente vacía. Antes de tirar la botella, debe hablar con su proveedor de atención médica para ver si necesita una recarga. No tome dosis adicionales ni deje de tomar FLONASE Aerosol nasal de 50 mcg sin hablar con su proveedor de atención médica.
Limpieza de su spray nasal FLONASE:
Su aerosol nasal debe limpiarse al menos 1 vez por semana.
1. Retire la cubierta antipolvo y tire suavemente hacia arriba para liberar el aplicador nasal.
2. Lave el aplicador y la cubierta antipolvo con agua tibia del grifo. Deje secar a temperatura ambiente.
3. Vuelva a colocar el aplicador y la cubierta contra el polvo en la botella.
4. Si el aplicador nasal se obstruye, puede retirarlo y dejarlo en remojo en agua tibia. Enjuague el aplicador nasal con agua fría del grifo. Seque el aplicador nasal y vuelva a colocarlo en la botella. No intente desbloquear el aplicador nasal insertando un alfiler u otro objeto afilado.
Almacenamiento de su aerosol nasal FLONASE:
- Almacene el aerosol nasal FLONASE de 50 mcg entre 4 °C y 30 °C (39 °F y 86 °F).
- No use su aerosol nasal FLONASE después de la fecha que se muestra como "EXP" en la etiqueta o caja.
