Tratamiento de la diabetes: Glucophage 500mg, 850mg, 1000mg Metformin Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Glucophage y cómo se usa?
Glucophage es un medicamento recetado que se usa para mejorar el control del azúcar en la sangre en adultos con diabetes mellitus tipo 2. Glucophage se puede usar solo o con otros medicamentos.
Glucophage 850 mg pertenece a una clase de medicamentos llamados antidiabéticos.
No se sabe si Glucophage es seguro y eficaz en niños menores de 10 años.
¿Cuáles son los posibles efectos secundarios de Glucophage?
- dolor muscular inusual,
- siento frio,
- dificultad para respirar,
- sentirse mareado o aturdido,
- cansancio,
- debilidad,
- dolor de estómago,
- vómitos y
- frecuencia cardíaca lenta o irregular
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Glucophage incluyen:
- baja azúcar en la sangre,
- náuseas,
- malestar estomacal y
- Diarrea
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Glucophage. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
ADVERTENCIA
ACIDOSIS LÁCTICA
Los casos posteriores a la comercialización de acidosis láctica asociada con metformina han resultado en muerte, hipotermia, hipotensión y bradiarritmias resistentes. El inicio de la acidosis láctica asociada a metformina suele ser sutil, acompañado únicamente de síntomas inespecíficos como malestar general, mialgias, dificultad respiratoria, somnolencia y dolor abdominal. La acidosis láctica asociada a metformina se caracterizó por niveles elevados de lactato en sangre (> 5 mmol/litro), acidosis con desequilibrio aniónico (sin evidencia de cetonuria o cetonemia), un aumento de la relación lactato/piruvato; y niveles plasmáticos de metformina generalmente >5 mcg/mL [ver ADVERTENCIAS Y PRECAUCIONES].
Los factores de riesgo de acidosis láctica asociada a metformina incluyen insuficiencia renal, uso concomitante de ciertos fármacos (p. ej., inhibidores de la anhidrasa carbónica como topiramato), edad de 65 años o más, estudio radiológico con contraste, cirugía y otros procedimientos, estados hipóxicos (p. ej., , insuficiencia cardíaca congestiva aguda), consumo excesivo de alcohol e insuficiencia hepática.
Se proporcionan los pasos para reducir el riesgo y controlar la acidosis láctica asociada a la metformina en estos grupos de alto riesgo [ver DOSIS Y ADMINISTRACIÓN, CONTRAINDICACIONES, ADVERTENCIAS Y PRECAUCIONES].
Si se sospecha acidosis láctica asociada a metformina, suspenda inmediatamente GLUCOPHAGE o GLUCOPHAGE XR e instituya medidas generales de apoyo en un entorno hospitalario. Se recomienda hemodiálisis inmediata [ver ADVERTENCIAS Y PRECAUCIONES].
DESCRIPCIÓN
GLUCOPHAGE/GLUCOPHAGE 500mg XR contiene el agente antihiperglucémico metformina, que es una biguanida, en forma de monoclorhidrato. El nombre químico del clorhidrato de metformina es clorhidrato de diamida de N,N-dimetilimidodicarbonimidica. La fórmula estructural es la siguiente:
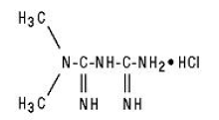
El clorhidrato de metformina es un compuesto cristalino de color blanco a blanquecino con una fórmula molecular de C4H11N5 • HCl y un peso molecular de 165,63. Es fácilmente soluble en agua y prácticamente insoluble en acetona, éter y cloroformo. El pKa de la metformina es 12,4. El pH de una solución acuosa al 1% de clorhidrato de metformina es 6,68.
Los comprimidos de GLUCOPHAGE contienen 500 mg, 850 mg o 1000 mg de clorhidrato de metformina, lo que equivale a 389,93 mg, 662,88 mg y 779,86 mg de metformina base, respectivamente. Cada tableta contiene los ingredientes inactivos povidona y estearato de magnesio. Además, el recubrimiento de los comprimidos de 500 mg y 850 mg contiene hipromelosa y el recubrimiento del comprimido de 1000 mg contiene hipromelosa y polietilenglicol.
GLUCOPHAGE 500 mg XR contiene 500 mg o 750 mg de clorhidrato de metformina, lo que equivale a 389,93 mg, 584,90 mg de base de metformina, respectivamente.
Las tabletas de GLUCOPHAGE XR de 500 mg contienen los ingredientes inactivos hipromelosa, celulosa microcristalina, carboximetilcelulosa de sodio y estearato de magnesio.
Las tabletas GLUCOPHAGE 850mg XR 750 mg contienen los ingredientes inactivos hipromelosa, carboximetilcelulosa sódica, estearato de magnesio y pigmento rojo de óxido de hierro.
INDICACIONES
GLUCOPHAGE 850 mg está indicado como complemento de la dieta y el ejercicio para mejorar el control glucémico en adultos y pacientes pediátricos de 10 años de edad y mayores con diabetes mellitus tipo 2.
GLUCOPHAGE XR está indicado como complemento de la dieta y el ejercicio para mejorar el control glucémico en adultos con diabetes mellitus tipo 2.
DOSIFICACIÓN Y ADMINISTRACIÓN
Dosis para adultos
glucófago
- La dosis inicial recomendada de GLUCOPHAGE 850 mg es de 500 mg por vía oral dos veces al día o de 850 mg una vez al día, administrados con las comidas.
- Aumente la dosis en incrementos de 500 mg por semana o 850 mg cada 2 semanas según el control glucémico y la tolerabilidad, hasta una dosis máxima de 2550 mg por día, administrada en dosis divididas.
- Las dosis superiores a 2000 mg pueden tolerarse mejor administradas 3 veces al día con las comidas.
Glucofago XR
- Trague las tabletas de GLUCOPHAGE XR enteras y nunca las triture, corte ni mastique.
- La dosis inicial recomendada de GLUCOPHAGE XR es de 500 mg por vía oral una vez al día con la cena.
- Aumente la dosis en incrementos de 500 mg por semana según el control glucémico y la tolerabilidad, hasta un máximo de 2000 mg una vez al día con la cena.
- Si no se logra el control glucémico con GLUCOPHAGE XR 2000 mg una vez al día, considere una prueba de GLUCOPHAGE 850 mg XR 1000 mg dos veces al día. Si se requieren dosis más altas, cambie a GLUCOPHAGE 500 mg en dosis diarias totales de hasta 2550 mg administrados en dosis diarias divididas, como se describe anteriormente.
- Los pacientes que reciben GLUCOPHAGE 1000 mg pueden cambiar a GLUCOPHAGE 850 mg XR una vez al día con la misma dosis diaria total, hasta 2000 mg una vez al día.
Dosis pediátrica de Glucophage
- La dosis inicial recomendada de GLUCOPHAGE 850 mg para pacientes pediátricos de 10 años de edad y mayores es de 500 mg por vía oral dos veces al día, administrada con las comidas.
- Aumente la dosis en incrementos de 500 mg semanales sobre la base del control glucémico y la tolerabilidad, hasta un máximo de 2000 mg por día, administrados en dosis divididas dos veces al día.
Recomendaciones de uso en insuficiencia renal
- Evalúe la función renal antes de iniciar GLUCOPHAGE/GLUCOPHAGE 500 mg XR y periódicamente a partir de entonces.
- GLUCOPHAGE/GLUCOPHAGE 500 mg XR está contraindicado en pacientes con una tasa de filtración glomerular estimada (TFGe) inferior a 30 ml/minuto/1,73 m2.
- No se recomienda el inicio de GLUCOPHAGE/GLUCOPHAGE 850 mg XR en pacientes con una eGFR entre 30 y 45 ml/minuto/1,73 m2.
- En pacientes que toman GLUCOPHAGE/GLUCOPHAGE 1000 mg XR cuyo eGFR luego cae por debajo de 45 mL/min/1.73 m2, evalúe el beneficio-riesgo de continuar con la terapia.
- Suspender GLUCOPHAGE/GLUCOPHAGE 1000 mg XR si la TFGe del paciente luego cae por debajo de 30 ml/minuto/1,73 m2 [ver ADVERTENCIAS Y PRECAUCIONES ].
Interrupción de los procedimientos de obtención de imágenes con contraste yodado
Suspender GLUCOPHAGE/GLUCOPHAGE XR en el momento o antes de un procedimiento de obtención de imágenes con contraste yodado en pacientes con una TFGe entre 30 y 60 ml/min/1,73 m2; en pacientes con antecedentes de enfermedad hepática, alcoholismo o insuficiencia cardíaca; o en pacientes a los que se les administrará contraste yodado intraarterial. Vuelva a evaluar la eGFR 48 horas después del procedimiento de imagen; reinicie GLUCOPHAGE/GLUCOPHAGE XR si la función renal es estable.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
GLUCOPHAGE 850 mg está disponible como:
- Comprimidos: redondos de 500 mg, de color blanco a blanquecino, recubiertos con película grabados con "BMS 6060" alrededor de la periferia de un lado y "500" grabados en la cara del otro lado.
- Comprimidos: redondos de 850 mg, de color blanco a blanquecino, recubiertos con película grabados con "BMS 6070" alrededor de la periferia de un lado y "850" grabados en la cara del otro lado.
- Comprimidos: 1000 mg blancos, ovalados, biconvexos, recubiertos con película con "BMS 6071" grabado en un lado y "1000" grabado en el lado opuesto y con una línea de bisección en ambos lados.
GLUCOPHAGE XR está disponible como:
- Tabletas de liberación prolongada: 500 mg de color blanco a blanquecino, en forma de cápsula, biconvexas, con "BMS 6063" grabado en un lado y "500" grabado en la cara del otro lado.
- Tabletas de liberación prolongada: 750 mg de color rojo pálido y pueden tener una apariencia moteada, en forma de cápsula, biconvexa, con "BMS 6064" grabado en un lado y "750" grabado en el otro lado.
Almacenamiento y manipulación
Almacenamiento
Almacenar a 20°–25°C (68°–77°F); excursiones permitidas a 15°–30°C (59°–86°F). [Consulte Temperatura ambiente controlada por la USP.]
Dispensar en recipientes resistentes a la luz.
Distribuido por: Bristol-Myers Squibb Company Princeton, NJ 08543 EE. UU. Revisado: mayo de 2018.
EFECTOS SECUNDARIOS
Las siguientes reacciones adversas también se analizan en otra parte de la etiqueta:
- Acidosis láctica [ver CUADRO DE ADVERTENCIA y ADVERTENCIAS Y PRECAUCIONES ]
- Deficiencia de vitamina B12 [ver ADVERTENCIAS Y PRECAUCIONES ]
- Hipoglucemia [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en estudios clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy diversas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica.
glucófago
En un ensayo clínico de EE. UU. de GLUCOPHAGE 850 mg en pacientes con diabetes mellitus tipo 2, un total de 141 pacientes recibieron GLUCOPHAGE 1000 mg hasta 2550 mg por día. Las reacciones adversas notificadas en más del 5 % de los pacientes tratados con GLUCOPHAGE 500 mg y que fueron más frecuentes que en los pacientes tratados con placebo se enumeran en la Tabla 1.
La diarrea condujo a la suspensión de GLUCOPHAGE 500 mg en el 6 % de los pacientes. Además, se informaron las siguientes reacciones adversas en ≥1 % a ≤5 % de los pacientes tratados con GLUCOPHAGE y se informaron con más frecuencia con GLUCOPHAGE que con el placebo: heces anormales, hipoglucemia, mialgia, mareo, disnea, trastorno de las uñas, erupción cutánea, aumento de la sudoración, sabor molestias en el pecho, escalofríos, síndrome gripal, sofocos, palpitaciones.
En ensayos clínicos de 500 mg de GLUCOPHAGE de 29 semanas de duración, se observó una disminución a niveles por debajo de lo normal de los niveles séricos de vitamina B12 previamente normales en aproximadamente el 7 % de los pacientes.
Pacientes pediátricos
En ensayos clínicos con GLUCOPHAGE en pacientes pediátricos con diabetes mellitus tipo 2, el perfil de reacciones adversas fue similar al observado en adultos.
Glucopagina XR
En ensayos controlados con placebo, se administró GLUCOPHAGE 1000 mg XR a 781 pacientes. Las reacciones adversas informadas en más del 5 % de los pacientes con GLUCOPHAGE 850 mg XR, y que fueron más comunes en los pacientes tratados con GLUCOPHAGE XR que con el placebo, se enumeran en la Tabla 2.
La diarrea condujo a la suspensión de GLUCOPHAGE XR en el 0,6 % de los pacientes. Además, se informaron las siguientes reacciones adversas en ≥1,0 % a ≤5,0 % de los pacientes con GLUCOPHAGE XR y se informaron con más frecuencia con GLUCOPHAGE XR que con placebo: dolor abdominal, estreñimiento, distensión abdominal, dispepsia/acidez estomacal, flatulencia, mareos, dolor de cabeza, infección respiratoria, alteración del gusto.
Experiencia posterior a la comercialización
Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación de metformina. Debido a que estas reacciones son informadas voluntariamente por una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Se han informado lesiones hepáticas colestásicas, hepatocelulares y hepatocelulares mixtas con el uso posterior a la comercialización de metformina.
INTERACCIONES CON LA DROGAS
La Tabla 3 presenta interacciones farmacológicas clínicamente significativas con GLUCOPHAGE/GLUCOPHAGE XR.
ADVERTENCIAS
Incluido como parte de la "PRECAUCIONES" Sección
PRECAUCIONES
Acidosis láctica
Ha habido casos posteriores a la comercialización de acidosis láctica asociada a metformina, incluidos casos mortales. Estos casos tuvieron un inicio sutil y se acompañaron de síntomas inespecíficos como malestar general, mialgias, dolor abdominal, dificultad respiratoria o aumento de la somnolencia; sin embargo, se han producido hipotensión y bradiarritmias resistentes con acidosis grave. La acidosis láctica asociada a metformina se caracterizó por concentraciones elevadas de lactato en sangre (>5 mmol/L), acidosis con desequilibrio aniónico (sin evidencia de cetonuria o cetonemia) y un aumento de la relación lactato:piruvato; Los niveles plasmáticos de metformina fueron generalmente >5 mcg/mL. La metformina disminuye la captación hepática de lactato aumentando los niveles de lactato en sangre, lo que puede aumentar el riesgo de acidosis láctica, especialmente en pacientes en riesgo.
Si se sospecha acidosis láctica asociada con metformina, se deben instituir medidas generales de apoyo de inmediato en un entorno hospitalario, junto con la suspensión inmediata de GLUCOPHAGE/GLUCOPHAGE 500 mg XR. En pacientes tratados con GLUCOPHAGE/GLUCOPHAGE XR con diagnóstico o fuerte sospecha de acidosis láctica, se recomienda hemodiálisis inmediata para corregir la acidosis y eliminar la metformina acumulada (el clorhidrato de metformina es dializable con un aclaramiento de hasta 170 ml/min en buenas condiciones hemodinámicas). La hemodiálisis a menudo ha resultado en la reversión de los síntomas y la recuperación.
Instruya a los pacientes y sus familias sobre los síntomas de la acidosis láctica y, si estos síntomas ocurren, indíqueles que descontinúen GLUCOPHAGE/GLUCOPHAGE 1000 mg XR e informe estos síntomas a su proveedor de atención médica.
Para cada uno de los factores de riesgo conocidos y posibles de acidosis láctica asociada a metformina, a continuación se proporcionan recomendaciones para reducir el riesgo y controlar la acidosis láctica asociada a metformina:
- Insuficiencia renal: los casos de acidosis láctica asociada con metformina posteriores a la comercialización ocurrieron principalmente en pacientes con insuficiencia renal significativa.
El riesgo de acumulación de metformina y acidosis láctica asociada a metformina aumenta con la gravedad de la insuficiencia renal porque la metformina se excreta sustancialmente por vía renal. Las recomendaciones clínicas basadas en la función renal del paciente incluyen [ver DOSIFICACIÓN Y ADMINISTRACIÓN , FARMACOLOGÍA CLÍNICA ]:
- Antes de iniciar GLUCOPHAGE/GLUCOPHAGE 850mg XR, obtenga una tasa de filtración glomerular estimada (eGFR).
- GLUCOPHAGE/GLUCOPHAGE XR está contraindicado en pacientes con una TFGe inferior a 30 ml/min/1,73 m2 [ver CONTRAINDICACIONES ].
- No se recomienda el inicio de GLUCOPHAGE/GLUCOPHAGE XR en pacientes con eGFR entre 30 y 45 ml/min/1,73 m2.
- Obtenga una eGFR al menos una vez al año en todos los pacientes que toman GLUCOPHAGE/ GLUCOPHAGE 1000 mg XR. En pacientes con riesgo de desarrollar insuficiencia renal (p. ej., ancianos), se debe evaluar la función renal con mayor frecuencia.
- En pacientes que toman GLUCOPHAGE/GLUCOPHAGE 500 mg XR cuya eGFR cae por debajo de 45 ml/min/1,73 m2, evalúe el beneficio y el riesgo de continuar la terapia.
- Interacciones medicamentosas: el uso concomitante de GLUCOPHAGE/GLUCOPHAGE XR con medicamentos específicos puede aumentar el riesgo de acidosis láctica asociada con metformina: aquellos que deterioran la función renal, provocan cambios hemodinámicos significativos, interfieren con el equilibrio ácido-base o aumentan la acumulación de metformina. Considere un control más frecuente de los pacientes.
- 65 años o más: el riesgo de acidosis láctica asociada con la metformina aumenta con la edad del paciente porque los pacientes de edad avanzada tienen una mayor probabilidad de tener insuficiencia hepática, renal o cardíaca que los pacientes más jóvenes. Evaluar la función renal con mayor frecuencia en pacientes de edad avanzada.
- Estudios radiológicos con contraste: la administración de agentes de contraste yodados intravasculares en pacientes tratados con metformina ha provocado una disminución aguda de la función renal y la aparición de acidosis láctica. Suspender GLUCOPHAGE/GLUCOPHAGE XR en el momento o antes de un procedimiento de obtención de imágenes con contraste yodado en pacientes con una TFGe entre 30 y 60 ml/min/1,73 m2; en pacientes con antecedentes de insuficiencia hepática, alcoholismo o insuficiencia cardiaca; o en pacientes a los que se les administrará contraste yodado intraarterial. Vuelva a evaluar la eGFR 48 horas después del procedimiento de imagen y reinicie GLUCOPHAGE/GLUCOPHAGE XR si la función renal es estable.
- Cirugía y otros procedimientos: la retención de alimentos y líquidos durante la cirugía u otros procedimientos puede aumentar el riesgo de hipovolemia, hipotensión e insuficiencia renal. GLUCOPHAGE/GLUCOPHAGE XR debe interrumpirse temporalmente mientras los pacientes tengan una ingesta restringida de alimentos y líquidos.
- Estados hipóxicos: varios de los casos posteriores a la comercialización de acidosis láctica asociada con metformina ocurrieron en el contexto de insuficiencia cardíaca congestiva aguda (particularmente cuando se acompaña de hipoperfusión e hipoxemia). El colapso cardiovascular (choque), el infarto agudo de miocardio, la sepsis y otras condiciones asociadas con la hipoxemia se han asociado con acidosis láctica y pueden causar azotemia prerrenal. Cuando ocurra tal evento, suspenda GLUCOPHAGE/GLUCOPHAGE 1000mg XR.
- Ingesta excesiva de alcohol: el alcohol potencia el efecto de la metformina en el metabolismo del lactato. Se debe advertir a los pacientes sobre el consumo excesivo de alcohol mientras reciben GLUCOPHAGE/GLUCOPHAGE XR.
- Insuficiencia hepática: los pacientes con insuficiencia hepática han desarrollado casos de acidosis láctica asociada a metformina. Esto puede deberse a un aclaramiento de lactato alterado que da como resultado niveles sanguíneos de lactato más altos. Por lo tanto, evite el uso de GLUCOPHAGE/GLUCOPHAGE XR en pacientes con evidencia clínica o de laboratorio de enfermedad hepática.
Deficiencia de vitamina B12
En ensayos clínicos de 1000 mg de GLUCOPHAGE de 29 semanas de duración, se observó una disminución a niveles por debajo de lo normal de los niveles séricos de vitamina B12 previamente normales en aproximadamente el 7 % de los pacientes. Tal disminución, posiblemente debido a la interferencia con la absorción de B12 del complejo B12-factor intrínseco, puede estar asociada con anemia, pero parece ser rápidamente reversible con la interrupción de GLUCOPHAGE o la suplementación con vitamina B12. Ciertas personas (aquellas con una ingesta o absorción inadecuada de vitamina B12 o calcio) parecen estar predispuestas a desarrollar niveles de vitamina B12 por debajo de lo normal. Mida los parámetros hematológicos anualmente y la vitamina B12 en intervalos de 2 a 3 años en pacientes que reciben GLUCOPHAGE/GLUCOPHAGE 500 mg XR y maneje cualquier anormalidad [ver REACCIONES ADVERSAS ].
Hipoglucemia con uso concomitante con insulina e insulina
secretagogos
Se sabe que la insulina y los secretagogos de insulina (p. ej., sulfonilurea) causan hipoglucemia. GLUCOPHAGE/GLUCOPHAGE XR puede aumentar el riesgo de hipoglucemia cuando se combina con insulina y/o un secretagogo de insulina. Por lo tanto, es posible que se requiera una dosis más baja de insulina o secretagogo de insulina para minimizar el riesgo de hipoglucemia cuando se usa en combinación con GLUCOPHAGE/GLUCOPHAGE XR [ver INTERACCIONES CON LA DROGAS ].
Resultados macrovasculares
No se han realizado estudios clínicos que establezcan evidencia concluyente de reducción del riesgo macrovascular con GLUCOPHAGE/GLUCOPHAGE 850 mg XR.
Información de asesoramiento para pacientes
Aconseje al paciente que lea la etiqueta del paciente aprobada por la FDA ( INFORMACIÓN DEL PACIENTE ).
Acidosis láctica
Explicar los riesgos de la acidosis láctica, sus síntomas y las condiciones que predisponen a su desarrollo. Aconseje a los pacientes que descontinúen GLUCOPHAGE/GLUCOPHAGE XR de inmediato y que notifiquen de inmediato a su proveedor de atención médica si presentan hiperventilación, mialgias, malestar general, somnolencia inusual u otros síntomas inespecíficos sin causa aparente. Aconseje a los pacientes contra el consumo excesivo de alcohol e infórmeles sobre la importancia de las pruebas periódicas de la función renal mientras reciben GLUCOPHAGE/GLUCOPHAGE XR. Indique a los pacientes que informen a su médico que están tomando GLUCOPHAGE/GLUCOPHAGE 500 mg XR antes de cualquier procedimiento quirúrgico o radiológico, ya que puede ser necesaria una interrupción temporal [ver ADVERTENCIAS Y PRECAUCIONES ].
Hipoglucemia
Informe a los pacientes que se puede producir hipoglucemia cuando se coadministra GLUCOPHAGE/GLUCOPHAGE XR con sulfonilureas orales e insulina. Explicar a los pacientes que reciben terapia concomitante los riesgos de la hipoglucemia, sus síntomas y tratamiento, y las condiciones que predisponen a su desarrollo [ver ADVERTENCIAS Y PRECAUCIONES ].
Deficiencia de vitamina B12
Informar a los pacientes sobre la importancia de los parámetros hematológicos regulares mientras reciben GLUCOPHAGE/GLUCOPHAGE XR [ver ADVERTENCIAS Y PRECAUCIONES ].
Hembras en edad reproductiva
Informe a las mujeres que el tratamiento con GLUCOPHAGE/GLUCOPHAGE XR puede provocar la ovulación en algunas mujeres premenopáusicas anovulatorias, lo que puede conducir a un embarazo no deseado [ver Uso en poblaciones específicas ].
Información de administración de Glucophage XR
Informe a los pacientes que GLUCOPHAGE 500 mg XR debe tragarse entero y no triturado, cortado ni masticado, y que los ingredientes inactivos pueden ocasionalmente eliminarse en las heces como una masa blanda que puede parecerse a la tableta original.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
Se han realizado estudios de carcinogenicidad a largo plazo en ratas (duración de la dosis de 104 semanas) y ratones (duración de la dosis de 91 semanas) a dosis de hasta 900 mg/kg/día y 1500 mg/kg/día, respectivamente. Ambas dosis son aproximadamente 3 veces la dosis diaria máxima recomendada en humanos de 2550 mg según las comparaciones del área de superficie corporal. No se encontró evidencia de carcinogenicidad con metformina en ratones machos o hembras. De manera similar, no se observó potencial tumorigénico con metformina en ratas macho. Sin embargo, hubo una mayor incidencia de pólipos uterinos estromales benignos en ratas hembra tratadas con 900 mg/kg/día.
No hubo evidencia de un potencial mutagénico de la metformina en las siguientes pruebas in vitro: prueba de Ames (S. typhimurium), prueba de mutación genética (células de linfoma de ratón) o prueba de aberraciones cromosómicas (linfocitos humanos). Los resultados de la prueba de micronúcleos de ratón in vivo también fueron negativos.
La fertilidad de ratas macho o hembra no se vio afectada por la metformina cuando se administró en dosis de hasta 600 mg/kg/día, que es aproximadamente 2 veces la dosis diaria máxima recomendada en humanos de 2550 mg según las comparaciones del área de superficie corporal.
Uso en poblaciones específicas
El embarazo
Resumen de riesgos
Los datos limitados con GLUCOPHAGE/GLUCOPHAGE XR en mujeres embarazadas no son suficientes para determinar un riesgo asociado al fármaco de anomalías congénitas importantes o abortos espontáneos. Los estudios publicados con el uso de metformina durante el embarazo no han informado una asociación clara entre la metformina y el riesgo de malformaciones congénitas importantes o abortos espontáneos [ver Datos ]. Hay riesgos para la madre y el feto asociados con la diabetes mellitus mal controlada en el embarazo [ver Consideraciones clínicas ].
No se observaron efectos adversos en el desarrollo cuando se administró metformina a ratas y conejas Sprague Dawley preñadas durante el período de organogénesis en dosis de hasta 2 y 5 veces, respectivamente, una dosis clínica de 2550 mg, según el área de superficie corporal [ver Datos ].
El riesgo de fondo estimado de defectos congénitos importantes es del 6 al 10 % en mujeres con diabetes mellitus pregestacional con HbA1C >7 y se ha informado que es tan alto como del 20 al 25 % en mujeres con HbA1C >10. Se desconoce el riesgo de fondo estimado de aborto espontáneo para la población indicada. En la población general de los EE. UU., el riesgo de fondo estimado de defectos congénitos importantes y aborto espontáneo en embarazos reconocidos clínicamente es del 2 al 4 % y del 15 al 20 %, respectivamente.
Consideraciones clínicas
Riesgo materno y/o embrionario/fetal asociado a la enfermedad
La diabetes mellitus mal controlada en el embarazo aumenta el riesgo materno de cetoacidosis diabética, preeclampsia, abortos espontáneos, parto prematuro, muerte fetal y complicaciones en el parto. La diabetes mellitus mal controlada aumenta el riesgo fetal de defectos congénitos importantes, muerte fetal y morbilidad relacionada con la macrosomía.
Datos
Datos humanos
Los datos publicados de los estudios posteriores a la comercialización no han informado una asociación clara entre metformina y defectos de nacimiento importantes, abortos espontáneos o resultados maternos o fetales adversos cuando se usó metformina durante el embarazo. Sin embargo, estos estudios no pueden establecer definitivamente la ausencia de ningún riesgo asociado con la metformina debido a las limitaciones metodológicas, incluido el tamaño pequeño de la muestra y los grupos de comparación inconsistentes.
Datos de animales
El clorhidrato de metformina no afectó negativamente los resultados del desarrollo cuando se administró a ratas y conejas preñadas en dosis de hasta 600 mg/kg/día. Esto representa una exposición de aproximadamente 2 y 5 veces una dosis clínica de 2550 mg según las comparaciones del área de superficie corporal para ratas y conejos, respectivamente. La determinación de las concentraciones fetales demostró una barrera placentaria parcial a la metformina.
Lactancia
Resumen de riesgos
Estudios publicados limitados informan que la metformina está presente en la leche humana [ver Datos ]. Sin embargo, no hay información suficiente para determinar los efectos de la metformina en el lactante y no hay información disponible sobre los efectos de la metformina en la producción de leche. Por lo tanto, los beneficios para el desarrollo y la salud de la lactancia deben considerarse junto con la necesidad clínica de la madre de GLUCOPHAGE/GLUCOPHAGE 500 mg XR y cualquier posible efecto adverso en el niño amamantado por GLUCOPHAGE/GLUCOPHAGE 850 mg XR o por la afección materna subyacente.
Datos
Los estudios clínicos de lactancia publicados informan que la metformina está presente en la leche humana, lo que resultó en dosis para lactantes de aproximadamente 0,11 % a 1 % de la dosis materna ajustada según el peso y una relación leche/plasma que oscila entre 0,13 y 1. Sin embargo, los estudios no fueron diseñados para establecer definitivamente el riesgo del uso de metformina durante la lactancia debido al pequeño tamaño de la muestra y los datos limitados de eventos adversos recopilados en lactantes.
Hembras y machos con potencial reproductivo
Analice la posibilidad de un embarazo no deseado con mujeres premenopáusicas, ya que la terapia con GLUCOPHAGE/GLUCOPHAGE XR puede provocar la ovulación en algunas mujeres con anovulación.
Uso pediátrico
glucófago
Se ha establecido la seguridad y eficacia de GLUCOPHAGE para el tratamiento de la diabetes mellitus tipo 2 en pacientes pediátricos de 10 a 16 años. No se ha establecido la seguridad y eficacia de GLUCOPHAGE en pacientes pediátricos menores de 10 años.
El uso de GLUCOPHAGE 850 mg en pacientes pediátricos de 10 a 16 años para el tratamiento de la diabetes mellitus tipo 2 está respaldado por la evidencia de estudios adecuados y bien controlados de GLUCOPHAGE en adultos con datos adicionales de un estudio clínico controlado en pacientes pediátricos de 10 a 16 años. de edad con diabetes mellitus tipo 2, que demostró una respuesta similar en el control glucémico a la observada en adultos [ver Estudios clínicos ]. En este estudio, las reacciones adversas fueron similares a las descritas en adultos. Se recomienda una dosis diaria máxima de 2000 mg de GLUCOPHAGE 1000 mg. [Ver DOSIFICACIÓN Y ADMINISTRACIÓN .]
Glucophage 1000mg XR
No se ha establecido la seguridad y eficacia de GLUCOPHAGE XR en pacientes pediátricos.
Uso geriátrico
Los estudios clínicos controlados de GLUCOPHAGE/GLUCOPHAGE XR no incluyeron un número suficiente de pacientes de edad avanzada para determinar si responden de manera diferente a los pacientes más jóvenes. En general, la selección de la dosis para un paciente anciano debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedad concomitante u otra terapia farmacológica y el mayor riesgo. de acidosis láctica. Evaluar la función renal con mayor frecuencia en pacientes de edad avanzada [ver ADVERTENCIAS Y PRECAUCIONES ].
Insuficiencia renal
La metformina se excreta sustancialmente por vía renal y el riesgo de acumulación de metformina y acidosis láctica aumenta con el grado de insuficiencia renal. GLUCOPHAGE/GLUCOPHAGE 850 mg XR está contraindicado en insuficiencia renal grave, pacientes con una tasa de filtración glomerular estimada (TFGe) inferior a 30 ml/min/1,73 m2 [ver DOSIFICACIÓN Y ADMINISTRACIÓN , CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES , y FARMACOLOGÍA CLÍNICA ].
Deterioro hepático
El uso de metformina en pacientes con insuficiencia hepática se ha asociado con algunos casos de acidosis láctica. GLUCOPHAGE/GLUCOPHAGE 500 mg XR no se recomienda en pacientes con insuficiencia hepática. [ver ADVERTENCIAS Y PRECAUCIONES ].
SOBREDOSIS
Se ha producido una sobredosis de clorhidrato de metformina, incluida la ingestión de cantidades superiores a 50 gramos. Se notificó hipoglucemia en aproximadamente el 10 % de los casos, pero no se ha establecido una asociación causal con la metformina. Se ha notificado acidosis láctica en aproximadamente el 32 % de los casos de sobredosis de metformina [ver ADVERTENCIAS Y PRECAUCIONES ]. La metformina es dializable con un aclaramiento de hasta 170 ml/min en buenas condiciones hemodinámicas. Por lo tanto, la hemodiálisis puede ser útil para eliminar el fármaco acumulado en pacientes en quienes se sospecha una sobredosis de metformina.
CONTRAINDICACIONES
GLUCOPHAGE 1000 mg y GLUCOPHAGE 850 mg XR están contraindicados en pacientes con:
- Insuficiencia renal grave (TFGe inferior a 30 ml/min/1,73 m2) [ver ADVERTENCIAS Y PRECAUCIONES ].
- Hipersensibilidad a la metformina.
- Acidosis metabólica aguda o crónica, incluida la cetoacidosis diabética, con o sin coma.
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
La metformina es un agente antihiperglucemiante que mejora la tolerancia a la glucosa en pacientes con diabetes mellitus tipo 2, reduciendo la glucosa plasmática tanto basal como posprandial. La metformina disminuye la producción de glucosa hepática, disminuye la absorción intestinal de glucosa y mejora la sensibilidad a la insulina al aumentar la captación y utilización de glucosa periférica. Con la terapia con metformina, la secreción de insulina permanece sin cambios, mientras que los niveles de insulina en ayunas y la respuesta de insulina plasmática a lo largo del día pueden disminuir.
Farmacocinética
Absorción
La biodisponibilidad absoluta de un comprimido de GLUCOPHAGE de 500 mg administrado en ayunas es aproximadamente del 50 % al 60 %. Los estudios que utilizan dosis orales únicas de GLUCOPHAGE de 500 a 1500 mg y de 850 a 2550 mg indican que existe una falta de proporcionalidad de la dosis con dosis crecientes, lo que se debe a una menor absorción en lugar de una alteración en la eliminación. A las dosis clínicas habituales y los programas de dosificación de GLUCOPHAGE, las concentraciones plasmáticas de metformina en estado estacionario se alcanzan dentro de las 24 a 48 horas y generalmente son
Después de una dosis oral única de GLUCOPHAGE 500 mg XR, la Cmax se alcanza con un valor medio de 7 horas y un rango de 4 a 8 horas. Los niveles plasmáticos máximos son aproximadamente un 20 % inferiores en comparación con la misma dosis de GLUCOPHAGE de 1000 mg; sin embargo, el grado de absorción (medido por el AUC) es comparable al de GLUCOPHAGE.
En el estado estacionario, el AUC y la Cmax son menos que la dosis proporcional para GLUCOPHAGE XR dentro del rango de 500 a 2000 mg administrados una vez al día. Los niveles plasmáticos máximos son de aproximadamente 0,6, 1,1, 1,4 y 1,8 mcg/ml para dosis de 500, 1000, 1500 y 2000 mg una vez al día, respectivamente. El grado de absorción de metformina (medido por el AUC) de GLUCOPHAGE 500 mg XR en una dosis de 2000 mg una vez al día es similar a la misma dosis diaria total administrada como tabletas de GLUCOPHAGE 850 mg 1000 mg dos veces al día. Después de la administración repetida de GLUCOPHAGE XR, la metformina no se acumuló en el plasma.
Efecto de la comida:
Los alimentos disminuyen el grado de absorción y retrasan ligeramente la absorción de metformina, como lo demuestra una concentración plasmática máxima media (Cmax) aproximadamente un 40 % más baja, un área bajo la curva de concentración plasmática versus tiempo (AUC) un 25 % más baja y un minutos de prolongación del tiempo hasta la concentración plasmática máxima (Tmax) luego de la administración de una sola tableta de 850 mg de GLUCOPHAGE con alimentos, en comparación con la misma concentración de tableta administrada en ayunas.
Aunque el grado de absorción de metformina (medido por el AUC) de la tableta GLUCOPHAGE XR aumentó aproximadamente un 50 % cuando se administró con alimentos, no hubo efecto de los alimentos sobre la Cmax y la Tmax de metformina. Tanto las comidas altas como las bajas en grasas tuvieron el mismo efecto sobre la farmacocinética de GLUCOPHAGE XR.
Distribución
El volumen aparente de distribución (V/F) de la metformina luego de dosis orales únicas de GLUCOPHAGE 850 mg promedió 654 ± 358 L. La metformina se une de manera insignificante a las proteínas plasmáticas. La metformina se divide en eritrocitos, probablemente en función del tiempo.
Metabolismo
Los estudios de dosis única intravenosa en sujetos normales demuestran que la metformina se excreta sin cambios en la orina y no sufre metabolismo hepático (no se han identificado metabolitos en humanos) ni excreción biliar.
Eliminación
El aclaramiento renal (ver Tabla 4) es aproximadamente 3,5 veces mayor que el aclaramiento de creatinina, lo que indica que la secreción tubular es la vía principal de eliminación de metformina. Tras la administración oral, aproximadamente el 90% del fármaco absorbido se elimina por vía renal en las primeras 24 horas, con una semivida de eliminación plasmática de aproximadamente 6,2 horas. En sangre, la vida media de eliminación es de aproximadamente 17,6 horas, lo que sugiere que la masa de eritrocitos puede ser un compartimento de distribución.
Poblaciones Específicas
Insuficiencia renal
En pacientes con función renal disminuida, la vida media plasmática y sanguínea de la metformina se prolonga y el aclaramiento renal se reduce (ver Tabla 3) [Ver DOSIFICACIÓN Y ADMINISTRACIÓN , CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES y Uso en poblaciones específicas ].
Deterioro hepático
No se han realizado estudios farmacocinéticos de metformina en pacientes con insuficiencia hepática [Ver ADVERTENCIAS Y PRECAUCIONES y Uso en poblaciones específicas ].
Geriatría
Los datos limitados de estudios farmacocinéticos controlados de GLUCOPHAGE 1000 mg en sujetos sanos de edad avanzada sugieren que el aclaramiento plasmático total de metformina disminuye, la vida media se prolonga y la Cmax aumenta, en comparación con sujetos jóvenes sanos. Parece que el cambio en la farmacocinética de metformina con el envejecimiento se explica principalmente por un cambio en la función renal (ver Tabla 4). [Ver ADVERTENCIAS Y PRECAUCIONES y Uso en poblaciones específicas ].
Pediatría
Después de la administración de un único comprimido oral de GLUCOPHAGE 500 mg con alimentos, la media geométrica de la Cmax y el AUC de metformina difirieron en menos del 5 % entre pacientes pediátricos con diabetes tipo 2 (12-16 años de edad) y adultos sanos del mismo sexo y peso (20-16 años). 45 años de edad), todos con función renal normal.
Género
Los parámetros farmacocinéticos de metformina no difirieron significativamente entre sujetos normales y pacientes con diabetes mellitus tipo 2 cuando se analizaron según el género (hombres = 19, mujeres = 16).
La raza
No se han realizado estudios de los parámetros farmacocinéticos de metformina según la raza.
Interacciones con la drogas
Evaluación in vivo de las interacciones farmacológicas
Estudios clínicos
glucófago
Estudios clínicos en adultos
Se llevó a cabo un ensayo clínico multicéntrico, doble ciego, controlado con placebo en los EE. UU. en el que participaron pacientes obesos con diabetes mellitus tipo 2 cuya hiperglucemia no se controló adecuadamente solo con el tratamiento dietético (glucosa plasmática en ayunas [GPA] inicial de aproximadamente 240 mg/dl). Los pacientes fueron tratados con GLUCOPHAGE (hasta 2550 mg/día) o placebo durante 29 semanas. Los resultados se presentan en la Tabla 7.
El peso corporal inicial promedio fue de 201 lb y 206 lb en los brazos de GLUCOPHAGE 850 mg y placebo, respectivamente. El cambio medio en el peso corporal desde el inicio hasta la semana 29 fue de -1.4 lbs y -2.4 lbs en los brazos de GLUCOPHAGE 1000 mg y placebo, respectivamente. Un estudio de 29 semanas, doble ciego, controlado con placebo de GLUCOPHAGE y gliburida, solos y en combinación , se llevó a cabo en pacientes obesos con diabetes mellitus tipo 2 que no lograron un control glucémico adecuado mientras recibían dosis máximas de gliburida (GPA inicial de aproximadamente 250 mg/dL). Los pacientes aleatorizados al brazo de combinación comenzaron la terapia con GLUCOPHAGE 500 mg y gliburida 20 mg. Al final de cada semana de las primeras 4 semanas del ensayo, a estos pacientes se les aumentó la dosis de GLUCOPHAGE 500 mg en 500 mg si no habían logrado alcanzar el objetivo de glucosa plasmática en ayunas. Después de la semana 4, dichos ajustes de dosis se realizaron mensualmente, aunque a ningún paciente se le permitió exceder los 2500 mg de GLUCOPHAGE. Los pacientes del grupo de GLUCOPHAGE solo (metformina más placebo) suspendieron la gliburida y siguieron el mismo programa de titulación. Los pacientes en el brazo de gliburida continuaron con la misma dosis de gliburida. Al final del ensayo, aproximadamente el 70 % de los pacientes del grupo de combinación tomaban GLUCOPHAGE 2000 mg/gliburida 20 mg o GLUCOPHAGE 2500 mg/gliburida 20 mg. Los resultados se muestran en la Tabla 8.
El peso corporal inicial promedio fue de 202 lb, 203 lb y 204 lb en los brazos de GLUCOPHAGE/gliburida, gliburida y GLUCOPHAGE de 500 mg, respectivamente. El cambio medio en el peso corporal desde el inicio hasta la semana 29 fue de 0,9 lb, -0,7 lb y -8,4 lb en los brazos de GLUCOPHAGE/gliburida, gliburida y GLUCOPHAGE de 850 mg, respectivamente.
Estudios clínicos pediátricos
Un estudio doble ciego, controlado con placebo en pacientes pediátricos de 10 a 16 años con diabetes mellitus tipo 2 (GPA promedio 182.2 mg/dL), tratamiento con GLUCOPHAGE (hasta 2000 mg/día) por hasta 16 semanas (duración promedio de tratamiento 11 semanas) se llevó a cabo. Los resultados se muestran en la Tabla 9.
El peso corporal inicial promedio fue de 205 lb y 189 lb en los brazos de GLUCOPHAGE 850 mg y placebo, respectivamente. El cambio medio en el peso corporal desde el inicio hasta la semana 16 fue de -3,3 libras y -2,0 libras en los brazos de GLUCOPHAGE 500 mg y placebo, respectivamente.
Glucofago XR
Se realizó un estudio de 24 semanas, doble ciego, controlado con placebo de GLUCOPHAGE 1000 mg XR, tomado una vez al día con la cena, en pacientes con diabetes mellitus tipo 2 que no lograron controlar la glucemia con dieta y ejercicio. Los pacientes que ingresaron al estudio tenían una HbA1c inicial media de 8,0 % y una GPA inicial media de 176 mg/dl. La dosis de tratamiento se aumentó a 1500 mg una vez al día si en la semana 12 la HbA1c era ≥7,0 % pero
Se realizó un estudio de respuesta a la dosis, doble ciego, controlado con placebo, de 16 semanas de duración de GLUCOPHAGE 500 mg XR, tomado una vez al día con la cena o dos veces al día con las comidas, en pacientes con diabetes mellitus tipo 2 que no habían logrado alcanzar controlar con dieta y ejercicio. Los resultados se muestran en la Tabla 10.
El peso corporal inicial promedio fue de 193 lb, 192 lb, 188 lb, 196 lb, 193 lb y 194 lb en los brazos de GLUCOPHAGE XR de 500 mg, 1000 mg, 1500 mg y 2000 mg una vez al día, 1000 mg dos veces al día y placebo, respectivamente. . El cambio medio en el peso corporal desde el inicio hasta la semana 16 fue de -1,3 lb, -1,3 lb, -0,7 lb, -1,5 lb, -2,2 lb y -1,8 lb, respectivamente.
Se realizó un estudio aleatorizado, doble ciego, de 24 semanas de GLUCOPHAGE XR, tomado una vez al día con la cena, y GLUCOPHAGE 500 mg, tomado dos veces al día (con el desayuno y la cena), en pacientes con diabetes mellitus tipo 2 que habían sido tratados con GLUCOPHAGE 500 mg dos veces al día durante al menos 8 semanas antes del ingreso al estudio. Los resultados se muestran en la Tabla 11.
El peso corporal inicial promedio fue de 210 lb, 203 lb y 193 lb en los brazos de GLUCOPHAGE 500 mg dos veces al día y GLUCOPHAGE XR 1000 mg y 1500 mg una vez al día, respectivamente. El cambio medio en el peso corporal desde el inicio hasta la semana 24 fue de 0,9 lb, 1,1 lb y 0,9 lb, respectivamente.
INFORMACIÓN DEL PACIENTE
GLUCOPHAGE® [gloo-ko-fahzh] (clorhidrato de metformina) Comprimidos
y
GLUCOPHAGE® XR [gloo-ko-fahzh XR] (clorhidrato de metformina) tabletas de liberación prolongada
Lea la Información para el paciente que viene con GLUCOPHAGE y GLUCOPHAGE 1000mg XR antes de comenzar a tomarlo y cada vez que renueve su receta. Es posible que haya nueva información. Este folleto no reemplaza la conversación con su proveedor de atención médica sobre su condición médica o tratamiento.
¿Cuál es la información más importante que debo saber sobre GLUCOPHAGE 1000mg y GLUCOPHAGE 500mg XR?
Pueden ocurrir efectos secundarios graves en personas que toman GLUCOPHAGE o GLUCOPHAGE 1000mg XR, que incluyen:
Acidosis láctica. El clorhidrato de metformina, el medicamento en GLUCOPHAGE 500 mg y GLUCOPHAGE XR, puede causar un efecto secundario raro pero grave llamado acidosis láctica (una acumulación de ácido láctico en la sangre) que puede causar la muerte. La acidosis láctica es una emergencia médica y debe tratarse en un hospital.
Deje de tomar GLUCOPHAGE o GLUCOPHAGE 500 mg XR y llame a su proveedor de atención médica de inmediato si presenta alguno de los siguientes síntomas de acidosis láctica:
- sentirse muy débil y cansado
- tiene dolor muscular inusual (no normal)
- tener problemas para respirar
- tiene somnolencia inusual o duerme más de lo habitual
- tiene problemas estomacales o intestinales inexplicables con náuseas y vómitos o diarrea
- sentir frío, especialmente en los brazos y las piernas
- sentirse mareado o aturdido
- tiene latidos cardíacos lentos o irregulares
Tiene una mayor probabilidad de tener acidosis láctica si:
- tiene problemas renales. Las personas cuyos riñones no funcionan correctamente no deben tomar GLUCOPHAGE 850 mg O GLUCOPHAGE XR.
- tiene problemas hepáticos.
- tiene insuficiencia cardíaca congestiva que requiere tratamiento con medicamentos.
- bebe mucho alcohol (muy a menudo o bebe en "combustibles" a corto plazo).
- deshidratarse (perder una gran cantidad de líquidos corporales). Esto puede suceder si tiene fiebre, vómitos o diarrea. La deshidratación también puede ocurrir cuando suda mucho con la actividad o el ejercicio y no bebe suficientes líquidos.
- someterse a ciertas pruebas de rayos X con tintes inyectables o agentes de contraste.
- tener cirugia.
- tiene un ataque al corazón, una infección grave o un derrame cerebral.
- tiene 80 años de edad o más y no se ha hecho una prueba de función renal.
¿Qué son GLUCOPHAGE y GLUCOPHAGE 1000mg XR?
- GLUCOPHAGE y GLUCOPHAGE XR son medicamentos recetados que contienen clorhidrato de metformina. GLUCOPHAGE 500 mg y GLUCOPHAGE 1000 mg XR se usan con dieta y ejercicio para ayudar a controlar el nivel alto de azúcar en la sangre (hiperglucemia) en adultos con diabetes tipo 2.
- GLUCOPHAGE 850 mg y GLUCOPHAGE 500 mg XR no son para personas con diabetes tipo 1.
- GLUCOPHAGE 850 mg y GLUCOPHAGE 500 mg XR no son para personas con cetoacidosis diabética (aumento de cetonas en la sangre o la orina).
GLUCOPHAGE 850mg y GLUCOPHAGE 1000mg XR tienen el mismo ingrediente activo. Sin embargo, GLUCOPHAGE XR funciona por más tiempo en su cuerpo. Ambos medicamentos ayudan a controlar el azúcar en la sangre de varias maneras. Estos incluyen ayudar a su cuerpo a responder mejor a la insulina que produce naturalmente, disminuir la cantidad de azúcar que produce su hígado y disminuir la cantidad de azúcar que absorben sus intestinos. GLUCOPHAGE 1000 mg y GLUCOPHAGE 850 mg XR no hacen que su cuerpo produzca más insulina.
¿Quién no debe tomar GLUCOPHAGE o GLUCOPHAGE 850mg XR?
Algunas condiciones aumentan su probabilidad de contraer acidosis láctica o causan otros problemas si toma cualquiera de estos medicamentos. La mayoría de las condiciones enumeradas a continuación pueden aumentar su probabilidad de contraer acidosis láctica.
No tome GLUCOPHAGE 1000 mg o GLUCOPHAGE 500 mg XR si usted:
- tiene problemas renales
- es alérgico al clorhidrato de metformina en GLUCOPHAGE o GLUCOPHAGE 850mg XR o a cualquiera de los ingredientes en GLUCOPHAGE o GLUCOPHAGE XR. Consulte el final de este folleto para obtener una lista completa de los ingredientes de GLUCOPHAGE y GLUCOPHAGE XR.
- va a recibir una inyección de tinte o agentes de contraste para un procedimiento de rayos X o si va a someterse a una cirugía y no puede comer ni beber mucho. En estas situaciones, será necesario suspender GLUCOPHAGE 1000 mg o GLUCOPHAGE XR por un período breve. Hable con su proveedor de atención médica acerca de cuándo debe dejar de tomar GLUCOPHAGE 850 mg o GLUCOPHAGE 850 mg XR y cuándo debe comenzar nuevamente con GLUCOPHAGE o GLUCOPHAGE XR. Ver “¿Cuál es la información más importante que debo saber sobre GLUCOPHAGE o GLUCOPHAGE XR?”
¿Qué debo decirle a mi proveedor de atención médica antes de tomar GLUCOPHAGE o GLUCOPHAGE 1000mg XR?
Antes de tomar GLUCOPHAGE 500 mg o GLUCOPHAGE XR, informe a su proveedor de atención médica si:
- tiene diabetes tipo 1. GLUCOPHAGE 850 mg o GLUCOPHAGE 500 mg XR no deben usarse para tratar a personas con diabetes tipo 1.
- tiene antecedentes o riesgo de cetoacidosis diabética (niveles altos de ciertos ácidos, conocidos como cetonas, en la sangre o la orina). GLUCOPHAGE 1000 mg o GLUCOPHAGE XR no deben usarse para el tratamiento de la cetoacidosis diabética.
- tiene problemas renales.
- tiene problemas hepáticos.
- tiene problemas cardíacos, incluida la insuficiencia cardíaca congestiva.
- son mayores de 80 años. Si tiene más de 80 años, no debe tomar GLUCOPHAGE 1000 mg o GLUCOPHAGE XR a menos que sus riñones hayan sido revisados y estén normales.
- bebe alcohol con mucha frecuencia, o bebe mucho alcohol en “atracones” breves.
- están tomando insulina.
- tiene otras condiciones médicas.
- está embarazada o planea quedar embarazada. No se sabe si GLUCOPHAGE o GLUCOPHAGE 850mg XR dañarán a su bebé por nacer. Si está embarazada, hable con su proveedor de atención médica sobre la mejor manera de controlar su nivel de azúcar en la sangre mientras está embarazada.
- está amamantando o planea amamantar. No se sabe si GLUCOPHAGE 850 mg o GLUCOPHAGE XR pasa a la leche materna. Hable con su proveedor de atención médica sobre la mejor manera de alimentar a su bebé mientras toma GLUCOPHAGE 500 mg o GLUCOPHAGE 500 mg XR.
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluyendo medicamentos recetados y de venta libre, vitaminas y suplementos a base de hierbas. Conozca los medicamentos que toma. Mantenga una lista de ellos para mostrársela a su proveedor de atención médica y farmacéutico cuando obtenga un nuevo medicamento.
- GLUCOPHAGE o GLUCOPHAGE XR pueden afectar el funcionamiento de otros medicamentos, y otros medicamentos pueden afectar el funcionamiento de GLUCOPHAGE o GLUCOPHAGE XR.
¿Se puede usar GLUCOPHAGE o GLUCOPHAGE 500mg XR en niños?
Se ha demostrado que GLUCOPHAGE 1000 mg reduce efectivamente los niveles de glucosa en niños (de 10 a 16 años) con diabetes tipo 2. GLUCOPHAGE 1000 mg no se ha estudiado en niños menores de 10 años. GLUCOPHAGE 500 mg no se ha estudiado en combinación con otros medicamentos orales para el control de la glucosa o insulina en niños. Si tiene alguna pregunta sobre el uso de GLUCOPHAGE 1000 mg en niños, hable con su médico u otro proveedor de atención médica.
GLUCOPHAGE XR no se ha estudiado en niños.
¿Cómo debo tomar GLUCOPHAGE o GLUCOPHAGE XR?
- Tome GLUCOPHAGE 850 mg o GLUCOPHAGE 850 mg XR exactamente como le indique su proveedor de atención médica.
- GLUCOPHAGE o GLUCOPHAGE 850 mg XR deben tomarse con las comidas para ayudar a disminuir el efecto secundario del malestar estomacal.
- Trague GLUCOPHAGE o GLUCOPHAGE 500 mg XR entero. No triture, corte ni mastique GLUCOPHAGE 1000mg XR.
- veces, es posible que expulse una masa blanda en las heces (evacuación intestinal) que se parece a las tabletas de GLUCOPHAGE 850 mg o GLUCOPHAGE XR. Esto no es dañino y no afectará la forma en que GLUCOPHAGE 850mg XR funciona para controlar su diabetes.
- Cuando su cuerpo está bajo algún tipo de estrés, como fiebre, trauma (como un accidente automovilístico), infección o cirugía, la cantidad de medicamento para la diabetes que necesita puede cambiar. Informe a su proveedor de atención médica de inmediato si tiene alguno de estos problemas.
- Su proveedor de atención médica debe realizar análisis de sangre para verificar qué tan bien están funcionando sus riñones antes y durante su tratamiento con GLUCOPHAGE 1000 mg o GLUCOPHAGE 500 mg XR.
- Su proveedor de atención médica controlará su diabetes con análisis de sangre regulares, incluidos sus niveles de azúcar en la sangre y su hemoglobina A1C.
- Siga las instrucciones de su proveedor de atención médica para tratar un nivel demasiado bajo de azúcar en la sangre (hipoglucemia). Hable con su proveedor de atención médica si el nivel bajo de azúcar en la sangre es un problema para usted. Ver “¿Cuáles son los posibles efectos secundarios de GLUCOPHAGE o GLUCOPHAGE XR?”
- Controle su nivel de azúcar en la sangre como se lo indique su proveedor de atención médica.
- Siga la dieta y el programa de ejercicios recetados mientras toma GLUCOPHAGE 850 mg o GLUCOPHAGE 850 mg XR.
- Si olvida una dosis de GLUCOPHAGE 1000 mg o GLUCOPHAGE 850 mg XR, tome la próxima dosis según lo prescrito a menos que su proveedor de atención médica le indique lo contrario. No tome una dosis extra al día siguiente.
- Si toma demasiado GLUCOPHAGE 500 mg o GLUCOPHAGE 500 mg XR, llame a su proveedor de atención médica, al centro local de control de intoxicaciones o vaya a la sala de emergencias del hospital más cercano de inmediato.
¿Qué debo evitar mientras tomo GLUCOPHAGE o GLUCOPHAGE 1000mg XR?
No tome muchas bebidas alcohólicas mientras toma GLUCOPHAGE o GLUCOPHAGE XR. Esto significa que no debe beber en exceso durante períodos cortos y no debe beber mucho alcohol de forma regular. El alcohol puede aumentar la probabilidad de contraer acidosis láctica.
¿Cuáles son los efectos secundarios de GLUCOPHAGE y GLUCOPHAGE XR?
- Acidosis láctica. La metformina, el ingrediente activo de GLUCOPHAGE 1000 mg y GLUCOPHAGE 500 mg XR, puede causar una condición rara pero grave llamada acidosis láctica (una acumulación de ácido en la sangre) que puede causar la muerte. La acidosis láctica es una emergencia médica y debe tratarse en el hospital.
Llame a su médico de inmediato si tiene alguno de los siguientes síntomas, que podrían ser signos de acidosis láctica:
- siente frío en las manos o los pies
- te sientes mareado o aturdido
- usted tiene un ritmo cardíaco lento o irregular
- te sientes muy débil o cansado
- tienes problemas para respirar
- te sientes somnoliento o somnoliento
- tiene dolores de estómago, náuseas o vómitos
La mayoría de las personas que han tenido acidosis láctica con metformina tienen otras cosas que, combinadas con la metformina, llevaron a la acidosis láctica. Informe a su médico si tiene cualquiera de los siguientes, porque tiene una mayor probabilidad de tener acidosis láctica con GLUCOPHAGE 850 mg o GLUCOPHAGE 500 mg XR si:
- tiene problemas renales graves, o sus riñones se ven afectados por ciertas pruebas de rayos X que usan un tinte inyectable
- tiene problemas hepáticos
- beber alcohol con mucha frecuencia, o beber mucho alcohol en "atracones" breves
- deshidratarse (perder una gran cantidad de líquidos corporales). Esto puede suceder si tiene fiebre, vómitos o diarrea. La deshidratación también puede ocurrir cuando suda mucho con la actividad o el ejercicio y no bebe suficientes líquidos.
- tener cirugia
- tiene un ataque al corazón, una infección grave o un derrame cerebral
Los efectos secundarios comunes de GLUCOPHAGE 500 mg y GLUCOPHAGE 1000 mg XR incluyen diarrea, náuseas y malestar estomacal. Estos efectos secundarios generalmente desaparecen después de tomar el medicamento por un tiempo. Tomar su medicamento con las comidas puede ayudar a reducir estos efectos secundarios. Informe a su médico si los efectos secundarios le molestan mucho, duran más de unas pocas semanas, reaparecen después de que han desaparecido o comienzan más tarde en la terapia. Es posible que necesite una dosis más baja o que deba dejar de tomar el medicamento por un período corto o para siempre.
Aproximadamente 3 de cada 100 personas que toman GLUCOPHAGE o GLUCOPHAGE 1000mg XR tienen un sabor metálico desagradable cuando comienzan a tomar el medicamento. Dura poco tiempo.
GLUCOPHAGE 850 mg y GLUCOPHAGE 500 mg XR rara vez causan hipoglucemia (bajo nivel de azúcar en la sangre) por sí mismos. Sin embargo, la hipoglucemia puede ocurrir si no come lo suficiente, si bebe alcohol o si toma otros medicamentos para reducir el nivel de azúcar en la sangre.
¿Cómo debo almacenar GLUCOPHAGE 500 mg y GLUCOPHAGE XR?
Almacene GLUCOPHAGE y GLUCOPHAGE 850 mg XR a una temperatura de 68 °F a 77 °F (20 °C a 25 °C).
Mantenga GLUCOPHAGE 850 mg y GLUCOPHAGE 500 mg XR y todos los medicamentos fuera del alcance de los niños.
Información general sobre el uso de GLUCOPHAGE 850mg y GLUCOPHAGE 850mg XR
Si tiene preguntas o problemas, hable con su médico u otro proveedor de atención médica. Puede pedirle a su médico o farmacéutico la información sobre GLUCOPHAGE 850 mg y GLUCOPHAGE 500 mg XR que está escrita para profesionales de la salud. A veces, los medicamentos se prescriben para fines distintos a los enumerados en el prospecto de información para el paciente. No use GLUCOPHAGE 1000 mg o GLUCOPHAGE 1000 mg XR para una condición para la cual no fue recetado. No compartas tu medicina con otras personas.
¿Cuáles son los ingredientes de GLUCOPHAGE y GLUCOPHAGE 500mg XR?
Principios activos de GLUCOPHAGE: clorhidrato de metformina.
Ingredientes inactivos en cada tableta de GLUCOPHAGE: povidona y estearato de magnesio. Además, el recubrimiento de los comprimidos de 500 mg y 850 mg contiene hipromelosa y el recubrimiento del comprimido de 1000 mg contiene hipromelosa y polietilenglicol.
Principios activos de GLUCOPHAGE 1000mg XR: clorhidrato de metformina.
Ingredientes inactivos en cada tableta de GLUCOPHAGE 1000mg XR 500 mg: carboximetilcelulosa de sodio, hipromelosa, celulosa microcristalina y estearato de magnesio.
Ingredientes inactivos en cada tableta de GLUCOPHAGE XR 750 mg: carboximetilcelulosa de sodio, hipromelosa y estearato de magnesio.
¿Qué es la diabetes tipo 2?
La diabetes tipo 2 es una afección en la que su cuerpo no produce suficiente insulina y la insulina que produce su cuerpo no funciona tan bien como debería. Su cuerpo también puede producir demasiada azúcar. Cuando esto sucede, el azúcar (glucosa) se acumula en la sangre. Esto puede conducir a problemas médicos graves.
El objetivo principal del tratamiento de la diabetes es reducir el nivel de azúcar en la sangre a un nivel normal.
El nivel alto de azúcar en la sangre se puede reducir con dieta y ejercicio, y con ciertos medicamentos cuando sea necesario.
Hable con su proveedor de atención médica sobre cómo prevenir, reconocer y tratar el nivel bajo de azúcar en la sangre (hipoglucemia), el nivel alto de azúcar en la sangre (hiperglucemia) y los problemas que tiene debido a la diabetes.
