Precose 25mg, 50mg Acarbose Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Precose 50 mg y cómo se usa?
Precose (tabletas de acarbosa) es un inhibidor oral de alfa-glucosidasa que se usa para tratar la diabetes tipo 2. Precose 50 mg a veces se usa en combinación con insulina u otros medicamentos para la diabetes que se toman por vía oral. Precose 25 mg está disponible en forma genérica.
¿Cuáles son los efectos secundarios de Precose 25 mg?
Los efectos secundarios comunes de Precose incluyen:
- Diarrea,
- gas,
- hinchazón,
- malestar estomacal, o
- dolor de estómago en las primeras semanas de tratamiento a medida que su cuerpo se adapta a este medicamento, pero generalmente mejora con el tiempo.
Otros efectos secundarios de Precose 50 mg incluyen erupción cutánea o picazón. Informe a su médico si tiene efectos secundarios raros pero muy graves de Precose 25 mg, que incluyen:
- cansancio inusual,
- náuseas o vómitos persistentes,
- dolor estomacal o abdominal intenso,
- sangrado rectal,
- ojos o piel amarillentos, o
- orina oscura.
DESCRIPCIÓN
PRECOSE® (tabletas de acarbosa) es un inhibidor oral de alfa-glucosidasa para uso en el tratamiento de la diabetes mellitus tipo 2. La acarbosa es un oligosacárido que se obtiene de los procesos de fermentación de un microorganismo, Actinoplanes utahensis, y se conoce químicamente como O-4,6-didesoxi4-[[(1S,4R,5S,6S)-4,5,6-trihidroxi- 3-(hidroximetil)-2-ciclohexen-1-il]amino] α-D-glucopiranos il-(1 → 4)-O-α-D-glucopiranosil-(1 →4)-D-glucosa. Es un polvo de color blanco a blanquecino con un peso molecular de 645,6. La acarbosa es soluble en agua y tiene un pKa de 5,1. Su fórmula empírica es C25H43NO18 y su estructura química es la siguiente:
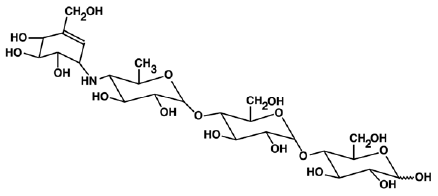
PRECOSE 50 mg está disponible en comprimidos de 25 mg, 50 mg y 100 mg para uso oral. Los ingredientes inactivos son almidón, celulosa microcristalina, estearato de magnesio y dióxido de silicio coloidal.
INDICACIONES
PRECOSE está indicado como complemento de la dieta y el ejercicio para mejorar el control glucémico en adultos con diabetes mellitus tipo 2.
DOSIFICACIÓN Y ADMINISTRACIÓN
No existe un régimen de dosificación fijo para el manejo de la diabetes mellitus con PRECOSE o cualquier otro agente farmacológico. La dosis de PRECOSE 25 mg debe individualizarse en función de la eficacia y la tolerancia sin exceder la dosis máxima recomendada de 100 mg tres veces al día. PRECOSE debe tomarse tres veces al día al comienzo (con el primer bocado) de cada comida principal.
PRECOSE debe iniciarse con una dosis baja, con un aumento gradual de la dosis como se describe a continuación, tanto para reducir los efectos secundarios gastrointestinales como para permitir la identificación de la dosis mínima requerida para un control glucémico adecuado del paciente. Si no se sigue la dieta prescrita, los efectos secundarios intestinales pueden intensificarse. Si se desarrollan síntomas muy angustiantes a pesar de la adherencia a la dieta diabética prescrita, se debe consultar al médico y se debe reducir la dosis de manera temporal o permanente.
Durante el inicio del tratamiento y la titulación de la dosis (ver a continuación), se puede usar la glucosa plasmática posprandial de una hora para determinar la respuesta terapéutica a PRECOSE e identificar la dosis mínima efectiva para el paciente. Posteriormente, la hemoglobina glicosilada debe medirse a intervalos de aproximadamente tres meses. El objetivo terapéutico debe ser disminuir tanto la glucosa plasmática posprandial como los niveles de hemoglobina glicosilada a niveles normales o casi normales mediante el uso de la dosis efectiva más baja de PRECOSE, ya sea como monoterapia o en combinación con sulfonilureas, insulina o metformina.
Dosis inicial
La dosis inicial recomendada de PRECOSE 25 mg es de 25 mg administrados por vía oral tres veces al día al comienzo (con el primer bocado) de cada comida principal. Sin embargo, algunos pacientes pueden beneficiarse de una titulación de dosis más gradual para minimizar los efectos secundarios gastrointestinales. Esto se puede lograr iniciando el tratamiento con 25 mg una vez al día y aumentando posteriormente la frecuencia de administración para alcanzar los 25 mg tres veces al día.
Dosis de mantenimiento
Una vez que se alcanza un régimen de dosificación de 25 mg tres veces al día, la dosis de PRECOSE de 50 mg debe ajustarse a intervalos de 4 a 8 semanas en función de los niveles de glucosa posprandial o de hemoglobina glicosilada de una hora, y de la tolerancia. La dosis se puede aumentar de 25 mg tres veces al día a 50 mg tres veces al día. Algunos pacientes pueden beneficiarse de un aumento adicional de la dosis a 100 mg tres veces al día. La dosis de mantenimiento varía de 50 mg tres veces al día a 100 mg tres veces al día. riesgo de transaminasas séricas elevadas, solo los pacientes con un peso corporal > 60 kg deben ser considerados para la titulación de la dosis por encima de 50 mg tres veces al día (ver PRECAUCIONES ). Si no se observa una reducción adicional en los niveles de glucosa posprandial o de hemoglobina glicosilada con la titulación a 100 mg tres veces al día, se debe considerar la reducción de la dosis. Una vez que se establece una dosis eficaz y tolerada, debe mantenerse.
Dosis máxima
La dosis máxima recomendada para pacientes ≤ 60 kg es de 50 mg tres veces al día La dosis máxima recomendada para pacientes > 60 kg es de 100 mg tres veces al día
Pacientes que reciben sulfonilureas o insulina
Las sulfonilureas o la insulina pueden causar hipoglucemia. PRECOSE administrado en combinación con una sulfonilurea o insulina causará una mayor disminución de la glucosa en sangre y puede aumentar el potencial de hipoglucemia. Si ocurre hipoglucemia, se deben hacer los ajustes apropiados en la dosis de estos agentes.
CÓMO SUMINISTRADO
PRECOSE está disponible en comprimidos redondos sin ranurar de 25 mg, 50 mg o 100 mg. La concentración de cada tableta es de color blanco a amarillo. El comprimido de 25 mg está codificado con la palabra "PRECOSE" en un lado y "25" en el otro lado. El comprimido de 50 mg está codificado con la palabra “PRECOSE” y “50” en el mismo lado. El comprimido de 100 mg está codificado con la palabra “PRECOSE” y “100” en el mismo lado. PRECOSE está disponible en frascos de 100 y 50 mg de concentración en paquetes de dosis unitaria de 100.
No almacenar a más de 25°C (77°F). Proteger de la humedad. Para las botellas, mantenga el recipiente bien cerrado.
Bayer HealthCare Pharmaceuticals Inc. Wayne, NJ 07470. Fabricado en Alemania. 11/11EFECTOS SECUNDARIOS
Tracto digestivo
Los síntomas gastrointestinales son las reacciones más comunes a PRECOSE. En ensayos estadounidenses controlados con placebo, las incidencias de dolor abdominal, diarrea y flatulencia fueron del 19 %, 31 % y 74 % respectivamente en 1255 pacientes tratados con PRECOSE 50–300 mg tres veces al día, mientras que las incidencias correspondientes fueron del 9 %, 12 % y 29% en 999 pacientes tratados con placebo.
En un estudio de seguridad de un año, durante el cual los pacientes mantuvieron diarios de síntomas gastrointestinales, el dolor abdominal y la diarrea tendieron a volver a los niveles previos al tratamiento con el tiempo, y la frecuencia e intensidad de las flatulencias tendieron a disminuir con el tiempo. El aumento de los síntomas del tracto gastrointestinal en pacientes tratados con PRECOSE 50 mg es una manifestación del mecanismo de acción de PRECOSE y está relacionado con la presencia de carbohidratos no digeridos en el tracto GI inferior.
Si no se sigue la dieta prescrita, los efectos secundarios intestinales pueden intensificarse. Si se desarrollan síntomas muy angustiantes a pesar de la adherencia a la dieta diabética prescrita, se debe consultar al médico y se debe reducir la dosis de manera temporal o permanente.
Niveles elevados de transaminasas séricas
Ver PRECAUCIONES .
Otros hallazgos anormales de laboratorio
Pequeñas reducciones en el hematocrito ocurrieron con mayor frecuencia en los pacientes tratados con PRECOSE que en los pacientes tratados con placebo, pero no se asociaron con reducciones en la hemoglobina. Los niveles bajos de calcio sérico y de vitamina B6 en plasma se asociaron con la terapia de 50 mg de PRECOSE, pero se cree que son espurios o no tienen importancia clínica.
Informes de eventos adversos posteriores a la comercialización
Los eventos adversos adicionales informados a partir de la experiencia posterior a la comercialización en todo el mundo incluyen hepatitis fulminante con desenlace fatal, reacciones cutáneas de hipersensibilidad (por ejemplo, erupción cutánea, eritema, exantema y uticaria), edema, íleo/subíleo, ictericia y/o hepatitis y daño hepático asociado, trombocitopenia y neumatosis. cystoides intestinalis (ver PRECAUCIONES ).
Neumatosis cistoides intestinalis
Ha habido informes poco frecuentes posteriores a la comercialización de neumatosis quística intestinal asociada con el uso de inhibidores de alfa-glucosidasa, incluido Precose. La neumatosis quística intestinal puede presentarse con síntomas de diarrea, secreción de moco, sangrado rectal y estreñimiento. Las complicaciones pueden incluir neumoperitoneo, vólvulo, obstrucción intestinal, intususcepción, hemorragia intestinal y perforación intestinal. Si se sospecha neumatosis quística intestinalis, suspenda Precose 25 mg y realice el diagnóstico por imágenes apropiado.
INTERACCIONES CON LA DROGAS
Ciertos medicamentos tienden a producir hiperglucemia y pueden conducir a la pérdida del control de la glucosa en sangre. Estos fármacos incluyen las tiazidas y otros diuréticos, corticosteroides, fenotiazinas, productos tiroideos, estrógenos, anticonceptivos orales, fenitoína, ácido nicotínico, simpaticomiméticos, bloqueadores de los canales de calcio e isoniazida. Cuando dichos medicamentos se administran a un paciente que recibe PRECOSE 25 mg, se debe observar de cerca al paciente por si pierde el control de la glucosa en sangre. Cuando dichos medicamentos se retiran de pacientes que reciben PRECOSE 50 mg en combinación con sulfonilureas o insulina, se debe observar de cerca a los pacientes para detectar cualquier evidencia de hipoglucemia.
Pacientes que reciben sulfonilureas o insulina: Los agentes de sulfonilureas o la insulina pueden causar hipoglucemia. PRECOSE 25 mg administrado en combinación con una sulfonilurea o insulina puede causar una mayor disminución de la glucosa en sangre y puede aumentar el potencial de hipoglucemia. Si ocurre hipoglucemia, se deben hacer los ajustes apropiados en la dosis de estos agentes. Muy raramente, se han notificado casos individuales de shock hipoglucémico en pacientes que reciben tratamiento con PRECOSE en combinación con sulfonilureas y/o insulina.
Los adsorbentes intestinales (por ejemplo, carbón) y las preparaciones de enzimas digestivas que contienen enzimas que dividen los carbohidratos (por ejemplo, amilasa, pancreatina) pueden reducir el efecto de PRECOSE y no deben tomarse de manera concomitante.
Se ha demostrado que PRECOSE 25 mg cambia la biodisponibilidad de la digoxina cuando se administran conjuntamente, lo que puede requerir un ajuste de la dosis de digoxina. (Ver FARMACOLOGÍA CLÍNICA , Interacciones fármaco-fármaco .)
ADVERTENCIAS
No se proporcionó información
PRECAUCIONES
General
Resultados macrovasculares
No se han realizado estudios clínicos que establezcan evidencia concluyente de reducción del riesgo macrovascular con PRECOSE 25 mg o cualquier otro fármaco antidiabético.
Hipoglucemia
Debido a su mecanismo de acción, PRECOSE cuando se administra solo no debe causar hipoglucemia en ayunas o en estado posprandial. Las sulfonilureas o la insulina pueden causar hipoglucemia. Debido a que PRECOSE 50 mg administrado en combinación con una sulfonilurea o insulina causará una mayor disminución de la glucosa en sangre, puede aumentar el potencial de hipoglucemia. La hipoglucemia no ocurre en pacientes que reciben metformina sola en las circunstancias habituales de uso, y no se observó un aumento en la incidencia de hipoglucemia en pacientes cuando se agregó PRECOSE 50 mg a la terapia con metformina.
La glucosa oral (dextrosa), cuya absorción no es inhibida por PRECOSE, debe usarse en lugar de la sacarosa (azúcar de caña) en el tratamiento de la hipoglucemia leve a moderada. La sacarosa, cuya hidrólisis a glucosa y fructosa es inhibida por PRECOSE, no es adecuada para la corrección rápida de la hipoglucemia. La hipoglucemia grave puede requerir el uso de una infusión de glucosa intravenosa o una inyección de glucagón.
Niveles elevados de transaminasas séricas
En estudios a largo plazo (hasta 12 meses, e incluyendo dosis de PRECOSE de 25 mg hasta 300 mg tres veces al día) realizados en los Estados Unidos, las elevaciones emergentes del tratamiento de las transaminasas séricas (AST y/o ALT) por encima del límite superior normal (ULN ), más de 1,8 veces el ULN y más de 3 veces el ULN ocurrieron en el 14 %, 6 % y 3 %, respectivamente, de los pacientes tratados con PRECOSE en comparación con el 7 %, 2 % y 1 %, respectivamente, de pacientes tratados con placebo. Aunque estas diferencias entre tratamientos fueron estadísticamente significativas, estas elevaciones fueron asintomáticas, reversibles, más comunes en mujeres y, en general, no se asociaron con otra evidencia de disfunción hepática. Además, estas elevaciones de transaminasas séricas parecían estar relacionadas con la dosis. En estudios de EE. UU. que incluyeron dosis de 50 mg de PRECOSE hasta la dosis máxima aprobada de 100 mg tres veces al día, las elevaciones de AST y/o ALT emergentes del tratamiento en cualquier nivel de gravedad fueron similares entre los pacientes tratados con PRECOSE y los pacientes tratados con placebo (p ≥ 0,496) .
En aproximadamente 3 millones de años-paciente de experiencia internacional posterior a la comercialización con PRECOSE 50 mg, se informaron 62 casos de elevaciones de transaminasas séricas > 500 UI/L (29 de los cuales se asociaron con ictericia). Cuarenta y uno de estos 62 pacientes recibieron tratamiento con 100 mg tres veces al día o más y 33 de 45 pacientes cuyo peso se informó pesaban
Pérdida de control de la glucosa en sangre
Cuando los pacientes diabéticos están expuestos a estrés como fiebre, trauma, infección o cirugía, puede ocurrir una pérdida temporal del control de la glucosa en sangre. En esos momentos, puede ser necesaria una terapia temporal con insulina.
Pruebas de laboratorio
La respuesta terapéutica a PRECOSE debe controlarse mediante pruebas periódicas de glucosa en sangre. Se recomienda medir los niveles de hemoglobina glicosilada para monitorear el control glucémico a largo plazo.
PRECOSE 25 mg, particularmente en dosis superiores a 50 mg tres veces al día, puede provocar elevaciones de las transaminasas séricas y, en raras ocasiones, hiperbilirrubinemia. Se recomienda controlar los niveles de transaminasas séricas cada 3 meses durante el primer año de tratamiento con PRECOSE y periódicamente a partir de entonces. Si se observan transaminasas elevadas, puede estar indicada una reducción de la dosis o la suspensión del tratamiento, especialmente si persisten las elevaciones.
Insuficiencia renal
Las concentraciones plasmáticas de PRECOSE en voluntarios con insuficiencia renal aumentaron proporcionalmente en relación con el grado de disfunción renal. No se han realizado ensayos clínicos a largo plazo en pacientes diabéticos con disfunción renal significativa (creatinina sérica > 2,0 mg/dl). Por lo tanto, no se recomienda el tratamiento de estos pacientes con PRECOSE 50 mg.
Carcinogénesis, mutagénesis y deterioro de la fertilidad
Se realizaron ocho estudios de carcinogenicidad con acarbosa. Se realizaron seis estudios en ratas (dos cepas, Sprague-Dawley y Wistar) y dos estudios en hámsters.
En el primer estudio con ratas, las ratas Sprague-Dawley recibieron acarbosa en el alimento en dosis altas (hasta aproximadamente 500 mg/kg de peso corporal) durante 104 semanas. El tratamiento con acarbosa resultó en un aumento significativo en la incidencia de tumores renales (adenomas y adenocarcinomas) y tumores benignos de células de Leydig. Este estudio se repitió con un resultado similar. Se realizaron más estudios para separar los efectos carcinogénicos directos de la acarbosa de los efectos indirectos resultantes de la desnutrición de carbohidratos inducida por las grandes dosis de acarbosa empleadas en los estudios. En un estudio con ratas Sprague-Dawley, se mezcló acarbosa con el alimento, pero se evitó la privación de carbohidratos mediante la adición de glucosa a la dieta.

En un estudio de 26 meses con ratas Sprague-Dawley, se administró acarbosa por sonda posprandial diaria para evitar los efectos farmacológicos del fármaco. En ambos estudios, no se produjo el aumento de la incidencia de tumores renales observado en los estudios originales. La acarbosa también se administró en los alimentos y por sonda posprandial en dos estudios separados en ratas Wistar. No se encontró una mayor incidencia de tumores renales en ninguno de estos estudios con ratas Wistar. En dos estudios de alimentación de hámsteres, con y sin suplementos de glucosa, tampoco hubo evidencia de carcinogenicidad.
La acarbosa no indujo ningún daño en el ADN in vitro en el ensayo de aberración cromosómica de CHO, el ensayo de mutagénesis bacteriana (Ames) o el ensayo de unión al ADN. In vivo, no se detectó daño en el ADN en la prueba letal dominante en ratones macho ni en la prueba de micronúcleos de ratón.
Los estudios de fertilidad realizados en ratas después de la administración oral no produjeron ningún efecto adverso sobre la fertilidad o sobre la capacidad general de reproducción.
El embarazo
Efectos teratogénicos: Embarazo Categoría B.
No se ha establecido la seguridad de PRECOSE en mujeres embarazadas. Se han realizado estudios de reproducción en ratas a dosis de hasta 480 mg/kg (que corresponden a 9 veces la exposición en humanos, según los niveles sanguíneos del fármaco) y no han revelado evidencia de alteración de la fertilidad o daño al feto debido a la acarbosa. En conejos, la reducción del aumento de peso corporal materno, probablemente como resultado de la actividad farmacodinámica de altas dosis de acarbosa en los intestinos, puede haber sido responsable de un ligero aumento en el número de pérdidas embrionarias. Sin embargo, los conejos que recibieron 160 mg/kg de acarbosa (que corresponde a 10 veces la dosis en el hombre, según el área de superficie corporal) no mostraron evidencia de embriotoxicidad y no hubo evidencia de teratogenicidad a una dosis 32 veces mayor que la dosis en el hombre (sobre la base del área de superficie corporal). área de superficie). Sin embargo, no existen estudios adecuados y bien controlados de PRECOSE 25 mg en mujeres embarazadas. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, este medicamento debe usarse durante el embarazo solo si es claramente necesario. Debido a que la información actual sugiere fuertemente que los niveles anormales de glucosa en sangre durante el embarazo están asociados con una mayor incidencia de anomalías congénitas, así como con una mayor morbilidad y mortalidad neonatal, la mayoría de los expertos recomiendan que se use insulina durante el embarazo para mantener los niveles de glucosa en sangre lo más cerca posible de lo normal. .
Madres lactantes
Se ha encontrado una pequeña cantidad de radiactividad en la leche de ratas lactantes después de la administración de acarbosa radiomarcada. No se sabe si este fármaco se excreta en la leche humana. Debido a que muchos medicamentos se excretan en la leche humana, PRECOSE 25 mg no debe administrarse a mujeres lactantes.
Uso pediátrico
No se ha establecido la seguridad y eficacia de PRECOSE 25 mg en pacientes pediátricos.
Uso geriátrico
Del número total de sujetos en estudios clínicos de PRECOSE 25 mg en los Estados Unidos, el 27 % tenía 65 años o más, mientras que el 4 % tenía 75 años o más. No se observaron diferencias generales en seguridad y eficacia entre estos sujetos y sujetos más jóvenes. El área media en estado estacionario bajo la curva (AUC) y las concentraciones máximas de acarbosa fueron aproximadamente 1,5 veces mayores en los voluntarios de edad avanzada que en los voluntarios jóvenes; Sin embargo, estas diferencias no fueron estadisticamente significativas.
SOBREDOSIS
diferencia de las sulfonilureas o la insulina, una sobredosis de PRECOSE no provocará hipoglucemia. Una sobredosis puede provocar aumentos transitorios de flatulencia, diarrea y molestias abdominales que desaparecen en breve. En caso de sobredosis, no se debe dar al paciente bebidas o comidas que contengan hidratos de carbono (polisacáridos, oligosacáridos y disacáridos) durante las próximas 4 a 6 horas.
CONTRAINDICACIONES
PRECOSE 25 mg está contraindicado en pacientes con hipersensibilidad conocida al fármaco. Precose 25 mg está contraindicado en pacientes con cetoacidosis diabética o cirrosis. PRECOSE 25 mg también está contraindicado en pacientes con enfermedad inflamatoria intestinal, ulceración colónica, obstrucción intestinal parcial o en pacientes predispuestos a la obstrucción intestinal. Además, PRECOSE está contraindicado en pacientes que tienen enfermedades intestinales crónicas asociadas con trastornos marcados de la digestión o absorción y en pacientes que tienen condiciones que pueden empeorar como resultado de una mayor formación de gases en el intestino.
FARMACOLOGÍA CLÍNICA
La acarbosa es un oligosacárido complejo que retrasa la digestión de los carbohidratos ingeridos, lo que resulta en un aumento menor de la concentración de glucosa en sangre después de las comidas. Como consecuencia de la reducción de la glucosa plasmática, PRECOSE reduce los niveles de hemoglobina glicosilada en pacientes con diabetes mellitus tipo 2. La glicosilación sistémica de proteínas no enzimáticas, como se refleja en los niveles de hemoglobina glicosilada, es una función de la concentración promedio de glucosa en sangre a lo largo del tiempo.
Mecanismo de acción
diferencia de las sulfonilureas, PRECOSE 50 mg no aumenta la secreción de insulina. La acción antihiperglucémica de la acarbosa resulta de una inhibición competitiva y reversible de la alfa-amilasa pancreática y de las enzimas alfa-glucósido hidrolasa intestinal unidas a la membrana. La alfa-amilasa pancreática hidroliza almidones complejos a oligosacáridos en la luz del intestino delgado, mientras que las alfa-glucosidasas intestinales unidas a la membrana hidrolizan oligosacáridos, trisacáridos y disacáridos a glucosa y otros monosacáridos en el borde en cepillo del intestino delgado. En pacientes diabéticos, esta inhibición de la enzima da como resultado un retraso en la absorción de glucosa y una disminución de la hiperglucemia posprandial.
Debido a que su mecanismo de acción es diferente, el efecto de PRECOSE para mejorar el control glucémico es aditivo al de las sulfonilureas, la insulina o la metformina cuando se usan en combinación. Además, PRECOSE 50mg disminuye los efectos insulinotrópicos y de aumento de peso de las sulfonilureas.
La acarbosa no tiene actividad inhibitoria contra la lactasa y, por lo tanto, no se esperaría que indujera intolerancia a la lactosa.
Farmacocinética
Absorción
En un estudio de 6 hombres sanos, se absorbió menos del 2 % de una dosis oral de acarbosa como fármaco activo, mientras que se absorbió aproximadamente el 35 % de la radiactividad total de una dosis oral marcada con 14C. Un promedio del 51 % de una dosis oral se excretó en las heces como radiactividad relacionada con el fármaco no absorbida dentro de las 96 horas posteriores a la ingestión. Debido a que la acarbosa actúa localmente dentro del tracto gastrointestinal, se desea terapéuticamente esta baja biodisponibilidad sistémica del compuesto original. Después de la administración oral de acarbosa marcada con 14C a voluntarios sanos, las concentraciones plasmáticas máximas de radiactividad se alcanzaron entre 14 y 24 horas después de la administración, mientras que las concentraciones plasmáticas máximas del fármaco activo se alcanzaron aproximadamente 1 hora. La absorción retardada de la radiactividad relacionada con la acarbosa refleja la absorción de metabolitos que pueden formarse por bacterias intestinales o hidrólisis enzimática intestinal.
Metabolismo
La acarbosa se metaboliza exclusivamente en el tracto gastrointestinal, principalmente por bacterias intestinales, pero también por enzimas digestivas. Una fracción de estos metabolitos (aproximadamente el 34% de la dosis) fue absorbida y posteriormente excretada en la orina. Al menos 13 metabolitos se han separado cromatográficamente de muestras de orina. Los principales metabolitos se han identificado como derivados del 4-metilpirogalol (es decir, conjugados de sulfato, metilo y glucurónido). Un metabolito (formado por la escisión de una molécula de glucosa a partir de acarbosa) también tiene actividad inhibidora de alfa-glucosidasa. Este metabolito, junto con el compuesto original, recuperado de la orina, representa menos del 2 % de la dosis total administrada.
Excreción
La fracción de acarbosa que se absorbe como fármaco intacto se excreta casi por completo por vía renal. Cuando se administró acarbosa por vía intravenosa, el 89 % de la dosis se recuperó en la orina como fármaco activo en 48 horas. Por el contrario, menos del 2 % de una dosis oral se recuperó en la orina como fármaco activo (es decir, compuesto original y metabolito activo). Esto es consistente con la baja biodisponibilidad del fármaco original. La vida media de eliminación plasmática de la actividad de la acarbosa es de aproximadamente 2 horas en voluntarios sanos. En consecuencia, la acumulación del fármaco no se produce con la dosificación oral tres veces al día (tres veces al día).
Poblaciones Especiales
El área media en estado estacionario bajo la curva (AUC) y las concentraciones máximas de acarbosa fueron aproximadamente 1,5 veces mayores en los voluntarios de edad avanzada que en los voluntarios jóvenes; Sin embargo, estas diferencias no fueron estadisticamente significativas. Los pacientes con insuficiencia renal grave (Clcr
Interacciones fármaco-fármaco
Los estudios en voluntarios sanos han demostrado que PRECOSE no tiene ningún efecto sobre la farmacocinética o la farmacodinámica de la nifedipina, el propranolol o la ranitidina. PRECOSE no interfirió con la absorción o disposición de la sulfonilurea gliburida en pacientes diabéticos. PRECOSE puede afectar la biodisponibilidad de la digoxina y puede requerir un ajuste de la dosis de digoxina en un 16 % (intervalo de confianza del 90 %: 8-23 %), disminuir la Cmáx media de digoxina en un 26 % (intervalo de confianza del 90 %: 16-34 %) y disminuir el valle medio concentraciones de digoxina en un 9 % (límite de confianza del 90 %: disminución del 19 % a aumento del 2 %). (Ver PRECAUCIONES: INTERACCIONES CON LA DROGAS .)
La cantidad de metformina absorbida mientras se tomaba PRECOSE era bioequivalente a la cantidad absorbida cuando se tomaba un placebo, según lo indicado por los valores de AUC en plasma. Sin embargo, el nivel plasmático máximo de metformina se redujo en aproximadamente un 20 % al tomar PRECOSE debido a un ligero retraso en la absorción de metformina. Hay poca o ninguna interacción clínicamente significativa entre PRECOSE y metformina.
Ensayos clínicos
Experiencia clínica de estudios de búsqueda de dosis en pacientes con diabetes mellitus tipo 2 que solo reciben tratamiento dietético
Se combinaron los resultados de seis estudios controlados de monoterapia de dosis fija de PRECOSE en el tratamiento de la diabetes mellitus tipo 2, en los que participaron 769 pacientes tratados con PRECOSE, y se calculó un promedio ponderado de la diferencia con respecto al placebo en el cambio medio desde el inicio en la hemoglobina glicosilada ( HbA1c) se calculó para cada nivel de dosis como se presenta a continuación:
Aunque los estudios utilizaron una dosis máxima de 200 o 300 mg tres veces al día, la dosis máxima recomendada para pacientes 60 kg es de 100 mg tres veces al día
Los resultados de estos seis estudios de monoterapia de dosis fija también se combinaron para obtener un promedio ponderado de la diferencia con respecto al placebo en el cambio medio desde el inicio para los niveles de glucosa en plasma posprandiales de una hora, como se muestra en la siguiente figura:
Figura 1 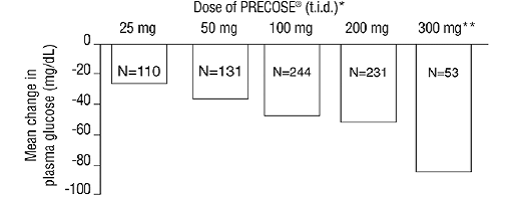
Experiencia Clínica en Pacientes con Diabetes Mellitus Tipo 2 en Monoterapia, o en Combinación con Sulfonilureas, Metformina o Insulina
PRECOSE se estudió como monoterapia y como tratamiento combinado con sulfonilurea, metformina o tratamiento con insulina. Los efectos del tratamiento sobre los niveles de HbA1c y los niveles de glucosa posprandiales de una hora se resumen para cuatro estudios aleatorizados, doble ciego, controlados con placebo realizados en los Estados Unidos en las Tablas 2 y 3, respectivamente. Las diferencias de tratamiento a las que se restó el placebo, que se resumen a continuación, fueron estadísticamente significativas para ambas variables en todos estos estudios.
El estudio 1 (n=109) involucró a pacientes en tratamiento de base solo con dieta. El efecto medio de la adición de PRECOSE a la terapia dietética fue un cambio en la HbA1c de -0,78 % y una mejora de la glucosa posprandial de una hora de -74,4 mg/dl.
En el Estudio 2 (n=137), el efecto medio de la adición de PRECOSE 25 mg al tratamiento máximo con sulfonilureas fue un cambio en la HbA1c de -0,54 % y una mejora de la glucosa posprandial de una hora de -33,5 mg/dl.
En el Estudio 3 (n=147), el efecto medio de la adición de PRECOSE 50 mg al tratamiento máximo con metformina fue un cambio en la HbA1c de -0,65 % y una mejora de la glucosa posprandial a la hora de -34,3 mg/dL.
El estudio 4 (n=145) demostró que PRECOSE añadido a pacientes con tratamiento de base con insulina dio como resultado un cambio medio en HbA1c de -0,69 % y una mejora de la glucosa posprandial de una hora de -36,0 mg/dl.
En Canadá se llevó a cabo un estudio de un año de duración de PRECOSE como monoterapia o en combinación con sulfonilurea, metformina o tratamiento con insulina, en el que se incluyeron 316 pacientes en el análisis de eficacia principal (Figura 2). En los grupos de dieta, sulfonilureas y metformina, la disminución media de HbA1c producida por la adición de PRECOSE 50 mg fue estadísticamente significativa a los seis meses, y este efecto fue persistente al año. En los pacientes tratados con PRECOSE con insulina, hubo una reducción estadísticamente significativa en la HbA1c a los seis meses y una tendencia a la reducción al año.
Figura 2 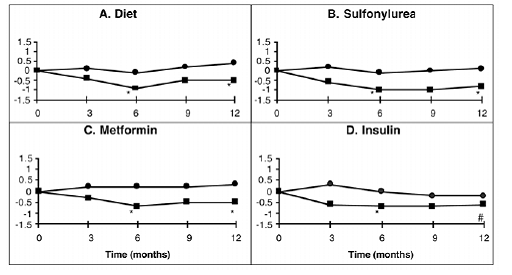
Figura 2: Efectos de PRECOSE (III) y Placebo (III) sobre el cambio medio en los niveles de HbA1c desde el inicio durante un estudio de un año en pacientes con diabetes mellitus tipo 2 cuando se usa en combinación con: (A) dieta sola; (B) sulfonilurea; (C) metformina; o (D) insulina. Se probaron las diferencias de tratamiento a los 6 y 12 meses: * p
INFORMACIÓN DEL PACIENTE
Se debe indicar a los pacientes que tomen PRECOSE 50 mg por vía oral tres veces al día al comienzo (con el primer bocado) de cada comida principal. Es importante que los pacientes continúen adhiriéndose a las instrucciones dietéticas, un programa de ejercicio regular y análisis regulares de glucosa en orina y/o sangre.
PRECOSE en sí mismo no causa hipoglucemia incluso cuando se administra a pacientes en ayunas. Sin embargo, las sulfonilureas y la insulina pueden reducir los niveles de azúcar en la sangre lo suficiente como para causar síntomas o, a veces, hipoglucemia potencialmente mortal. Debido a que PRECOSE administrado en combinación con una sulfonilurea o insulina causará una mayor disminución del azúcar en la sangre, puede aumentar el potencial hipoglucémico de estos agentes. La hipoglucemia no ocurre en pacientes que reciben metformina sola en las circunstancias habituales de uso, y no se observó un aumento en la incidencia de hipoglucemia en pacientes cuando se agregó PRECOSE a la terapia con metformina. El riesgo de hipoglucemia, sus síntomas y tratamiento, y las condiciones que predisponen a su desarrollo deben ser bien entendidos por los pacientes y familiares responsables. Debido a que PRECOSE 50 mg previene la descomposición del azúcar de mesa, los pacientes deben tener una fuente de glucosa fácilmente disponible (dextrosa, D-glucosa) para tratar los síntomas de niveles bajos de azúcar en la sangre cuando toman PRECOSE en combinación con una sulfonilurea o insulina.
Si se presentan efectos secundarios con PRECOSE, generalmente se desarrollan durante las primeras semanas de terapia. Por lo general, son efectos gastrointestinales de leves a moderados, como flatulencia, diarrea o molestias abdominales, y generalmente disminuyen en frecuencia e intensidad con el tiempo.
