Cartia XT 180mg Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Cartia y cómo se usa?
Cartia es un medicamento recetado que se usa para tratar los síntomas del dolor torácico (angina), la presión arterial alta (hipertensión), la taquicardia supraventricular paroxística y la fibrilación auricular (aleteo). Cartia se puede usar solo o con otros medicamentos.
Cartia pertenece a una clase de medicamentos llamados antiarrítmicos, IV; Bloqueadores de los canales de calcio; Bloqueadores de canales de calcio, no dihidropiridínicos.
¿Cuáles son los posibles efectos secundarios de Cartia?
Cartia puede causar efectos secundarios graves que incluyen:
- Dolor de pecho,
- latidos lentos del corazón,
- latidos del corazón palpitantes,
- revoloteando en tu pecho,
- aturdimiento,
- hinchazón,
- rápido aumento de peso,
- dificultad para respirar,
- fiebre,
- dolor de garganta,
- ojos irritados,
- dolor de piel, y
- erupción cutánea roja o morada con ampollas y descamación
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Cartia incluyen:
- leve dolor de cabeza,
- mareos leves y
- síntomas de resfriado (nariz tapada, estornudos, dolor de garganta)
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Cartia. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
DESCRIPCIÓN
El clorhidrato de diltiazem es un inhibidor del flujo celular de iones de calcio (bloqueador de canales lentos o antagonista del calcio). Químicamente, el clorhidrato de diltiazem es 1,5-benzotiazepin-4(5H)ona,3-(acetiloxi)-5-[2-(dimetilamino)etil]-2, 3-dihidro-2-(4-metoxifenil)-, monoclorhidrato ,(+)-cis-. La estructura química es:
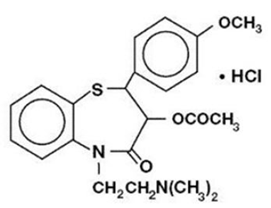
El clorhidrato de diltiazem es un polvo cristalino de color blanco a blanquecino con sabor amargo. Es soluble en agua, metanol y cloroformo. Tiene un peso molecular de 450,98. La cápsula de liberación prolongada de clorhidrato de diltiazem (una dosis diaria) está formulada como una cápsula de liberación prolongada que se toma una vez al día y contiene 120 mg, 180 mg, 240 mg o 300 mg de clorhidrato de diltiazem.
Además, cada cápsula contiene los siguientes ingredientes inactivos: citrato de acetiltributilo, copolímero de metacrilato de amonio-NF, D & C Red #28, D & C Yellow #10, D & C Yellow #10 Aluminium Lake, etilcelulosa, FD & C Blue #1 Laca de aluminio, FD & C Blue #2 Laca de aluminio, FD & C Red #40, FD & C Red #40 Laca de aluminio, gelatina-NF, estearato de magnesio, copolímero de ácido metacrílico-NF, propilenglicol, polisorbato 80-NF, almidón , sacarosa, talco USP y dióxido de titanio. Las cápsulas de 180 mg y 240 mg contienen óxido de hierro amarillo. Además, la cápsula de 240 mg también contiene óxido de hierro negro y óxido de hierro rojo.
Para administración oral.
Este medicamento cumple con la Liberación de Medicamentos 9 de la USP.
INDICACIONES
Las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) están indicadas para el tratamiento de la hipertensión. Puede usarse solo o en combinación con otros medicamentos antihipertensivos.
Las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) están indicadas para el tratamiento de la angina estable crónica y la angina debida a espasmo de la arteria coronaria.
DOSIFICACIÓN Y ADMINISTRACIÓN
Los pacientes controlados con diltiazem solo o en combinación con otros medicamentos pueden cambiar a cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis una vez al día) a la dosis diaria total equivalente más cercana. Algunos pacientes pueden necesitar dosis más altas de cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día). Los pacientes deben ser monitoreados de cerca. Puede ser necesaria una titulación posterior a dosis más altas o más bajas y debe iniciarse según se justifique clínicamente. Existe una experiencia clínica general limitada con dosis superiores a 360 mg, pero se han estudiado dosis de hasta 540 mg en ensayos clínicos. La incidencia de efectos secundarios aumenta a medida que aumenta la dosis, siendo el bloqueo AV de primer grado, los mareos y la bradicardia sinusal los que tienen la mayor relación con la dosis.
Hipertensión
La dosis debe ajustarse mediante titulación a las necesidades individuales del paciente. Cuando se usa como monoterapia, las dosis iniciales razonables son de 180 a 240 mg una vez al día, aunque algunos pacientes pueden responder a dosis más bajas. El efecto antihipertensivo máximo generalmente se observa a los 14 días de terapia crónica; por lo tanto, los ajustes de dosis deben programarse en consecuencia. El rango de dosificación habitual estudiado en los ensayos clínicos fue de 240 a 360 mg una vez al día. Los pacientes individuales pueden responder a dosis más altas de hasta 480 mg una vez al día.
Angina de pecho
Las dosis para el tratamiento de la angina deben ajustarse a las necesidades de cada paciente, comenzando con una dosis de 120 o 180 mg una vez al día. Los pacientes individuales pueden responder a dosis más altas de hasta 480 mg una vez al día. Cuando sea necesario, la titulación se puede realizar durante un período de 7 a 14 días.
Clorhidrato de diltiazem Cápsulas de liberación prolongada USP (Dosificación una vez al día)
Uso concomitante con otros agentes cardiovasculares
CÓMO SUMINISTRADO
NOTA: EL PRODUCTO PUEDE TENER OLOR.
Condiciones de almacenaje
Almacenar a 20° a 25°C (68° a 77°F) [Ver Temperatura ambiente controlada por USP ].
Evite la humedad excesiva.
Dispense en un recipiente hermético resistente a la luz como se define en la USP.
Fabricado por: Actavis Laboratories FL, Inc., Fort Lauderdale, FL 33314 EE. UU. Distribuido por: Actavis Pharma, Inc., Parsippany, NJ 07054 EE. UU. Revisado: diciembre de 2014
EFECTOS SECUNDARIOS
Las reacciones adversas graves han sido raras en los estudios realizados hasta la fecha, pero debe reconocerse que los pacientes con función ventricular alterada y anomalías de la conducción cardíaca generalmente se han excluido de estos estudios.
La siguiente tabla presenta las reacciones adversas más comunes informadas en ensayos de angina e hipertensión controlados con placebo en pacientes que recibieron diltiazem clorhidrato en cápsulas de liberación prolongada (dosificación una vez al día) hasta 360 mg con tasas en pacientes con placebo que se muestran para comparación.
Cápsula de liberación prolongada de clorhidrato de diltiazem (una vez al día) Ensayos combinados de angina e hipertensión controlados con placebo
En ensayos clínicos de cápsulas de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día), tabletas de clorhidrato de diltiazem y cápsulas de liberación prolongada de clorhidrato de diltiazem que involucraron a más de 3200 pacientes, los eventos más comunes (es decir, más del 1%) fueron edema (4.6%) , cefalea (4,6 %), mareos (3,5 %), astenia (2,6 %), bloqueo AV de primer grado (2,4 %), bradicardia (1,7 %), sofocos (1,4 %), náuseas (1,4 %) y erupción cutánea ( 1,2%).
Además, los siguientes eventos se informaron con poca frecuencia (menos del 1 %) en los ensayos de angina o hipertensión:
Cardiovascular: Angina, arritmia, bloqueo AV (segundo o tercer grado), bloqueo de rama, insuficiencia cardíaca congestiva, anomalías en el ECG, hipotensión, palpitaciones, síncope, taquicardia, extrasístoles ventriculares.
Sistema nervioso: Sueños anormales, amnesia, depresión, alteración de la marcha, alucinaciones, insomnio, nerviosismo, parestesia, cambios de personalidad, somnolencia, tinnitus, temblor.
Gastrointestinal: Anorexia, estreñimiento, diarrea, boca seca, disgeusia, dispepsia, elevaciones leves de SGOT, SGPT, LDH y fosfatasa alcalina (ver ADVERTENCIAS , Lesión hepática aguda ), sed, vómitos, aumento de peso.
Dermatológico: Petequias, fotosensibilidad, prurito, urticaria.
Otro: Ambliopía, aumento de CPK, disnea, epistaxis, irritación ocular, hiperglucemia, hiperuricemia, impotencia, calambres musculares, congestión nasal, nocturia, dolor osteoarticular, poliuria, dificultades sexuales.
Los siguientes eventos posteriores a la comercialización se informaron con poca frecuencia en pacientes que recibieron diltiazem: pustulosis exantemática generalizada aguda, reacciones alérgicas, alopecia, angioedema (incluido edema facial o periorbitario), asistolia, eritema multiforme (incluido el síndrome de Stevens-Johnson, necrólisis epidérmica tóxica), dermatitis exfoliativa , síntomas extrapiramidales, hiperplasia gingival, anemia hemolítica, aumento del tiempo de sangrado, leucopenia, fotosensibilidad (incluyendo queratosis liquenoide e hiperpigmentación en áreas de la piel expuestas al sol), púrpura, retinopatía, miopatía y trombocitopenia. Además, se han observado eventos como infarto de miocardio que no son fácilmente distinguibles de la historia natural de la enfermedad en estos pacientes. Se han notificado varios casos bien documentados de exantema generalizado, algunos caracterizados como vasculitis leucocitoclástica. Sin embargo, aún no se ha establecido una relación definitiva de causa y efecto entre estos eventos y la terapia con diltiazem.
Para informar SOSPECHAS DE REACCIONES ADVERSAS, comuníquese con Actavis al 1-800-272-5525 o con la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch.
INTERACCIONES CON LA DROGAS
Debido al potencial de efectos aditivos, se justifica la precaución y la titulación cuidadosa en pacientes que reciben diltiazem concomitantemente con otros agentes que se sabe que afectan la contractilidad y/o la conducción cardíacas (ver ADVERTENCIAS ). Los estudios farmacológicos indican que puede haber efectos aditivos en la prolongación de la conducción AV cuando se usan betabloqueantes o digitálicos concomitantemente con diltiazem (ver ADVERTENCIAS ).
Al igual que con todos los medicamentos, se debe tener cuidado al tratar a pacientes con múltiples medicamentos. Diltiazem es tanto un sustrato como un inhibidor del sistema enzimático citocromo P-450 3A4. Otros fármacos que son sustratos, inhibidores o inductores específicos de este sistema enzimático pueden tener un impacto significativo en la eficacia y el perfil de efectos secundarios del diltiazem. Los pacientes que toman otros medicamentos que son sustratos de CYP450 3A4, especialmente los pacientes con insuficiencia renal y/o hepática, pueden requerir un ajuste de la dosis al comenzar o interrumpir la administración concomitante de diltiazem para mantener los niveles sanguíneos terapéuticos óptimos.
anestésicos
Los bloqueadores de los canales de calcio pueden potenciar la depresión de la contractilidad, la conductividad y el automatismo cardíacos, así como la dilatación vascular asociada con los anestésicos. Cuando se usan concomitantemente, los anestésicos y los bloqueadores de calcio deben titularse cuidadosamente.
Benzodiazepinas
Los estudios demostraron que el diltiazem aumentó el AUC del midazolam y el triazolam de 3 a 4 veces y la Cmax de 2 veces, en comparación con el placebo. La vida media de eliminación de midazolam y triazolam también aumentó (1,5 a 2,5 veces) durante la administración concomitante con diltiazem. Estos efectos farmacocinéticos observados durante la coadministración de diltiazem pueden resultar en un aumento de los efectos clínicos (p. ej., sedación prolongada) tanto del midazolam como del triazolam.
Bloqueadores beta
Los estudios domésticos controlados y no controlados sugieren que el uso concomitante de diltiazem y betabloqueantes generalmente se tolera bien, pero los datos disponibles no son suficientes para predecir los efectos del tratamiento concomitante en pacientes con disfunción ventricular izquierda o anomalías de la conducción cardíaca.
La administración de clorhidrato de diltiazem concomitantemente con propranolol en cinco voluntarios normales resultó en un aumento de los niveles de propranolol en todos los sujetos y la biodisponibilidad de propranolol aumentó aproximadamente un 50%. In vitro, el propranolol parece ser desplazado de sus sitios de unión por el diltiazem. Si se inicia o suspende la terapia combinada junto con propranolol, puede estar justificado un ajuste en la dosis de propranolol (ver ADVERTENCIAS ).
buspirona
En nueve sujetos sanos, el diltiazem aumentó significativamente el AUC medio de la buspirona en 5,5 veces y la Cmax en 4,1 veces en comparación con el placebo. La T½ y Tmax de buspirona no se vieron significativamente afectadas por diltiazem. Los efectos potenciados y el aumento de la toxicidad de la buspirona pueden ser posibles durante la administración concomitante con diltiazem. Pueden ser necesarios ajustes posteriores de la dosis durante la coadministración, y deben basarse en la evaluación clínica.
Carbamazepina
Se ha informado que la administración concomitante de diltiazem con carbamazepina da como resultado niveles séricos elevados de carbamazepina (40% a 72% de aumento), lo que resulta en toxicidad en algunos casos. Los pacientes que reciben estos medicamentos al mismo tiempo deben ser monitoreados por posibles interacciones medicamentosas.
cimetidina
Un estudio en seis voluntarios sanos mostró un aumento significativo en los niveles plasmáticos máximos de diltiazem (58 %) y el área bajo la curva (53 %) después de un curso de 1 semana de cimetidina a 1200 mg por día y una dosis única de diltiazem 60 mg. La ranitidina produjo aumentos más pequeños y no significativos. El efecto puede estar mediado por la inhibición conocida de la cimetidina del citocromo P-450 hepático, el sistema enzimático responsable del metabolismo de primer paso del diltiazem. Los pacientes que actualmente reciben terapia con diltiazem deben ser monitoreados cuidadosamente para detectar un cambio en el efecto farmacológico al iniciar y suspender la terapia con cimetidina. Puede estar justificado un ajuste en la dosis de diltiazem.
clonidina
Se ha informado bradicardia sinusal que resultó en hospitalización e inserción de marcapasos en asociación con el uso de clonidina junto con diltiazem. Monitoree la frecuencia cardíaca en pacientes que reciben diltiazem y clonidina concomitantemente.
ciclosporina
Se ha observado una interacción farmacocinética entre diltiazem y ciclosporina durante estudios en pacientes con trasplante renal y cardíaco. En los receptores de trasplantes renales y cardíacos, fue necesaria una reducción de la dosis de ciclosporina que osciló entre el 15 % y el 48 % para mantener las concentraciones mínimas de ciclosporina similares a las observadas antes de la adición de diltiazem. Si estos agentes se van a administrar concurrentemente, se deben monitorear las concentraciones de ciclosporina, especialmente cuando se inicia, ajusta o suspende la terapia con diltiazem.
No se ha evaluado el efecto de la ciclosporina sobre las concentraciones plasmáticas de diltiazem.
Digital
La administración de diltiazem con digoxina en 24 varones sanos aumentó las concentraciones plasmáticas de digoxina en aproximadamente un 20 %. Otro investigador no encontró un aumento en los niveles de digoxina en 12 pacientes con enfermedad arterial coronaria. Debido a que ha habido resultados contradictorios con respecto al efecto de los niveles de digoxina, se recomienda monitorear los niveles de digoxina al iniciar, ajustar y suspender la terapia con diltiazem para evitar una posible digitalización excesiva o insuficiente (ver ADVERTENCIAS ).
quinidina
Diltiazem aumenta significativamente el AUC(0-→) de la quinidina en un 51%, T½ en un 36% y disminuye su CL oral en un 33%. Puede estar justificado el control de los efectos adversos de la quinidina y ajustar la dosis en consecuencia.
rifampicina
La coadministración de rifampicina con diltiazem redujo las concentraciones plasmáticas de diltiazem a niveles indetectables. Cuando sea posible, debe evitarse la coadministración de diltiazem con rifampicina o cualquier inductor conocido de CYP3A4 y debe considerarse una terapia alternativa.
estatinas
Diltiazem es un inhibidor de CYP3A4 y se ha demostrado que aumenta significativamente el AUC de algunas estatinas. El riesgo de miopatía y rabdomiólisis con estatinas metabolizadas por CYP3A4 puede aumentar con el uso concomitante de diltiazem. Cuando sea posible, use una estatina no metabolizada por CYP3A4 junto con diltiazem; de lo contrario, se deben considerar los ajustes de dosis tanto para el diltiazem como para la estatina junto con un control estricto de los signos y síntomas de cualquier evento adverso relacionado con la estatina.
En un estudio cruzado con voluntarios sanos (N = 10), la coadministración de una dosis única de 20 mg de simvastatina al final de un régimen de 14 días con 120 mg dos veces al día de diltiazem SR resultó en un aumento de 5 veces en el AUC medio de simvastatina versus simvastatina solo. Los sujetos con una mayor exposición promedio en estado estacionario a diltiazem mostraron un mayor aumento en la exposición a simvastatina. Las simulaciones basadas en computadora mostraron que con una dosis diaria de 480 mg de diltiazem, se puede esperar un aumento promedio de 8 a 9 veces en el AUC de simvastatina. Si se requiere la coadministración de simvastatina con diltiazem, limite las dosis diarias de simvastatina a 10 mg y de diltiazem a 240 mg.
En un estudio cruzado de 4 vías, aleatorizado, abierto, de diez sujetos, la coadministración de diltiazem (120 mg dos veces al día de diltiazem SR durante 2 semanas) con una dosis única de 20 mg de lovastatina resultó en un aumento de 3 a 4 veces en la media AUC de lovastatina y versus lovastatina sola. En el mismo estudio, no hubo cambios significativos en el AUC de pravastatina en dosis única de 20 mg y durante la coadministración de diltiazem. Los niveles plasmáticos de diltiazem no se vieron afectados significativamente por lovastatina o pravastatina.
ADVERTENCIAS
Conducción cardíaca
Diltiazem prolonga los períodos refractarios del nódulo AV sin prolongar significativamente el tiempo de recuperación del nódulo sinusal, excepto en pacientes con síndrome del seno enfermo. En raras ocasiones, este efecto puede resultar en frecuencias cardíacas anormalmente lentas (particularmente en pacientes con síndrome del seno enfermo) o bloqueo AV de segundo o tercer grado (13 de 3290 pacientes o 0,40%). El uso concomitante de diltiazem con bloqueadores beta o digitálicos puede provocar efectos aditivos en la conducción cardíaca. Un paciente con angina de Prinzmetal desarrolló periodos de asistolia (2 a 5 segundos) después de una dosis única de 60 mg de diltiazem (ver REACCIONES ADVERSAS ).
Insuficiencia cardíaca congestiva
Aunque diltiazem tiene un efecto inotrópico negativo en preparaciones de tejido animal aislado, los estudios hemodinámicos en humanos con función ventricular normal no han mostrado una reducción en el índice cardíaco ni efectos negativos consistentes sobre la contractilidad (dp/dt). Un estudio agudo de diltiazem oral en pacientes con función ventricular alterada (fracción de eyección 24% ± 6%) mostró una mejoría en los índices de función ventricular sin una disminución significativa en la función contráctil (dp/dt). Se ha informado empeoramiento de la insuficiencia cardíaca congestiva en pacientes con deterioro preexistente de la función ventricular. La experiencia con el uso de clorhidrato de diltiazem en combinación con bloqueadores beta en pacientes con insuficiencia ventricular es limitada. Se debe tener precaución al usar esta combinación.
Hipotensión
Las disminuciones en la presión arterial asociadas con la terapia con diltiazem pueden ocasionalmente resultar en hipotensión sintomática.
Lesión hepática aguda
En estudios clínicos se han observado elevaciones leves de las transaminasas con y sin elevación concomitante de la fosfatasa alcalina y la bilirrubina. Tales elevaciones fueron generalmente transitorias y con frecuencia se resolvieron incluso con el tratamiento continuo con diltiazem. En raras ocasiones, se han observado elevaciones significativas de enzimas como la fosfatasa alcalina, LDH, SGOT, SGPT y otros fenómenos compatibles con lesión hepática aguda. Estas reacciones tendieron a ocurrir temprano después del inicio de la terapia (1 a 8 semanas) y han sido reversibles al suspender la terapia con medicamentos. La relación con el diltiazem es incierta en algunos casos, pero probable en algunos (ver PRECAUCIONES ).
PRECAUCIONES
General
El clorhidrato de diltiazem se metaboliza ampliamente en el hígado y se excreta por los riñones y la bilis. Como con cualquier fármaco administrado durante períodos prolongados, los parámetros de laboratorio de la función renal y hepática deben controlarse a intervalos regulares. El medicamento debe usarse con precaución en pacientes con insuficiencia renal o hepática. En estudios subagudos y crónicos en perros y ratas diseñados para producir toxicidad, las dosis altas de diltiazem se asociaron con daño hepático. En estudios hepáticos subagudos especiales, las dosis orales de 125 mg/kg y superiores en ratas se asociaron con cambios histológicos en el hígado, que fueron reversibles cuando se suspendió el fármaco. En perros, las dosis de 20 mg/kg también se asociaron con cambios hepáticos; sin embargo, estos cambios fueron reversibles con la dosificación continua.
Eventos dermatológicos (ver REACCIONES ADVERSAS puede ser transitorio y puede desaparecer a pesar del uso continuado de diltiazem. Sin embargo, también se han informado con poca frecuencia erupciones cutáneas que progresan a eritema multiforme y/o dermatitis exfoliativa. Si persiste una reacción dermatológica, el medicamento debe suspenderse.
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
Un estudio de 24 meses en ratas con dosis orales de hasta 100 mg/kg/día y un estudio de 21 meses en ratones con dosis orales de hasta 30 mg/kg/día no mostró evidencia de carcinogenicidad. Tampoco hubo respuesta mutagénica in vitro o in vivo en ensayos de células de mamífero o in vitro en bacterias. No se observó evidencia de alteración de la fertilidad en un estudio realizado en ratas macho y hembra con dosis orales de hasta 100 mg/kg/día.
El embarazo
Categoría C. Se han realizado estudios de reproducción en ratones, ratas y conejos. La administración de dosis que oscilan entre cinco y diez veces más (sobre una base de mg/kg) que la dosis terapéutica diaria recomendada ha resultado en letalidad embrionaria y fetal. Se ha informado que estas dosis, en algunos estudios, causan anomalías esqueléticas. En los estudios perinatales/postnatales, hubo un aumento en la incidencia de mortinatos con dosis 20 veces superiores a la dosis humana o más.
No hay estudios bien controlados en mujeres embarazadas; por lo tanto, use diltiazem en mujeres embarazadas solo si el beneficio potencial justifica el riesgo potencial para el feto.
Madres lactantes
Diltiazem se excreta en la leche humana. Un informe sugiere que las concentraciones en la leche materna pueden aproximarse a los niveles séricos. Si se considera esencial el uso de diltiazem, se debe instituir un método alternativo de alimentación infantil.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos.
Uso geriátrico
Los estudios clínicos de diltiazem no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. Otra experiencia clínica informada no ha identificado diferencias en las respuestas entre los ancianos y los pacientes más jóvenes. En general, la selección de la dosis para un paciente de edad avanzada debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedades concomitantes u otra terapia con medicamentos.
SOBREDOSIS
Las DL50 orales en ratones y ratas oscilan entre 415 y 740 mg/kg y entre 560 y 810 mg/kg, respectivamente. Las DL50 intravenosas en estas especies fueron de 60 y 38 mg/kg, respectivamente. Se considera que la LD50 oral en perros supera los 50 mg/kg, mientras que la letalidad se observó en monos a 360 mg/kg.
Se desconoce la dosis tóxica en el hombre. Debido al extenso metabolismo, los niveles en sangre después de una dosis estándar de diltiazem pueden variar más de diez veces, lo que limita la utilidad de los niveles en sangre en casos de sobredosis.
Ha habido informes de sobredosis de diltiazem en cantidades que oscilan entre
Los eventos observados después de una sobredosis de diltiazem incluyeron bradicardia, hipotensión, bloqueo cardíaco e insuficiencia cardíaca. La mayoría de los informes de sobredosis describieron alguna medida médica de apoyo y/o tratamiento farmacológico. La bradicardia respondió favorablemente con frecuencia a la atropina, al igual que el bloqueo cardíaco, aunque también se utilizó con frecuencia la estimulación cardíaca para tratar el bloqueo cardíaco. Se utilizaron líquidos y vasopresores para mantener la presión arterial y, en los casos de insuficiencia cardíaca, se administraron agentes inotrópicos. Además, algunos pacientes recibieron tratamiento con soporte ventilatorio, lavado gástrico, carbón activado y/o calcio intravenoso.
La efectividad de la administración intravenosa de calcio para revertir los efectos farmacológicos de la sobredosis de diltiazem ha sido inconsistente. En unos pocos casos informados, la sobredosis con bloqueadores de los canales de calcio asociada con hipotensión y bradicardia que inicialmente era refractaria a la atropina se volvió más sensible a la atropina después de que los pacientes recibieron calcio intravenoso. En algunos casos, se ha administrado calcio intravenoso (1 g de cloruro de calcio o 3 g de gluconato de calcio) durante 5 minutos y se repite cada 10 a 20 minutos según sea necesario. También se ha administrado gluconato de calcio en infusión continua a razón de 2 g por hora durante 10 horas. Pueden ser necesarias infusiones de calcio durante 24 horas o más. Los pacientes deben ser monitoreados para detectar signos de hipercalcemia.
En caso de sobredosis o respuesta exagerada, se deben emplear medidas de apoyo adecuadas además de la descontaminación gastrointestinal. Diltiazem no parece ser eliminado por vía peritoneal o hemodiálisis. Los datos limitados sugieren que la plasmaféresis o la hemoperfusión con carbón pueden acelerar la eliminación de diltiazem después de una sobredosis. Según los efectos farmacológicos conocidos del diltiazem y/o las experiencias clínicas notificadas, se pueden considerar las siguientes medidas:
Bradicardia: Administrar atropina (0,6 a 1 mg). Si no hay respuesta al bloqueo vagal, administre isoproterenol con precaución.
Bloqueo AV de alto grado: Tratar como para la bradicardia anterior. El bloqueo AV fijo de alto grado debe tratarse con marcapasos cardíaco.
Falla cardiaca: Administrar agentes inotrópicos (isoproterenol, dopamina o dobutamina) y diuréticos.
Hipotensión: Vasopresores (p. ej., dopamina o norepinefrina).
El tratamiento y la dosis reales deben depender de la gravedad de la situación clínica y del juicio y experiencia del médico tratante.
CONTRAINDICACIONES
Diltiazem está contraindicado en (1) pacientes con síndrome del seno enfermo excepto en presencia de un marcapasos ventricular en funcionamiento, (2) pacientes con bloqueo AV de segundo o tercer grado excepto en presencia de un marcapasos ventricular en funcionamiento, (3) pacientes con hipotensión (menos de 90 mm Hg sistólica), (4) pacientes que han demostrado hipersensibilidad al fármaco y (5) pacientes con infarto agudo de miocardio y congestión pulmonar documentada por rayos X al ingreso.
FARMACOLOGÍA CLÍNICA
Se cree que los efectos terapéuticos de las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) están relacionados con su capacidad para inhibir la entrada celular de iones de calcio durante la despolarización de la membrana del músculo liso cardíaco y vascular.
Mecanismos de acción
Hipertensión
Las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) producen su efecto antihipertensivo principalmente mediante la relajación del músculo liso vascular y la disminución resultante de la resistencia vascular periférica. La magnitud de la reducción de la presión arterial está relacionada con el grado de hipertensión; por lo tanto, los individuos hipertensos experimentan un efecto antihipertensivo, mientras que en los normotensos sólo hay una modesta caída de la presión arterial.
Angina de pecho
Se ha demostrado que las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) producen aumentos en la tolerancia al ejercicio, probablemente debido a su capacidad para reducir la demanda de oxígeno del miocardio. Esto se logra a través de reducciones en la frecuencia cardíaca y la presión arterial sistémica en cargas de trabajo máximas y submáximas. Se ha demostrado que el diltiazem es un potente dilatador de las arterias coronarias, tanto epicárdicas como subendocárdicas. El diltiazem inhibe el espasmo de la arteria coronaria espontáneo e inducido por ergonovina.
En modelos animales, el diltiazem interfiere con la corriente de entrada lenta (despolarizante) en el tejido excitable. Provoca desacoplamiento de excitación-contracción en varios tejidos miocárdicos sin cambios en la configuración del potencial de acción. El diltiazem produce relajación del músculo liso vascular coronario y dilatación de las arterias coronarias grandes y pequeñas a niveles de fármaco que causan poco o ningún efecto inotrópico negativo. Los aumentos resultantes en el flujo sanguíneo coronario (epicárdico y subendocárdico) ocurren en modelos isquémicos y no isquémicos y se acompañan de disminuciones dependientes de la dosis en la presión arterial sistémica y disminuciones en la resistencia periférica.
Efectos hemodinámicos y electrofisiológicos
Al igual que otros antagonistas de los canales de calcio, el diltiazem disminuye la conducción sinoauricular y auriculoventricular en tejidos aislados y tiene un efecto inotrópico negativo en preparaciones aisladas. En el animal intacto, se puede observar una prolongación del intervalo AH a dosis más altas.
En el hombre, el diltiazem previene el espasmo de la arteria coronaria espontáneo y provocado por la ergonovina. Provoca una disminución de la resistencia vascular periférica y una caída modesta de la presión arterial en individuos normotensos y, en estudios de tolerancia al ejercicio en pacientes con cardiopatía isquémica, reduce el producto frecuencia cardíaca-presión arterial para cualquier carga de trabajo dada. Los estudios realizados hasta la fecha, principalmente en pacientes con buena función ventricular, no han revelado evidencia de un efecto inotrópico negativo; el gasto cardíaco, la fracción de eyección y la presión diastólica final del ventrículo izquierdo no se han visto afectados. Dichos datos no tienen valor predictivo con respecto a los efectos en pacientes con función ventricular deficiente, y se ha informado un aumento de la insuficiencia cardíaca en pacientes con deterioro preexistente de la función ventricular. Todavía hay pocos datos sobre la interacción de diltiazem y betabloqueantes en pacientes con función ventricular deficiente. La frecuencia cardíaca en reposo suele reducirse ligeramente con el diltiazem.
En pacientes hipertensos, las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosificación una vez al día) producen efectos antihipertensivos tanto en posición supina como de pie. En un estudio doble ciego, paralelo, de respuesta a la dosis que utilizó dosis que oscilaron entre 90 y 540 mg una vez al día, la cápsula de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día) redujo la presión arterial diastólica en decúbito supino de manera aparentemente lineal durante todo el período. rango de dosis estudiado. Los cambios en la presión arterial diastólica, medidos en el punto mínimo, para el placebo, 90 mg, 180 mg, 360 mg y 540 mg fueron -2,9, -4,5, -6,1, -9,5 y -10,5 mm Hg, respectivamente. La hipotensión postural se observa con poca frecuencia al adoptar repentinamente una posición erguida. No hay taquicardia refleja asociada con los efectos antihipertensivos crónicos. Las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) disminuyen la resistencia vascular, aumentan el gasto cardíaco (al aumentar el volumen sistólico); y produce una ligera disminución o ningún cambio en la frecuencia cardíaca. Durante el ejercicio dinámico, se inhiben los aumentos de la presión diastólica, mientras que la presión sistólica máxima alcanzable suele reducirse. La terapia crónica con cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis de una vez al día) no produce cambios o un aumento en las catecolaminas plasmáticas. No se ha observado un aumento de la actividad del eje renina-angiotensina-aldosterona. Las cápsulas de liberación prolongada de clorhidrato de diltiazem USP (dosis una vez al día) reducen los efectos renales y periféricos de la angiotensina II. Los modelos animales hipertensos responden al diltiazem con reducciones en la presión arterial y aumento de la diuresis y natriuresis sin un cambio en la relación sodio/potasio urinario.
En un estudio de dosis-respuesta paralelo, doble ciego de dosis de 60 mg a 480 mg una vez al día, la cápsula de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día) aumentó el tiempo hasta la finalización del ejercicio de manera lineal en toda la dosis rango estudiado. La mejora en el tiempo hasta la finalización del ejercicio utilizando un protocolo de ejercicio de Bruce, medido en el punto mínimo, para placebo, 60 mg, 120 mg, 240 mg, 360 mg y 480 mg fue de 29, 40, 56, 51, 69 y 68 segundos , respectivamente. A medida que se aumentaron las dosis de la cápsula de liberación prolongada de clorhidrato de diltiazem (dosis de una vez al día), disminuyó la frecuencia general de la angina. Se administró una cápsula de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día), 180 mg una vez al día, o placebo en un estudio doble ciego a pacientes que recibían tratamiento concomitante con nitratos de acción prolongada y/o betabloqueantes. Se observó un aumento significativo en el tiempo hasta la terminación del ejercicio y una disminución significativa en la frecuencia general de la angina. En este ensayo, la frecuencia general de eventos adversos en el grupo de tratamiento con cápsulas de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día) fue la misma que en el grupo de placebo.
El diltiazem intravenoso en dosis de 20 mg prolonga el tiempo de conducción de la HA y los periodos refractarios funcionales y efectivos del nodo AV en aproximadamente un 20%. En un estudio que involucró dosis orales únicas de 300 mg de clorhidrato de diltiazem en seis voluntarios normales, la prolongación máxima promedio de PR fue del 14% sin casos de bloqueo AV mayor que el primer grado. La prolongación del intervalo AH asociada con diltiazem no es más pronunciada en pacientes con bloqueo cardíaco de primer grado. En pacientes con síndrome del seno enfermo, el diltiazem prolonga significativamente la duración del ciclo sinusal (hasta un 50% en algunos casos).
La administración oral crónica de clorhidrato de diltiazem a pacientes en dosis de hasta 540 mg/día ha resultado en pequeños aumentos en el intervalo PR y en ocasiones produce una prolongación anormal (ver ADVERTENCIAS ).
Farmacocinética y Metabolismo
El diltiazem se absorbe bien en el tracto gastrointestinal y está sujeto a un amplio efecto de primer paso, lo que proporciona una biodisponibilidad absoluta (en comparación con la administración intravenosa) de alrededor del 40 %. El diltiazem sufre un metabolismo extenso en el que solo del 2% al 4% del fármaco sin cambios aparece en la orina. Los fármacos que inducen o inhiben las enzimas microsomales hepáticas pueden alterar la disposición del diltiazem.
La medición de la radiactividad total después de la administración IV corta en voluntarios sanos sugiere la presencia de otros metabolitos no identificados, que alcanzan concentraciones más altas que las del diltiazem y se eliminan más lentamente; la vida media de la radiactividad total es de unas 20 horas en comparación con las 2 a 5 horas del diltiazem.
Los estudios de unión in vitro muestran que el diltiazem se une en un 70 % a un 80 % a las proteínas plasmáticas. Los estudios competitivos de unión de ligandos in vitro también han demostrado que la unión de diltiazem no se ve alterada por concentraciones terapéuticas de digoxina, hidroclorotiazida, fenilbutazona, propranolol, ácido salicílico o warfarina. La vida media de eliminación plasmática luego de la administración de una o varias drogas es de aproximadamente 3,0 a 4,5 horas. El desacetil diltiazem también está presente en el plasma a niveles del 10% al 20% del fármaco original y es del 25% al 50% tan potente como vasodilatador coronario como el diltiazem. Las concentraciones mínimas terapéuticas de diltiazem en plasma parecen estar en el rango de 50 a 200 ng/mL. Hay una desviación de la linealidad cuando se aumentan las dosis; la vida media aumenta ligeramente con la dosis. Un estudio que comparó a pacientes con función hepática normal con pacientes con cirrosis encontró un aumento en la vida media y un aumento del 69 % en la biodisponibilidad en los pacientes con insuficiencia hepática. Un solo estudio en nueve pacientes con insuficiencia renal grave no mostró diferencias en el perfil farmacocinético de diltiazem en comparación con pacientes con función renal normal.
Cápsulas de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día)
Cuando se compara con un régimen de tabletas de diltiazem en estado estacionario, más del 95% del fármaco se absorbe de la formulación de cápsulas de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día). Una sola dosis de 360 mg de la cápsula produce niveles plasmáticos detectables en 2 horas y niveles plasmáticos máximos entre 10 y 14 horas; la absorción se produce a lo largo del intervalo de dosificación. Cuando se coadministró la cápsula de liberación prolongada de clorhidrato de diltiazem (dosis de una vez al día) con un desayuno con alto contenido de grasa, el grado de absorción de diltiazem no se vio afectado. No se produce vertido de dosis. La vida media de eliminación aparente después de una dosis única o múltiple es de 5 a 8 horas. Se observa una desviación de la linealidad similar a la observada con las tabletas de diltiazem y las cápsulas de clorhidrato de diltiazem (dos veces al día). A medida que se aumenta la dosis de las cápsulas de liberación prolongada de clorhidrato de diltiazem (dosis una vez al día) de una dosis diaria de 120 mg a 240 mg, hay un aumento en el área bajo la curva de 2,7 veces. Cuando se aumenta la dosis de 240 mg a 360 mg, se produce un aumento del área bajo la curva de 1,6 veces.
INFORMACIÓN DEL PACIENTE
No se proporcionó información. por favor refiérase a ADVERTENCIAS y PRECAUCIONES secciones.
