Cordarone 100mg, 50mg Amiodarone Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Cordarone 100 mg y cómo se usa?
Cordarone 100 mg IV es un medicamento recetado que se usa para tratar los síntomas del ritmo cardíaco irregular (arritmias ventriculares).
- Cordarone IV se puede usar solo o con otros medicamentos.
- Cordarone 50mg IV pertenece a una clase de medicamentos llamados Antidysrhythmisc, III.
¿Cuáles son los posibles efectos secundarios de Cordarone 100 mg?
Cordarone 100 mg puede causar efectos secundarios graves, que incluyen:
- dificultad para respirar,
- desmayo,
- latidos cardíacos rápidos o irregulares,
- Dolor de pecho,
- sibilancias, y
- respiración dificultosa
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Cordarone 100 mg IV incluyen:
- presión arterial baja (hipotensión),
- ritmo cardíaco lento,
- paro cardiaco,
- náuseas,
- fiebre,
- insuficiencia cardíaca congestiva,
- ritmo cardíaco anormal,
- shock cardiogénico y
- anomalías en las pruebas de función hepática
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Cordarone. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
ADVERTENCIA
TOXICIDAD PULMONAR, HEPÁTICA Y CARDÍACA
CORDARONE 100 mg está diseñado para usarse solo en pacientes con las arritmias potencialmente mortales indicadas porque su uso se acompaña de una toxicidad considerable [ver INDICACIONES Y USO].
CORDARONE puede causar toxicidad pulmonar (neumonitis por hipersensibilidad o neumonitis intersticial/alveolar) que ha resultado en una enfermedad clínicamente manifiesta en tasas de hasta el 17% en algunas series de pacientes. La toxicidad pulmonar ha sido mortal aproximadamente el 10% de las veces. Obtenga una radiografía de tórax de referencia y pruebas de función pulmonar, incluida la capacidad de difusión, cuando se inicie la terapia con 100 mg de CORDARONE. Repetir la anamnesis, el examen físico y la radiografía de tórax cada 3 a 6 meses [ver ADVERTENCIAS Y PRECAUCIONES].
CORDARONE puede causar hepatotoxicidad, que puede ser fatal. Obtenga las transaminasas hepáticas basales y periódicas y suspenda o reduzca la dosis si el aumento excede tres veces lo normal, o se duplica en un paciente con una base elevada. Discontinúe CORDARONE si el paciente experimenta signos o síntomas de daño hepático clínico [ver ADVERTENCIAS Y PRECAUCIONES].
CORDARONE puede exacerbar las arritmias. Inicie CORDARONE 50 mg en un entorno clínico donde estén disponibles electrocardiogramas continuos y reanimación cardíaca [ver ADVERTENCIAS Y PRECAUCIONES].
DESCRIPCIÓN
CORDARONE (amiodarona HCl) es un fármaco antiarrítmico, disponible para administración oral en forma de comprimidos ranurados de color rosa que contienen 200 mg de clorhidrato de amiodarona. Los ingredientes inactivos presentes son dióxido de silicio coloidal, lactosa, estearato de magnesio, povidona, almidón y FD&C Red 40. CORDARONE es un derivado de benzofurano: 2-butil-3-benzofuranil 4-[2-(dietilamino)-etoxi]- 3, Clorhidrato de 5-diyodofenilcetona.
La fórmula estructural es la siguiente:
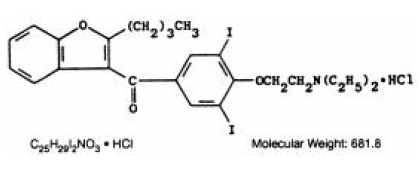
La amiodarona HCl es un polvo cristalino de color blanco a crema. Es ligeramente soluble en agua, soluble en alcohol y libremente soluble en cloroformo. Contiene 37,3% de yodo en peso.
INDICACIONES
CORDARONE está indicado para el tratamiento de la fibrilación ventricular recurrente documentada y potencialmente mortal y la taquicardia hemodinámicamente inestable recurrente potencialmente mortal en adultos que no han respondido a las dosis adecuadas de otros antiarrítmicos disponibles o cuando no se pueden tolerar agentes alternativos.
DOSIFICACIÓN Y ADMINISTRACIÓN
La dosis debe individualizarse según la gravedad de la arritmia y la respuesta. Use la dosis efectiva más baja. Obtenga una radiografía de tórax basal, pruebas de función pulmonar, pruebas de función tiroidea y aminotransferasas hepáticas. Corregir la hipopotasemia, la hipomagnesemia y la hipocalcemia antes de iniciar el tratamiento
Dósis recomendada
Inicie el tratamiento con dosis de carga de 800 a 1600 mg/día hasta que se produzca la respuesta terapéutica inicial (generalmente de 1 a 3 semanas). Una vez que se logre un control adecuado de la arritmia, o si los efectos secundarios se vuelven prominentes, reduzca la dosis de 50 mg de CORDARONE a 600 a 800 mg/día durante un mes y luego a la dosis de mantenimiento, generalmente 400 mg/día.
Administración
Administrar CORDARONE consistentemente con respecto a las comidas [ver FARMACOLOGÍA CLÍNICA ]. Se sugiere la administración de CORDARONE en dosis divididas con las comidas para dosis diarias totales de 1000 mg o más, o cuando se presenta intolerancia gastrointestinal.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
Comprimidos de 200 mg: comprimidos rosados, redondos, de cara convexa, con una “C” en relieve y marcados con “200” en un lado, con el reverso ranurado y marcado con “WYETH” y “4188”.
Almacenamiento y manipulación
CORDARONE® (amiodarona HCl) Tabletas están disponibles en frascos de 60 tabletas de la siguiente manera:
200 miligramos , CDN 0008-4188-04, comprimidos rosados redondos, de cara convexa, con una "C" en relieve y marcado "200" en un lado, con el reverso ranurado y marcado "WYETH" y "4188".
Mantener bien cerrado.
Almacenar a temperatura ambiente controlada, 20° a 25°C (68° a 77°F).
Proteger de la luz.
Dispense en un recipiente hermético resistente a la luz.
Fabricado por Sanofi Winthrop Industrie, 1, rue de la Vierge, 33440 Ambares, Francia. Distribuido por: Wyeth Pharmaceuticals Inc., una subsidiaria de Pfizer Inc., Filadelfia, PA 19101. Revisado: octubre de 2018
EFECTOS SECUNDARIOS
Las siguientes reacciones adversas graves se describen con más detalle en otras secciones de la información de prescripción:
- Toxicidad pulmonar [ver ADVERTENCIAS Y PRECAUCIONES ]
- Lesión hepática [ver ADVERTENCIAS Y PRECAUCIONES ]
- Empeoramiento de la arritmia [ver ADVERTENCIAS Y PRECAUCIONES ]
- Deterioro visual y pérdida de la visión [ver ADVERTENCIAS Y PRECAUCIONES ]
- Anomalías de la tiroides [ver ADVERTENCIAS Y PRECAUCIONES ]
- Bradicardia [ver ADVERTENCIAS Y PRECAUCIONES ]
- Neuropatía periférica [ver ADVERTENCIAS Y PRECAUCIONES ]
- Fotosensibilidad y decoloración de la piel [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy diversas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica.
la dosis de mantenimiento habitual (400 mg/día) y superiores, CORDARONE 100 mg provoca reacciones adversas en alrededor de las tres cuartas partes de todos los pacientes, lo que da lugar a la suspensión en un 7 a un 18 %.
En encuestas de casi 5000 pacientes tratados en estudios abiertos en EE. UU. y en informes publicados de tratamiento con CORDARONE, las reacciones adversas que con mayor frecuencia requirieron la interrupción de CORDARONE incluyeron infiltrados o fibrosis pulmonares, taquicardia ventricular paroxística, insuficiencia cardíaca congestiva y elevación de las enzimas hepáticas. Otros síntomas que causaron interrupciones con menos frecuencia incluyeron alteraciones visuales, fotosensibilidad, decoloración azul de la piel, hipertiroidismo e hipotiroidismo.
Las siguientes tasas de efectos secundarios se basan en un estudio retrospectivo de 241 pacientes tratados durante 2 a 1515 días (media de 441,3 días):
Tiroides
Frecuentes: hipotiroidismo, hipertiroidismo.
Cardiovascular
Frecuentes: insuficiencia cardíaca congestiva, arritmias cardíacas, disfunción del nódulo SA.
Gastrointestinal
Muy comunes: Náuseas, vómitos.
Frecuentes: estreñimiento, anorexia, dolor abdominal.
dermatológico
Frecuentes: Dermatitis solar/fotosensibilidad.
neurológico
Frecuentes: Malestar y fatiga, temblor/movimientos involuntarios anormales, falta de coordinación, marcha anormal/ataxia, mareos, parestesias, disminución de la libido, insomnio, dolor de cabeza, trastornos del sueño.
Oftálmico
Frecuentes: Alteraciones visuales.
Hepático
Frecuentes: pruebas de función hepática anormales, trastornos hepáticos inespecíficos.
Respiratorio
Frecuentes: Inflamación o fibrosis pulmonar.
Otro
Frecuentes: enrojecimiento, gusto y olfato anormales, edema, salivación anormal, anomalías en la coagulación.
Poco frecuentes: coloración azulada de la piel, erupción cutánea, equimosis espontánea, alopecia, hipotensión y anomalías de la conducción cardíaca.
Experiencia posterior a la comercialización
Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación de CORDARONE. Debido a que estas reacciones son informadas voluntariamente por una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
hematológico anemia hemolítica, anemia aplásica, pancitopenia, neutropenia, trombocitopenia, agranulocitosis, granuloma.
Inmune : reacción anafiláctica/anafilactoide (incluyendo shock), angioedema.
neurológico : pseudotumor cerebri, síntomas parkinsonianos como acinesia y bradicinesia (a veces reversibles con la suspensión del tratamiento), polineuropatía desmielinizante.
Psiquiátrico : alucinación, estado confusional, desorientación, delirio.
Cardíaco : hipotensión (a veces fatal), paro sinusal.
Respiratorio : neumonía eosinofílica, síndrome de dificultad respiratoria aguda en el postoperatorio, broncoespasmo, bronquiolitis obliterante, neumonía organizada, hemorragia alveolar pulmonar, derrame pleural, pleuritis.
Gastrointestinal : pancreatitis, pancreatitis aguda.
Hepático : hepatitis, hepatitis colestásica, cirrosis.
Trastornos de la piel y del tejido subcutáneo urticaria, necrólisis epidérmica tóxica (a veces mortal), eritema multiforme, síndrome de Stevens-Johnson, dermatitis exfoliativa, dermatitis ampollosa, erupción medicamentosa con eosinofilia y síntomas sistémicos (DRESS), eccema, prurito, cáncer de piel, síndrome similar al lupus.
musculoesquelético : miopatía, debilidad muscular, rabdomiolisis.
Renal : insuficiencia renal, insuficiencia renal, insuficiencia renal aguda.
Reproductivo : epididimitis, impotencia.
cuerpo como un todo : fiebre, boca seca.
endocrino y metabólico : nódulos tiroideos/ cáncer de tiroides, síndrome de secreción inadecuada de hormona antidiurética (SIADH).
Vascular : vasculitis.
INTERACCIONES CON LA DROGAS
Debido a la larga vida media de la amiodarona, es de esperar que las interacciones farmacológicas persistan durante semanas o meses después de suspender la amiodarona.
Las interacciones farmacológicas con amiodarona se describen en la Tabla 1 a continuación.
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Persistencia de los efectos adversos
Debido a la larga vida media de la amiodarona (15 a 142 días) y su metabolito activo desetilamiodarona (14 a 75 días), las reacciones adversas y las interacciones farmacológicas pueden persistir durante varias semanas después de la interrupción de la amiodarona [ver FARMACOLOGÍA CLÍNICA ].
Toxicidad pulmonar
CORDARONE puede causar un síndrome clínico de tos y disnea progresiva acompañado de datos funcionales, radiográficos, de gammagrafía con galio y patológicos compatibles con toxicidad pulmonar. La toxicidad pulmonar secundaria a CORDARONE puede resultar de toxicidad directa o indirecta representada por neumonitis por hipersensibilidad (incluida la neumonía eosinofílica) o neumonitis intersticial/alveolar, respectivamente. Se ha informado que las tasas de toxicidad pulmonar alcanzan el 17% y son fatales en aproximadamente el 10% de los casos. Obtenga una radiografía de tórax de referencia y pruebas de función pulmonar, incluida la capacidad de difusión, cuando se inicie la terapia con 50 mg de CORDARONE. Repita la historia, el examen físico y la radiografía de tórax cada 3 a 6 meses o si se presentan síntomas. Considere una terapia antiarrítmica alternativa si el paciente experimenta signos o síntomas de toxicidad pulmonar. La prednisona, de 40 a 60 mg/día, con disminución gradual durante varias semanas, puede ser útil para tratar la toxicidad pulmonar.
Síndrome de Dificultad Respiratoria del Adulto (SDRA)
Después de la operación, se informaron casos de ARDS en pacientes que recibieron terapia con CORDARONE que se sometieron a cirugía cardíaca o no cardíaca. Aunque los pacientes generalmente responden bien a la terapia respiratoria vigorosa, en raras ocasiones el desenlace ha sido fatal.
lesión hepática
Con frecuencia se observan elevaciones asintomáticas de los niveles de enzimas hepáticas, pero CORDARONE 100 mg puede causar lesiones hepáticas potencialmente mortales. La histología se asemeja a la de la hepatitis alcohólica o cirrosis. Obtenga transaminasas hepáticas basales y periódicas. Si las transaminasas exceden tres veces lo normal, o se duplican en un paciente con una línea de base elevada, suspenda o reduzca la dosis de CORDARONE 100 mg, obtenga pruebas de seguimiento y trate adecuadamente.
Empeoramiento de la arritmia
CORDARONE 100 mg puede exacerbar la arritmia de presentación en alrededor del 2 al 5 % de los pacientes o causar una nueva fibrilación ventricular, taquicardia ventricular incesante, aumento de la resistencia a la cardioversión y taquicardia ventricular polimórfica asociada con la prolongación del intervalo QTc (Torsade de Pointes [TdP]).
Corregir la hipopotasemia, la hipomagnesemia y la hipocalcemia antes de iniciar el tratamiento con CORDARONE, ya que estos trastornos pueden exagerar el grado de prolongación del QTc y aumentar el potencial de TdP. Preste especial atención al equilibrio de electrolitos y ácido-base en pacientes que experimentan diarrea severa o prolongada o que reciben medicamentos que afectan los niveles de electrolitos, como diuréticos, laxantes, corticosteroides sistémicos o anfotericina B.
Deterioro visual y pérdida de la visión
Neuropatía óptica y neuritis óptica
En pacientes tratados con amiodarona se han notificado casos de neuropatía óptica y neuritis óptica, que por lo general resultan en deficiencia visual y, en ocasiones, ceguera permanente, y pueden ocurrir en cualquier momento durante la terapia. Si aparecen síntomas de discapacidad visual, como cambios en la agudeza visual y disminución de la visión periférica, considere suspender CORDARONE 100 mg y remita de inmediato para un examen oftalmológico. Se recomienda un examen oftalmológico regular, incluyendo examen de fondo de ojo y examen con lámpara de hendidura, durante la administración de CORDARONE [ver REACCIONES ADVERSAS ].
Microdepósitos Corneales
Los microdepósitos corneales aparecen en la mayoría de los adultos tratados con CORDARONE. Suelen ser perceptibles sólo mediante un examen con lámpara de hendidura, pero dan lugar a síntomas como halos visuales o visión borrosa hasta en el 10% de los pacientes. Los microdepósitos corneales son reversibles al reducir la dosis o finalizar el tratamiento. Los microdepósitos asintomáticos por sí solos no son una razón para reducir la dosis o suspender el tratamiento [ver REACCIONES ADVERSAS ].
Anomalías de la tiroides
CORDARONE 50 mg inhibe la conversión periférica de tiroxina (T4) a triyodotironina (T3) y puede causar un aumento de los niveles de tiroxina, una disminución de los niveles de T3 y un aumento de los niveles de T3 inversa inactiva (rT3) en pacientes clínicamente eutiroideos. CORDARONE 50 mg puede causar hipotiroidismo (informado en hasta el 10% de los pacientes) o hipertiroidismo (que ocurre en aproximadamente el 2% de los pacientes). Controle la función tiroidea antes del tratamiento y periódicamente después, particularmente en pacientes de edad avanzada y en cualquier paciente con antecedentes de nódulos tiroideos, bocio u otra disfunción tiroidea.
El hipertiroidismo puede inducir un avance de la arritmia. Si aparecen nuevos signos de arritmia, se debe considerar la posibilidad de hipertiroidismo. Los medicamentos antitiroideos, los bloqueadores β-adrenérgicos y la terapia temporal con corticosteroides pueden ser necesarios para tratar los síntomas del hipertiroidismo. La acción de los fármacos antitiroideos puede retrasarse en la tirotoxicosis inducida por amiodarona debido a cantidades sustanciales de hormonas tiroideas preformadas almacenadas en la glándula. La terapia con yodo radiactivo está contraindicada debido a la baja captación de yodo radiactivo asociada con el hipertiroidismo inducido por amiodarona. El hipertiroidismo inducido por CORDARONE puede ser seguido por un período transitorio de hipotiroidismo.
El hipotiroidismo puede ser primario o posterior a la resolución del hipertiroidismo inducido por amiodarona anterior. Se ha informado hipotiroidismo severo y coma mixedematoso, a veces fatal, en asociación con la terapia con amiodarona. En algunos pacientes clínicamente hipotiroideos tratados con amiodarona, los valores del índice de tiroxina libre pueden ser normales. Controle el hipotiroidismo reduciendo la dosis o suspendiendo la suplementación con CORDARONE y hormona tiroidea.
bradicardia
CORDARONE causa bradicardia sintomática o paro sinusal con supresión de focos de escape en 2 a 4% de los pacientes. El riesgo aumenta con los trastornos electrolíticos o el uso concomitante de antiarrítmicos o cronotropos negativos [ver INTERACCIONES CON LA DROGAS ]. La bradicardia puede requerir un marcapasos para controlar la frecuencia.
Se informaron casos posteriores a la comercialización de bradicardia sintomática, algunos que requirieron la inserción de un marcapasos y al menos uno fatal, cuando se iniciaron ledipasvir/sofosbuvir o sofosbuvir con simeprevir en pacientes que tomaban amiodarona. La bradicardia generalmente se presentó en cuestión de horas o días, pero en algunos casos se presentó hasta 2 semanas después de iniciar el tratamiento antiviral. La bradicardia generalmente se resolvió después de la interrupción del tratamiento antiviral. Se desconoce el mecanismo de este efecto. Monitoree la frecuencia cardíaca en pacientes que toman o suspenden recientemente amiodarona al comenzar el tratamiento antiviral [ver INTERACCIONES CON LA DROGAS ].
Dispositivos cardíacos implantables
En pacientes con desfibriladores o marcapasos implantados, la administración crónica de fármacos antiarrítmicos puede afectar los umbrales de estimulación o desfibrilación. Por lo tanto, al inicio y durante el tratamiento con amiodarona, se deben evaluar los umbrales de estimulación y desfibrilación.
Toxicidad Fetal
CORDARONE puede causar daño fetal cuando se administra a una mujer embarazada. La exposición fetal puede aumentar el potencial de efectos cardíacos, tiroideos, de desarrollo neurológico, neurológicos y de crecimiento en el recién nacido [ver Uso en poblaciones específicas ].
Neuropatía periférica
La administración crónica de CORDARONE puede provocar neuropatía periférica, que puede no resolverse cuando se suspende CORDARONE.
Fotosensibilidad y decoloración de la piel
CORDARONE induce fotosensibilización en alrededor del 10% de los pacientes; se puede proporcionar cierta protección con cremas protectoras contra el sol o ropa protectora. Durante el tratamiento a largo plazo, puede ocurrir una decoloración azul grisácea de la piel expuesta. El riesgo puede aumentar en pacientes de tez clara o con exposición solar excesiva. Puede ocurrir cierta reversión de la decoloración al suspender el fármaco.
Cirugía
Agentes anestésicos volátiles
Los pacientes que reciben tratamiento con CORDARONE 100 mg pueden ser más sensibles a los efectos depresores del miocardio y de conducción de los anestésicos inhalatorios halogenados.
Información de asesoramiento para pacientes
Aconseje al paciente que lea la etiqueta del paciente aprobada por la FDA ( Guía de medicamentos ).
Informar a las mujeres embarazadas sobre el riesgo potencial para el feto. Aconseje a las mujeres con potencial reproductivo que informen a su prescriptor de un embarazo conocido o sospechado [ver Uso en poblaciones específicas ].
Aconseje a las mujeres que no se recomienda amamantar durante el tratamiento con CORDARONE [ver Uso en poblaciones específicas ].
Aconseje a los pacientes que eviten el jugo de toronja y la hierba de San Juan.
Aconseje a los pacientes que busquen atención médica si experimentan signos y síntomas de toxicidad pulmonar, empeoramiento de la arritmia, bradicardia, discapacidad visual o hipo e hipertiroidismo.
La etiqueta de este producto puede haber sido actualizada. Para obtener información completa sobre la prescripción, visite www.pfizer.com.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
El clorhidrato de amiodarona se asoció con un aumento estadísticamente significativo relacionado con la dosis en la incidencia de tumores tiroideos (adenoma y/o carcinoma folicular) en ratas. La incidencia de tumores tiroideos fue mayor que la del control con el nivel de dosis más bajo probado, es decir, 5 mg/kg/día (aproximadamente 0,08 veces la dosis de mantenimiento máxima recomendada en humanos*).
Los estudios de mutagenicidad (test de Ames, micronúcleos y lisogénico) con CORDARONE fueron negativos.
En un estudio en el que se administró amiodarona HCl a ratas macho y hembra, comenzando 9 semanas antes del apareamiento, se observó una reducción de la fertilidad a un nivel de dosis de 90 mg/kg/día (aproximadamente 1,4 veces la dosis de mantenimiento máxima recomendada en humanos*).
*600 mg en un paciente de 60 kg (dosis comparada en función del área de superficie corporal)
Uso en poblaciones específicas
El embarazo
Resumen de riesgos
Los datos disponibles de los informes posteriores a la comercialización y las series de casos publicadas indican que el uso de amiodarona en mujeres embarazadas puede aumentar el riesgo de efectos adversos fetales, incluidos hipo e hipertiroidismo neonatal, bradicardia neonatal, anomalías del desarrollo neurológico, parto prematuro y restricción del crecimiento fetal. La amiodarona y su metabolito, desetilamiodarona (DEA), atraviesan la placenta. Las arritmias subyacentes no tratadas, incluidas las arritmias ventriculares, durante el embarazo representan un riesgo para la madre y el feto (ver Consideraciones clínicas ). En estudios con animales, la administración de amiodarona a conejos, ratas y ratones durante la organogénesis resultó en toxicidad embriofetal a dosis inferiores a la dosis máxima recomendada de mantenimiento en humanos (ver Datos ). Informar a las mujeres embarazadas sobre el riesgo potencial para el feto.
Se desconoce el riesgo de fondo estimado de defectos congénitos importantes y aborto espontáneo para la población indicada. Todos los embarazos tienen un riesgo de fondo de defecto congénito, pérdida u otros resultados adversos. En la población general de los EE. UU., el riesgo de fondo estimado de defectos congénitos importantes y aborto espontáneo en embarazos clínicamente reconocidos es del 2 % al 4 % y del 15 % al 20 %, respectivamente.
Consideraciones clínicas
Riesgo materno o embrionario/fetal asociado a la enfermedad
La incidencia de taquicardia ventricular aumenta y puede ser más sintomática durante el embarazo. Las arritmias ventriculares ocurren con mayor frecuencia en mujeres embarazadas con miocardiopatía subyacente, cardiopatía congénita, valvulopatía cardíaca o prolapso de la válvula mitral. La mayoría de los episodios de taquicardia se inician con latidos ectópicos y, por lo tanto, la aparición de episodios de arritmia puede aumentar durante el embarazo debido a la mayor propensión a la actividad ectópica. Las arritmias intercurrentes también pueden ocurrir durante el embarazo, ya que los niveles de tratamiento terapéutico pueden ser difíciles de mantener debido al aumento del volumen de distribución y al aumento del metabolismo del fármaco inherente al estado de embarazo.
Reacciones adversas fetales/neonatales
Se ha demostrado que la amiodarona y su metabolito atraviesan la placenta. Los efectos fetales adversos asociados con el uso de amiodarona materna durante el embarazo pueden incluir bradicardia neonatal, prolongación del intervalo QT y extrasístoles ventriculares periódicas, hipotiroidismo neonatal (con o sin bocio) detectado prenatalmente o en el recién nacido e informado incluso después de unos días de exposición, hipertiroxinemia neonatal, anomalías del neurodesarrollo independientes de la función tiroidea, que incluyen retraso del habla y dificultades con el lenguaje escrito y la aritmética, retraso en el desarrollo motor y ataxia, nistagmo espasmódico con titubeo sincrónico de la cabeza, restricción del crecimiento fetal y parto prematuro. Vigile al recién nacido en busca de signos y síntomas de trastornos de la tiroides y arritmias cardíacas.
Trabajo y entrega
El riesgo de arritmias puede aumentar durante el trabajo de parto y el parto. Las pacientes tratadas con CORDARONE deben ser monitoreadas continuamente durante el trabajo de parto y el parto [ver ADVERTENCIAS Y PRECAUCIONES ].
Datos
Datos de animales
En ratas y conejas preñadas durante el período de organogénesis, la amiodarona HCl en dosis de 25 mg/kg/día (aproximadamente 0,4 y 0,9 veces, respectivamente, la dosis de mantenimiento máxima recomendada en humanos*) no tuvo efectos adversos sobre el feto. En el conejo, 75 mg/kg/día (aproximadamente 2,7 veces la dosis de mantenimiento máxima recomendada en humanos*) provocó abortos en más del 90 % de los animales. En la rata, las dosis de 50 mg/kg/día o más se asociaron con un ligero desplazamiento de los testículos y una mayor incidencia de osificación incompleta de algunos huesos del cráneo y digitales; a 100 mg/kg/día o más, se redujeron los pesos corporales fetales; a 200 mg/kg/día, hubo una mayor incidencia de reabsorción fetal. (Estas dosis en la rata son aproximadamente 0,8, 1,6 y 3,2 veces la dosis de mantenimiento máxima recomendada en humanos*) También se observaron efectos adversos sobre el crecimiento y la supervivencia fetal en una de dos cepas de ratones a una dosis de 5 mg/kg/día ( aproximadamente 0,04 veces la dosis de mantenimiento máxima recomendada en humanos*).
*600 mg en un paciente de 60 kg (dosis comparadas en función del área de superficie corporal)
Lactancia
Resumen de riesgos
La amiodarona y uno de sus principales metabolitos, la DEA, están presentes en la leche materna entre el 3,5 % y el 45 % de la dosis materna de amiodarona ajustada al peso. Hay casos de hipotiroidismo y bradicardia en lactantes, aunque no está claro si estos efectos se deben a la exposición a la amiodarona en la leche materna. No se recomienda la lactancia durante el tratamiento con CORDARONE [ver ADVERTENCIAS Y PRECAUCIONES ].
Hembras y machos con potencial reproductivo
Esterilidad
Basado en estudios de fertilidad en animales, CORDARONE puede reducir la fertilidad femenina y masculina. No se sabe si este efecto es reversible. [ver Toxicología no clínica ].
Uso pediátrico
No se ha establecido la seguridad y eficacia de CORDARONE en pacientes pediátricos.
Uso geriátrico
Los sujetos normales mayores de 65 años muestran depuraciones más bajas y una mayor vida media del fármaco que los sujetos más jóvenes [ver FARMACOLOGÍA CLÍNICA ]. En general, la selección de la dosis para un paciente de edad avanzada debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedades concomitantes u otra terapia con medicamentos.
SOBREDOSIS
Ha habido casos, algunos fatales, de sobredosis de 50 mg de CORDARONE.
Controle el ritmo cardíaco y la presión arterial del paciente y, si se produce bradicardia, se puede utilizar un agonista β-adrenérgico o un marcapasos. Trate la hipotensión con perfusión tisular inadecuada con agentes inotrópicos y vasopresores positivos. Ni CORDARONE 50mg ni su metabolito son dializables.
CONTRAINDICACIONES
- Shock cardiogénico.
- Síndrome del seno enfermo, bloqueo auriculoventricular de segundo o tercer grado, bradicardia que lleva a un síncope sin un marcapasos en funcionamiento.
- Hipersensibilidad conocida al fármaco oa cualquiera de sus componentes, incluido el yodo.
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
La amiodarona se considera un fármaco antiarrítmico de clase III, pero posee características electrofisiológicas de las cuatro clases de Vaughan Williams. Al igual que los fármacos de clase I, la amiodarona bloquea los canales de sodio a frecuencias de estimulación rápida y, al igual que los fármacos de clase II, la amiodarona ejerce una acción antisimpática no competitiva. Uno de sus principales efectos, con la administración prolongada, es alargar el potencial de acción cardiaco, un efecto de clase III. El efecto cronotrópico negativo de la amiodarona en los tejidos ganglionares es similar al efecto de los fármacos de clase IV. Además de bloquear los canales de sodio, la amiodarona bloquea los canales de potasio del miocardio, lo que contribuye a la ralentización de la conducción y a la prolongación de la refractariedad. La acción antisimpática y el bloqueo de los canales de calcio y potasio son responsables de los efectos dromotrópicos negativos sobre el nódulo sinusal y del enlentecimiento de la conducción y prolongación de la refractariedad en el nódulo auriculoventricular (AV). Su acción vasodilatadora puede disminuir la carga de trabajo cardíaco y, en consecuencia, el consumo de oxígeno del miocardio.
CORDARONE prolonga la duración del potencial de acción de todas las fibras cardíacas mientras causa una reducción mínima de dV/dt (velocidad máxima de carrera ascendente del potencial de acción). El período refractario se prolonga en todos los tejidos cardíacos. CORDARONE aumenta el período refractario cardíaco sin influir en el potencial de membrana en reposo, excepto en células automáticas donde se reduce la pendiente del prepotencial, generalmente reduciendo la automaticidad. Estos efectos electrofisiológicos se reflejan en una disminución de la frecuencia sinusal de 15 a 20%, intervalos PR y QT aumentados de alrededor de 10%, el desarrollo de ondas U y cambios en el contorno de la onda T. Estos cambios no deberían requerir la suspensión de CORDARONE 50 mg ya que son evidencia de su acción farmacológica, aunque CORDARONE puede causar bradicardia sinusal marcada o paro sinusal y bloqueo cardíaco [ver ADVERTENCIAS Y PRECAUCIONES ].
hemodinámica
En estudios con animales y después de la administración intravenosa en humanos, CORDARONE 100 mg relaja el músculo liso vascular, reduce la resistencia vascular periférica (poscarga) y aumenta ligeramente el índice cardíaco. Sin embargo, después de la dosificación oral, CORDARONE 100 mg no produce cambios significativos en la fracción de eyección del ventrículo izquierdo (FEVI), incluso en pacientes con FEVI deprimida. Después de la dosificación intravenosa aguda en el hombre, CORDARONE 100 mg puede tener un efecto inotrópico negativo leve.
Farmacodinámica
No existe una relación bien establecida entre la concentración plasmática y la eficacia, pero parece que las concentraciones muy por debajo de 1 mg/L a menudo son ineficaces y que los niveles superiores a 2,5 mg/L generalmente no son necesarios. Las mediciones de concentración plasmática se pueden usar para identificar a los pacientes cuyos niveles son inusualmente bajos y que podrían beneficiarse de un aumento de la dosis, o inusualmente altos, y que podrían tener una reducción de la dosis con la esperanza de minimizar los efectos secundarios.
Los efectos sobre los ritmos anormales no se observan antes de 2 a 3 días y generalmente requieren de 1 a 3 semanas, incluso cuando se usa una dosis de carga. Puede haber un aumento continuo en el efecto durante períodos aún más largos. Existe evidencia de que el tiempo hasta el efecto es más corto cuando se usa un régimen de dosis de carga.
De acuerdo con la lenta tasa de eliminación, los efectos antiarrítmicos persisten durante semanas o meses después de suspender CORDARONE 50 mg, pero el tiempo de recurrencia es variable e impredecible. En general, cuando se reanuda el fármaco después de la recurrencia de la arritmia, el control se establece con relativa rapidez en comparación con la respuesta inicial, presumiblemente porque las reservas tisulares no se agotaron por completo.
Farmacocinética
Absorción
Luego de la administración oral en humanos, CORDARONE se absorbe lenta y variablemente. La biodisponibilidad de CORDARONE es aproximadamente del 50%. Las concentraciones plasmáticas máximas se alcanzan de 3 a 7 horas después de una dosis única. Las concentraciones plasmáticas con dosis crónicas de 100 a 600 mg/día son aproximadamente proporcionales a la dosis, con un aumento medio de 0,5 mg/l por cada 100 mg/día. Estos medios, sin embargo, incluyen una considerable variabilidad individual.
Los alimentos aumentan la velocidad y el grado de absorción de CORDARONE. Los efectos de los alimentos sobre la biodisponibilidad de CORDARONE se han estudiado en 30 sujetos sanos que recibieron una dosis única de 600 mg inmediatamente después de consumir una comida rica en grasas y después de un ayuno nocturno. El área bajo la curva de concentración plasmática-tiempo (AUC) y la concentración plasmática máxima (Cmax) de amiodarona aumentaron 2,3 (rango 1,7 a 3,6) y 3,8 (rango 2,7 a 4,4) veces, respectivamente, en presencia de alimentos. Los alimentos también aumentaron la tasa de absorción de amiodarona, disminuyendo el tiempo hasta la concentración plasmática máxima (Tmax) en un 37 %. El AUC medio y la Cmax media del principal metabolito de la amiodarona, DEA, aumentaron un 55 % (rango de 58 a 101 %) y un 32 % (rango de 4 a 84 %), respectivamente, pero no hubo cambios en la Tmax en presencia de alimento.
Distribución
CORDARONE se une en gran medida a las proteínas (aproximadamente un 96 %). CORDARONE tiene un volumen de distribución muy grande pero variable, con un promedio de alrededor de 60 l/kg, debido a la gran acumulación en varios sitios, especialmente en el tejido adiposo y órganos altamente perfundidos, como el hígado, los pulmones y el bazo.
Se ha identificado en el hombre un metabolito principal de CORDARONE 50 mg, DEA; se acumula en mayor medida en casi todos los tejidos. No hay datos disponibles sobre la actividad de la DEA en humanos, pero en animales tiene efectos electrofisiológicos y antiarrítmicos significativos, generalmente similares a los de la amiodarona. El papel y la contribución precisos de la DEA a la actividad antiarrítmica de la amiodarona oral no son seguros. El desarrollo de efectos ventriculares máximos de clase III después de la administración oral de 100 mg de CORDARONE en humanos se correlaciona más estrechamente con la acumulación de DEA a lo largo del tiempo que con la acumulación de amiodarona.
Eliminación
Después de la administración de una dosis única en 12 sujetos sanos, CORDARONE exhibió una farmacocinética multicompartimental con una semivida de eliminación terminal plasmática aparente media de 58 días (rango de 15 a 142 días) para la amiodarona y de 36 días (rango de 14 a 75 días) para el principio activo. metabolito (DEA). En pacientes, después de la interrupción de la terapia oral crónica, se ha demostrado que CORDARONE 100 mg tiene una eliminación bifásica con una reducción inicial del 50 % de los niveles plasmáticos después de 2,5 a 10 días. Una fase de eliminación de plasma terminal mucho más lenta muestra una vida media del compuesto original que varía de 26 a 107 días, con una media de aproximadamente 53 días y la mayoría de los pacientes en el rango de 40 a 55 días. En ausencia de un período de dosis de carga, las concentraciones plasmáticas en estado estacionario, con una dosis oral constante, se alcanzarían entre 130 y 535 días, con un promedio de 265 días. Para el metabolito, la vida media de eliminación plasmática media fue de aproximadamente 61 días. Estos datos probablemente reflejan una eliminación inicial del fármaco del tejido bien perfundido (la fase de semivida de 2,5 a 10 días), seguida de una fase terminal que representa una eliminación extremadamente lenta de los compartimentos del tejido mal perfundido, como la grasa.
La considerable variación entre sujetos en ambas fases de eliminación, así como la incertidumbre sobre qué compartimento es crítico para el efecto del fármaco, requiere atención a las respuestas individuales una vez que se logra el control de la arritmia con dosis de carga porque la dosis de mantenimiento correcta se determina, en parte, por las tasas de eliminación. Individualice las dosis de mantenimiento de CORDARONE [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Metabolismo
La amiodarona se metaboliza a DEA por el grupo de enzimas del citocromo P450 (CYP), específicamente CYP3A y CYP2C8. La isoenzima CYP3A está presente tanto en el hígado como en los intestinos. In vitro, la amiodarona y la DEA exhiben potencial para inhibir CYP2C9, CYP2C19, CYP2D6, CYP3A, CYP2A6, CYP2B6 y CYP2C8. La amiodarona y la DEA también tienen potencial para inhibir algunos transportadores como la glicoproteína P y el transportador de cationes orgánicos (OCT2).
Excreción
La amiodarona se elimina principalmente por metabolismo hepático y excreción biliar y la excreción de amiodarona o DEA en la orina es insignificante. Ni la amiodarona ni la DEA son dializables.
Poblaciones Específicas
efecto de la edad
Los sujetos normales mayores de 65 años muestran depuraciones más bajas (alrededor de 100 ml/h/kg) que los sujetos más jóvenes (alrededor de 150 ml/h/kg) y un aumento en la t½ de aproximadamente 20 a 47 días.
Insuficiencia renal
La insuficiencia renal no influye en la farmacocinética de la amiodarona o la DEA.
Deterioro hepático
Después de una dosis única de amiodarona intravenosa a pacientes cirróticos, se observan valores de concentración promedio y Cmax significativamente más bajos para DEA, pero los niveles medios de amiodarona no se modifican.
Enfermedad cardiaca
En pacientes con disfunción ventricular izquierda grave, la farmacocinética de la amiodarona no se modifica significativamente, pero la semivida de eliminación terminal de la DEA se prolonga.
Aunque no se ha definido un ajuste de dosis para pacientes con anomalías renales, hepáticas o cardíacas durante el tratamiento crónico con amiodarona oral, es prudente una estrecha vigilancia clínica para pacientes de edad avanzada y aquellos con disfunción ventricular izquierda grave.
Interacciones con la drogas
Efectos de otros agentes sobre la amiodarona
Jugo de toronja: El jugo de toronja administrado a voluntarios sanos aumentó el AUC de amiodarona en un 50 % y la Cmax en un 84 %, y disminuyó la DEA a concentraciones no cuantificables.
La cimetidina inhibe el CYP3A y puede aumentar los niveles séricos de amiodarona.
La colestiramina reduce la circulación enterohepática de la amiodarona aumentando así su eliminación. Esto da como resultado una reducción de los niveles séricos y de la vida media de la amiodarona.
Efectos de la amiodarona sobre los agentes
Sustratos CYP3A
La amiodarona tomada concomitantemente con quinidina aumenta la concentración sérica de quinidina en un 33 % después de dos días. La amiodarona tomada concomitantemente con procainamida durante menos de siete días aumenta las concentraciones plasmáticas de procainamida y n-acetil procainamida en un 55 % y un 33 %, respectivamente.
La loratadina, un antihistamínico no sedante, es metabolizado principalmente por CYP3A y su metabolismo puede ser inhibido por amiodarona.
La amiodarona puede inhibir el metabolismo de la lidocaína.
La ciclofosfamida es un profármaco, metabolizado por CYP450, incluido CYP3A, a un metabolito activo. La amiodarona puede inhibir el metabolismo de la ciclofosfamida.
El clopidogrel, un profármaco de tienopiridina inactivo, es metabolizado en el hígado por CYP3A a un metabolito activo. Se ha informado una interacción potencial entre clopidogrel y amiodarona que da como resultado una inhibición ineficaz de la agregación plaquetaria.
Antibióticos macrólidos/cetólidos
La amiodarona puede inhibir el metabolismo de los antibióticos macrólidos/cetólidos (excepto la azitromicina) y los fármacos antifúngicos azoles sistémicos.
Sustratos de glicoproteína P
La amiodarona tomada concomitantemente con digoxina aumenta la concentración sérica de digoxina en un 70 % después de un día.
El etexilato de dabigatrán cuando se toma concomitantemente con amiodarona oral puede resultar en una concentración sérica elevada de dabigatrán.
El dextrometorfano es un sustrato tanto para CYP2D6 como para CYP3A. La amiodarona inhibe CYP2D6. La administración oral crónica (> 2 semanas) de amiodarona altera el metabolismo del dextrometorfano y puede conducir a un aumento de las concentraciones séricas.
INFORMACIÓN DEL PACIENTE
CORDARONE® (KOR-DU-RON) (amiodarona) tabletas
¿Cuál es la información más importante que debo saber sobre CORDARONE 50mg?
CORDARONE puede causar efectos secundarios graves que pueden provocar la muerte, entre ellos:
- problemas pulmonares
- problemas hepáticos
- empeoramiento de los problemas de latidos del corazón
Llame a su proveedor de atención médica o busque ayuda médica de inmediato si tiene alguno de los siguientes síntomas durante el tratamiento con CORDARONE:
- dificultad para respirar, sibilancias, dificultad para respirar, tos, dolor en el pecho, regurgitación de sangre o fiebre
- náuseas o vómitos, orina de color marrón u oscuro, sentirse más cansado de lo normal, coloración amarillenta de la piel o el blanco de los ojos (ictericia) o dolor en la parte superior derecha del estómago
- palpitaciones, saltos, latidos rápidos o lentos, sensación de mareo o si se desmaya
- problemas de visión, incluyendo visión borrosa, halos de visión o sus ojos se vuelven sensibles a la luz. Debe realizarse exámenes oculares regulares antes y durante el tratamiento con CORDARONE.
CORDARONE debe iniciarse en un hospital para que su condición médica pueda ser monitoreada cuidadosamente.
CORDARONE solo debe usarse para tratar a personas a las que se les haya diagnosticado problemas de latidos cardíacos potencialmente mortales llamados arritmias ventriculares, cuando otros tratamientos no hayan funcionado o no los pueda tolerar.
CORDARONE 50mg puede causar otros efectos secundarios graves. Ver “¿Cuáles son los posibles efectos secundarios de CORDARONE 100mg?” Si tiene efectos secundarios graves durante el tratamiento, es posible que deba suspender CORDARONE, cambiar su dosis o recibir tratamiento médico. Hable con su proveedor de atención médica antes de dejar de tomar CORDARONE.
Es posible que aún tenga efectos secundarios después de suspender CORDARONE porque el medicamento permanece en su cuerpo durante meses después de que se suspende el tratamiento.
Debe realizarse chequeos regulares, análisis de sangre, radiografías de tórax antes y durante el tratamiento con CORDARONE 100 mg para detectar efectos secundarios graves. También debe realizarse pruebas de función pulmonar antes de iniciar el tratamiento con CORDARONE.
¿Qué es CORDARONE?
CORDARONE es un medicamento recetado que se usa para tratar a las personas a las que se les ha diagnosticado problemas de latidos cardíacos potencialmente mortales llamados arritmias ventriculares, cuando otros tratamientos no funcionaron o no los puede tolerar. No se sabe si CORDARONE es seguro y efectivo en niños.
¿Quién no debe tomar CORDARONE 100mg?
No tome CORDARONE 100 mg si:
- tiene un problema cardíaco grave llamado shock cardiogénico
- tiene ciertos tipos de la afección cardíaca llamada bloqueo cardíaco, con o sin frecuencia cardíaca lenta
- tiene un ritmo cardíaco lento con mareos o aturdimiento, y no tiene un marcapasos implantado
- es alérgico a la amiodarona, al yodo o a cualquiera de los demás componentes de CORDARONE. Consulte el final de esta Guía del medicamento para obtener una lista completa de los ingredientes de CORDARONE.
Antes de tomar CORDARONE 100 mg, informe a su proveedor de atención médica sobre todas sus afecciones médicas, incluso si usted:
- tiene problemas pulmonares o respiratorios
- tiene problemas hepáticos
- tiene o ha tenido problemas de tiroides
- tiene un ritmo cardíaco lento o problemas de presión arterial
- tiene diarrea o ha tenido diarrea durante un largo período de tiempo
- le han dicho que tiene niveles bajos de potasio, magnesio o calcio en la sangre
- tiene implantado un marcapasos o desfribrilador
- si planea someterse a una cirugía con anestesia general
- está embarazada o planea quedar embarazada. CORDARONE puede dañar a su bebé nonato. Informe a su proveedor de atención médica de inmediato si queda embarazada durante el tratamiento con CORDARONE. CORDARONE 100 mg puede permanecer en su cuerpo durante meses después de suspender el tratamiento.
- están amamantando o planean amamantar. CORDARONE 100 mg puede pasar a la leche materna y dañar a su bebé. No debe amamantar mientras toma CORDARONE. CORDARONE puede permanecer en su cuerpo durante meses después de suspender el tratamiento. Hable con su proveedor de atención médica sobre la mejor manera de alimentar a su bebé durante este tiempo.
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluidos los medicamentos recetados y de venta libre, las vitaminas y los suplementos a base de hierbas. CORDARONE 50mg y ciertos otros medicamentos pueden interactuar entre sí y causar efectos secundarios graves. Puede pedirle a su farmacéutico una lista de medicamentos que interactúan con CORDARONE.
¿Cómo debo tomar CORDARONE?
- Cuando le den de alta del hospital, tome CORDARONE exactamente como le indique su médico.
- Su proveedor de atención médica le dirá cuánto CORDARONE debe tomar y cuándo tomarlo.
- Su proveedor de atención médica puede cambiar su dosis de CORDARONE 50 mg según sea necesario si su ritmo cardíaco está controlado o si tiene ciertos efectos secundarios. Su proveedor de atención médica debe controlarlo atentamente cuando cambie su dosis de CORDARONE 50 mg.
- Tome su dosis de CORDARONE de la misma manera cada vez, con o sin alimentos.
- Si toma demasiado CORDARONE 100 mg, llame a su proveedor de atención médica o vaya a la sala de emergencias del hospital más cercano de inmediato. Si olvida una dosis, espere y tome la próxima dosis a la hora habitual. No tome dos dosis a la vez. Continúe con su próxima dosis programada regularmente.
¿Qué debo evitar mientras tomo CORDARONE?
- Evite beber jugo de toronja durante el tratamiento con CORDARONE. Beber jugo de toronja con CORDARONE 50 mg puede aumentar la cantidad de CORDARONE en su sangre y esto puede provocar efectos secundarios.
- CORDARONE 100mg puede hacer que su piel sea sensible a la luz solar. Podría sufrir quemaduras solares graves. Use protector solar y use un sombrero y ropa que cubra su piel para ayudarlo a protegerse si debe estar expuesto a la luz solar. Hable con su médico si se quema con el sol. Consulte "Problemas de la piel" en la sección de la Guía del medicamento “¿Cuáles son los posibles efectos secundarios de CORDARONE?” abajo.
¿Cuáles son los posibles efectos secundarios de CORDARONE?
CORADARONE puede causar efectos secundarios graves, que incluyen:
- Ver “¿Cuál es la información más importante que debo saber sobre CORDARONE?”
- Problemas nerviosos. CORDARONE 100mg puede causar problemas nerviosos. Llame a su proveedor de atención médica si presenta síntomas de problemas nerviosos, que incluyen: sensación de hormigueo o entumecimiento en las manos, las piernas o los pies, debilidad muscular, movimientos incontrolados, mala coordinación o dificultad para caminar.
- Problemas de la piel. CORDARONE puede hacer que su piel sea más sensible al sol o adquiera un color gris azulado. Las personas que tienen la piel clara o las personas que se exponen mucho al sol pueden tener un mayor riesgo de tener estos problemas de la piel. Parte del color gris azulado de la piel puede volver a la normalidad después de suspender CORDARONE.
- Problemas tiroideos. CORDARONE puede hacer que tenga una función tiroidea disminuida (hipotiroidismo), que a veces puede ser grave, o una tiroides hiperactiva (hipertiroidismo), que puede ser grave.
- Si desarrolla una función tiroidea disminuida durante el tratamiento con CORDARONE, es posible que su proveedor de atención médica necesite reducir su dosis o suspender su tratamiento con CORDARONE, y posiblemente recetarle un medicamento para reemplazar su hormona tiroidea.
- Una tiroides hiperactiva puede hacer que produzca demasiada hormona tiroidea. Puede tener latidos cardíacos anormales incluso mientras está recibiendo CORDARONE. Su proveedor de atención médica puede recetarle ciertos medicamentos para tratar su tiroides hiperactiva. Llame a su proveedor de atención médica si tiene latidos cardíacos anormales durante el tratamiento con CORDARONE. Esto puede significar que tiene una tiroides hiperactiva.
- Su proveedor de atención médica debe realizar pruebas para verificar su función tiroidea antes de comenzar y durante el tratamiento con CORDARONE.
- Llame a su proveedor de atención médica si desarrolla alguno de los siguientes síntomas de un problema de tiroides durante el tratamiento con CORDARONE:
- debilidad
- pérdida de peso o aumento de peso
- intolerancia al calor o al frío
- adelgazamiento del cabello
- transpiración
- cambios en sus períodos menstruales
- hinchazón del cuello (bocio)
- nerviosismo
- irritabilidad
- inquietud
- disminución de la concentración
- sentirse deprimido (en los ancianos)
- temblor
Los efectos secundarios más comunes de CORDARONE incluyen:
- problemas pulmonares
- problemas de latidos del corazón
- problemas del corazón
- problemas hepáticos
CORDARONE 50mg puede afectar la fertilidad en hombres y mujeres. No se sabe si los efectos son reversibles. Hable con su proveedor de atención médica si tiene inquietudes sobre la fertilidad.
Estos no son todos los posibles efectos secundarios de CORDARONE. Para obtener más información, consulte a su proveedor de atención médica o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
¿Cómo debo almacenar CORDARONE?
- Guarde CORDARONE 100mg a temperatura ambiente entre 20° y 25°C (68° y 77°F).
- Mantenga CORDARONE en un recipiente bien cerrado y mantenga CORDARONE 50 mg fuera de la luz.
Mantenga CORDARONE 50 mg y todos los medicamentos fuera del alcance de los niños.
Información general sobre el uso seguro y eficaz de CORDARONE
A veces, los medicamentos se recetan para fines distintos a los enumerados en la Guía del medicamento. No use CORDARONE para una condición para la cual no fue recetado. No le dé CORDARONE a otras personas, incluso si tienen los mismos síntomas que usted tiene. Puede que les haga daño. Puede pedirle a su farmacéutico o proveedor de atención médica información sobre CORDARONE escrita para profesionales de la salud.
¿Cuáles son los ingredientes de CORDARONE 100mg?
Ingrediente activo: clorhidrato de amiodarona
Ingredientes inactivos: dióxido de silicio coloidal, lactosa, estearato de magnesio, povidona, almidón y FD&C Red 40.
Esta Guía del medicamento ha sido aprobada por la Administración de Alimentos y Medicamentos de EE. UU.
