Clozaril 25mg, 50mg, 100mg Clozapine Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Clozaril y cómo se usa?
Clozaril 100 mg es un medicamento recetado que se usa para tratar los síntomas de la esquizofrenia. Clozaril 50 mg se puede usar solo o con otros medicamentos.
Clozaril 100mg pertenece a una clase de medicamentos llamados Antipsicóticos, 2da Generación.
No se sabe si Clozaril 25 mg es seguro y efectivo en niños.
¿Cuáles son los posibles efectos secundarios de Clozaril?
Clozaril puede causar efectos secundarios graves que incluyen:
- debilidad,
- fiebre,
- encías hinchadas,
- dolor de garganta,
- llagas dolorosas en la boca,
- dolor al tragar,
- llagas en la piel,
- síntomas de resfriado o gripe,
- tos,
- dificultad para respirar,
- movimientos musculares incontrolables de los labios, la lengua, los ojos, la cara, los brazos o las piernas,
- dolor de cabeza con dolor en el pecho y mareos intensos,
- latidos del corazón palpitantes,
- revoloteando en tu pecho,
- aturdimiento,
- tos repentina,
- respiración rápida,
- tosiendo sangre,
- sensación de opresión en el cuello o la mandíbula,
- espasmos o movimientos musculares incontrolables,
- convulsiones (apagón o convulsiones),
- orinar poco o nada,
- hinchazón en los pies o los tobillos,
- cansancio,
- dificultad para respirar,
- náuseas,
- dolor de estómago superior,
- pérdida de apetito,
- sangrado inusual,
- orina oscura,
- heces de color arcilla,
- coloración amarillenta de la piel o los ojos (ictericia),
- músculos muy rígidos (rígidos),
- fiebre alta,
- transpiración,
- confusión,
- latidos cardíacos rápidos o irregulares,
- temblores,
- aumento de la sed,
- aumento de la micción,
- hambre,
- boca seca,
- aliento con olor afrutado,
- somnolencia,
- piel seca,
- visión borrosa,
- pérdida de peso,
- moretones o sangrado fácil,
- hormigueo intenso o entumecimiento,
- debilidad muscular,
- dolor de estómago superior,
- Dolor de pecho,
- tos nueva o que empeora, y
- dificultad para respirar
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Clozaril incluyen:
- aumento de peso,
- temblor,
- mareo,
- sensación de giro,
- dolor de cabeza,
- somnolencia,
- náuseas,
- estreñimiento,
- boca seca,
- aumento de la salivación,
- visión borrosa,
- frecuencia cardíaca rápida y
- aumento de la sudoración
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Clozaril. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
ADVERTENCIA
NEUTROPENIA SEVERA; HIPOTENSIÓN ORTOSTÁTICA, BRADICARDIA Y SÍNCOPE; EMBARGO; MIOCARDITIS Y CARDIOMIOPATÍA; AUMENTO DE LA MORTALIDAD EN PACIENTES ANCIANOS CON PSICOSIS RELACIONADA CON DEMENCIA
Neutropenia severa
El tratamiento con CLOZARIL ha causado neutropenia grave, definida como un recuento absoluto de neutrófilos (RAN) inferior a 500/μL. La neutropenia grave puede provocar una infección grave y la muerte. Antes de iniciar el tratamiento con CLOZARIL, el ANC inicial debe ser de al menos 1500/ μL para la población general; y debe ser de al menos 1000/μl para pacientes con neutropenia étnica benigna (BEN) documentada. Durante el tratamiento, los pacientes deben someterse a un control regular del RAN. Aconseje a los pacientes que notifiquen de inmediato síntomas compatibles con neutropenia grave o infección (p. ej., fiebre, debilidad, letargo o dolor de garganta) [consulte DOSIS Y ADMINISTRACIÓN y ADVERTENCIAS Y PRECAUCIONES].
Debido al riesgo de neutropenia severa, CLOZARIL está disponible solo a través de un programa restringido bajo una Estrategia de Mitigación de Evaluación de Riesgo (REMS) llamado Programa Clozapine REMS. [ver ADVERTENCIAS Y PRECAUCIONES].
Hipotensión ortostática, bradicardia, síncope
Se han producido hipotensión ortostática, bradicardia, síncope y paro cardíaco con el tratamiento con CLOZARIL. El riesgo es mayor durante el período de titulación inicial, particularmente con un aumento rápido de la dosis. Estas reacciones pueden ocurrir con la primera dosis, con dosis tan bajas como 12,5 mg por día. Iniciar el tratamiento con 12,5 mg una o dos veces al día; valorar lentamente; y use dosis divididas. Use CLOZARIL con precaución en pacientes con enfermedad cardiovascular o cerebrovascular o condiciones que predispongan a la hipotensión (p. ej., deshidratación, uso de medicamentos antihipertensivos) [ver DOSIS Y ADMINISTRACIÓN y ADVERTENCIAS Y PRECAUCIONES].
convulsiones
Se han producido convulsiones con el tratamiento con CLOZARIL 25 mg. El riesgo está relacionado con la dosis. Inicie el tratamiento con 12,5 mg, titule gradualmente y utilice dosis divididas. Tenga cuidado al administrar CLOZARIL 50 mg a pacientes con antecedentes de convulsiones u otros factores de riesgo predisponentes para convulsiones (patología del SNC, medicamentos que reducen el umbral convulsivo, abuso de alcohol). Advierta a los pacientes sobre la participación en cualquier actividad en la que la pérdida repentina del conocimiento pueda causar un riesgo grave para ellos mismos o para los demás [ver DOSIS Y ADMINISTRACIÓN, ADVERTENCIAS Y PRECAUCIONES].
Miocarditis y Miocardiopatía
Se han producido miocarditis y cardiomiopatía fatales con el tratamiento con CLOZARIL. Suspender CLOZARIL 25 mg y obtener una evaluación cardíaca ante la sospecha de estas reacciones. En general, los pacientes con miocarditis o miocardiopatía relacionada con clozaril no deben volver a recibir CLOZARIL. Considere la posibilidad de miocarditis o cardiomiopatía si se presenta dolor torácico, taquicardia, palpitaciones, disnea, fiebre, síntomas parecidos a los de la gripe, hipotensión o cambios en el ECG [ver ADVERTENCIAS Y PRECAUCIONES].
Aumento de la mortalidad en pacientes ancianos con psicosis relacionada con demencia
Los pacientes de edad avanzada con psicosis relacionada con la demencia tratados con medicamentos antipsicóticos tienen un mayor riesgo de muerte. CLOZARIL no está aprobado para su uso en pacientes con psicosis relacionada con demencia [ver ADVERTENCIAS Y PRECAUCIONES].
DESCRIPCIÓN
CLOZARIL® (clozapina), un fármaco antipsicótico atípico, es un derivado de dibenzodiazepina tricíclica, 8-cloro-11-(4-metil-1-piperazinil)-5H-dibenzo [b,e] [1,4] diazepina. La fórmula estructural es
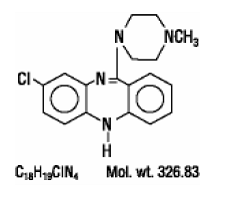
CLOZARIL está disponible en tabletas de color amarillo pálido de 25 mg y 100 mg para administración oral.
Ingrediente activo: clozapina
Los ingredientes inactivos son dióxido de silicio coloidal, lactosa, estearato de magnesio, povidona, almidón (maíz) y talco.
INDICACIONES
Esquizofrenia resistente al tratamiento
CLOZARIL 50 mg está indicado para el tratamiento de pacientes gravemente enfermos con esquizofrenia que no responden adecuadamente al tratamiento antipsicótico estándar. Debido a los riesgos de neutropenia severa y convulsiones asociados con su uso, CLOZARIL debe usarse solo en pacientes que no respondieron adecuadamente al tratamiento antipsicótico estándar [ver ADVERTENCIAS Y PRECAUCIONES ].
La eficacia de CLOZARIL en la esquizofrenia resistente al tratamiento se demostró en un estudio de 6 semanas, aleatorizado, doble ciego, con control activo que comparó CLOZARIL y clorpromazina en pacientes que habían fracasado con otros antipsicóticos [ver Estudios clínicos ].
Reducción del riesgo de conducta suicida recurrente en esquizofrenia o trastorno esquizoafectivo
CLOZARIL está indicado para reducir el riesgo de conducta suicida recurrente en pacientes con esquizofrenia o trastorno esquizoafectivo que se considera que tienen un riesgo crónico de volver a experimentar una conducta suicida, según la historia y el estado clínico reciente. El comportamiento suicida se refiere a las acciones de un paciente que lo ponen en riesgo de muerte.
La eficacia de CLOZARIL para reducir el riesgo de conducta suicida recurrente se demostró durante un período de tratamiento de dos años en el ensayo InterSePT™ [ver Estudios clínicos ].
DOSIFICACIÓN Y ADMINISTRACIÓN
Pruebas de laboratorio requeridas antes del inicio y durante la terapia
Antes de iniciar el tratamiento con CLOZARIL, se debe obtener un ANC de referencia. El ANC inicial debe ser de al menos 1500/μl para la población general y de al menos 1000/μl para pacientes con neutropenia étnica benigna (BEN) documentada. Para continuar el tratamiento, el ANC debe ser monitoreado regularmente [ver ADVERTENCIAS Y PRECAUCIONES ].
Información de dosificación
La dosis inicial es de 12,5 mg una o dos veces al día. La dosis diaria total se puede aumentar en incrementos de 25 mg a 50 mg por día, si se tolera bien, para lograr una dosis objetivo de 300 mg a 450 mg por día (administrada en dosis divididas) al final de 2 semanas. Posteriormente, la dosis puede incrementarse una o dos veces por semana, en incrementos de hasta 100 mg. La dosis máxima es de 900 mg por día. Para minimizar el riesgo de hipotensión ortostática, bradicardia y síncope, es necesario usar esta dosis inicial baja, programa de titulación gradual y dosis divididas [ver ADVERTENCIAS Y PRECAUCIONES ].
CLOZARIL se puede tomar con o sin alimentos [ver Farmacocinética ].
Tratamiento de mantenimiento
Generalmente, los pacientes que responden a CLOZARIL deben continuar el tratamiento de mantenimiento con su dosis efectiva más allá del episodio agudo.
Interrupción del tratamiento
El método de interrupción del tratamiento variará según el último ANC del paciente:
- Consulte las Tablas 2 o 3 para conocer el control adecuado del RAN en función del nivel de neutropenia si es necesaria la interrupción abrupta del tratamiento debido a una neutropenia de moderada a grave.
- Reduzca la dosis gradualmente durante un período de 1 a 2 semanas si se planea terminar la terapia con CLOZARIL 50 mg y no hay evidencia de neutropenia moderada a severa.
- Para la interrupción abrupta de la clozapina por un motivo no relacionado con la neutropenia, se recomienda continuar con la monitorización del ANC existente para los pacientes de la población general hasta que su ANC sea ≥1500/μL y para los pacientes con BEN hasta que su ANC sea ≥1000/μL o por encima de su valor inicial.
- Se requiere monitoreo adicional del ANC para cualquier paciente que informe el inicio de fiebre (temperatura de 38.5 °C o 101.3 °F, o más) durante las 2 semanas posteriores a la interrupción [ver ADVERTENCIAS Y PRECAUCIONES ].
- Vigile cuidadosamente a todos los pacientes en busca de recurrencia de síntomas psicóticos y síntomas relacionados con el rebote colinérgico, como sudoración profusa, dolor de cabeza, náuseas, vómitos y diarrea.
Reinicio del tratamiento
Cuando reinicie CLOZARIL en pacientes que hayan discontinuado CLOZARIL (es decir, 2 días o más desde la última dosis), reinicie con 12,5 mg una o dos veces al día. Esto es necesario para minimizar el riesgo de hipotensión, bradicardia y síncope [ver ADVERTENCIAS Y PRECAUCIONES ]. Si esa dosis es bien tolerada, la dosis puede aumentarse a la dosis terapéutica anterior más rápidamente de lo recomendado para el tratamiento inicial.
Ajustes de dosis con el uso concomitante de inhibidores de CYP1A2, CYP2D6, CYP3A4 o inductores de CYP1A2, CYP3A4
Puede ser necesario ajustar la dosis en pacientes con el uso concomitante de: inhibidores potentes de CYP1A2 (p. ej., fluvoxamina, ciprofloxacina o enoxacina); inhibidores moderados o débiles de CYP1A2 (p. ej., anticonceptivos orales o cafeína); inhibidores de CYP2D6 o CYP3A4 (p. ej., cimetidina, escitalopram, eritromicina, paroxetina, bupropión, fluoxetina, quinidina, duloxetina, terbinafina o sertralina); inductores de CYP3A4 (p. ej., fenitoína, carbamazepina, hierba de San Juan y rifampicina); o inductores de CYP1A2 (p. ej., fumar tabaco) (Tabla 1) [ver INTERACCIONES CON LA DROGAS ].
Insuficiencia renal o hepática o metabolizadores deficientes CYP2D6
Puede ser necesario reducir la dosis de CLOZARIL 50 mg en pacientes con insuficiencia renal o hepática significativa, o en metabolizadores lentos de CYP2D6 [ver Uso en poblaciones específicas ].
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
CLOZARIL (clozapina) está disponible en comprimidos redondos, de color amarillo pálido, sin recubrimiento, de 25 mg, 50 mg y 100 mg, con una ranura facilitada en un lado. Los comprimidos de Clozaril (clozapina) de 200 mg son comprimidos sin recubrir, de color amarillo pálido, en forma de cápsula, con una ranura facilitada en un lado.
CLOZARIL® (clozapina) Tabletas
25 miligramos
Comprimido redondo, de color amarillo pálido, sin recubrimiento. Grabado con “CLOZARIL” una vez en la periferia de un lado. Grabado con una partitura facilitada y "25" una vez en el otro lado. Botella de 100 .......... CDN 69809-0126-05
50 miligramos
Comprimido redondo, de color amarillo pálido, sin recubrimiento. Grabado con “CLOZARIL” una vez en la periferia de un lado. Grabado "50", una partitura facilitada y "mg" en el otro lado. Botella de 100 .......... CDN 69809-0130-05
100 miligramos
Comprimido redondo, de color amarillo pálido, sin recubrimiento. Grabado con “CLOZARIL” una vez en la periferia de un lado. Grabado con una partitura facilitada y "100" una vez en el otro lado. Botella de 100 .......... CDN 69809-0127-05
200 miligramos
Comprimido sin recubrir, de color amarillo pálido, con forma de cápsula. Grabado con “CLOZARIL” una vez en un lado. Grabado con "200", una partitura facilitada y "mg" en el otro lado. Botella de 100 .......... CDN 69809-0135-05
Almacenamiento y manipulación
La temperatura de almacenamiento no debe exceder los 30°C (86°F).
Mantener fuera del alcance de los niños.
Distribuido por: HLS Therapeutics (EE. UU.), Inc., Rosemont, PA 19010, (844) 457-8721. Revisado: febrero de 2021
EFECTOS SECUNDARIOS
Las siguientes reacciones adversas se analizan con más detalle en otras secciones de la etiqueta:
- Neutropenia severa [ver ADVERTENCIAS Y PRECAUCIONES ]
- Hipotensión ortostática, bradicardia y síncope [ver ADVERTENCIAS Y PRECAUCIONES ]
- Caídas [ver ADVERTENCIAS Y PRECAUCIONES ]
- Convulsiones [ver ADVERTENCIAS Y PRECAUCIONES ]
- Miocarditis, miocardiopatía e insuficiencia de la válvula mitral [ver ADVERTENCIAS Y PRECAUCIONES ]
- Aumento de la mortalidad en pacientes de edad avanzada con psicosis relacionada con demencia [ver ADVERTENCIAS Y PRECAUCIONES ]
- Hipomotilidad gastrointestinal con complicaciones graves [Ver ADVERTENCIAS Y PRECAUCIONES ]
- Eosinofilia [ver ADVERTENCIAS Y PRECAUCIONES ]
- Prolongación del intervalo QT [ver ADVERTENCIAS Y PRECAUCIONES ]
- Cambios metabólicos (hiperglucemia y diabetes mellitus, dislipidemia y aumento de peso) [ver ADVERTENCIAS Y PRECAUCIONES ]
- Síndrome neuroléptico maligno [ver ADVERTENCIAS Y PRECAUCIONES ]
- Hepatotoxicidad [ver ADVERTENCIAS Y PRECAUCIONES ]
- Fiebre [ver ADVERTENCIAS Y PRECAUCIONES ]
- Embolia pulmonar [ver ADVERTENCIAS Y PRECAUCIONES ]
- Toxicidad anticolinérgica [ver ADVERTENCIAS Y PRECAUCIONES ]
- Interferencia con el rendimiento cognitivo y motor [ver ADVERTENCIAS Y PRECAUCIONES ]
- Discinesia tardía [ver ADVERTENCIAS Y PRECAUCIONES ]
- Reacciones adversas cerebrovasculares [ver ADVERTENCIAS Y PRECAUCIONES ]
- Recurrencia de psicosis y rebote colinérgico después de una interrupción abrupta [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy diversas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica clínica.
Las reacciones adversas notificadas con mayor frecuencia (≥5 %) en los ensayos clínicos de CLOZARIL fueron: reacciones del SNC, que incluyen sedación, mareos/vértigo, dolor de cabeza y temblores; reacciones cardiovasculares, incluyendo taquicardia, hipotensión y síncope; reacciones del sistema nervioso autónomo, que incluyen hipersalivación, sudoración, sequedad de boca y alteraciones visuales; reacciones gastrointestinales, incluyendo estreñimiento y náuseas; y fiebre La Tabla 9 resume las reacciones adversas notificadas con mayor frecuencia (≥5%) en pacientes tratados con CLOZARIL (en comparación con pacientes tratados con clorpromazina) en el ensayo pivotal controlado de 6 semanas en esquizofrenia resistente al tratamiento.
La Tabla 10 resume las reacciones adversas informadas en pacientes tratados con CLOZARIL con una frecuencia del 2 % o más en todos los estudios de CLOZARIL (excluyendo el estudio InterSePT™ de 2 años). Estas tasas no se ajustan por la duración de la exposición.
La Tabla 11 resume las reacciones adversas notificadas con mayor frecuencia (>10 % del grupo de CLOZARIL o de olanzapina) en el estudio InterSePT™. Este fue un estudio de dos años adecuado y bien controlado que evaluó la eficacia de CLOZARIL en relación con la olanzapina para reducir el riesgo de comportamiento suicida en pacientes con esquizofrenia o trastorno esquizoafectivo. Las tasas no se ajustan según la duración de la exposición.
distonía
Efecto de clase
Los síntomas de distonía, contracciones anormales prolongadas de grupos musculares, pueden ocurrir en individuos susceptibles durante los primeros días de tratamiento. Los síntomas distónicos incluyen: espasmo de los músculos del cuello, que a veces progresa a opresión en la garganta, dificultad para tragar, dificultad para respirar y/o protrusión de la lengua. Si bien estos síntomas pueden ocurrir en dosis bajas, ocurren con mayor frecuencia y con mayor gravedad con alta potencia y en dosis más altas de fármacos antipsicóticos de primera generación. Se observa un riesgo elevado de distonía aguda en hombres y grupos de edad más jóvenes.
Experiencia posterior a la comercialización
Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación de clozapina. Debido a que estas reacciones son informadas voluntariamente por una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Sistema nervioso central
Delirio, EEG anormal, mioclono, parestesia, posible cataplejía, estado epiléptico, síntomas obsesivo-compulsivos, síndrome de piernas inquietas y reacciones adversas de rebote colinérgico posteriores a la interrupción.
Sistema cardiovascular
Fibrilación auricular o ventricular, taquicardia ventricular, palpitaciones, prolongación del intervalo QT, Torsades de Pointes, incompetencia de la válvula mitral asociada con miocardiopatía relacionada con clozapina, infarto de miocardio, paro cardíaco, miocarditis y edema periorbitario.
Sistema endocrino
Pseudofeocromocitoma
Sistema gastrointestinal
Pancreatitis aguda, disfagia, tumefacción de glándulas salivales, colitis, megacolon, isquemia intestinal o infarto.
Sistema Hepatobiliar
Colestasis, hepatitis, ictericia, hepatotoxicidad, esteatosis hepática, necrosis hepática, fibrosis hepática, cirrosis hepática, daño hepático (hepático, colestásico y mixto) e insuficiencia hepática.
Trastornos del sistema inmunológico
Angioedema, vasculitis leucocitoclástica.
Sistema urogenital
Nefritis intersticial aguda, enuresis nocturna, priapismo, insuficiencia renal y eyaculación retrógrada.
Trastornos de la piel y del tejido subcutáneo
Reacciones de hipersensibilidad: fotosensibilidad, vasculitis, eritema multiforme, trastorno de la pigmentación de la piel y síndrome de Stevens-Johnson.
Trastornos del sistema musculoesquelético y del tejido conjuntivo
Síndrome miasténico, rabdomiólisis y lupus eritematoso sistémico.
Sistema respiratorio
Aspiración, derrame pleural, neumonía, infección del tracto respiratorio inferior, apnea del sueño.
Sistema hemico y linfatico
Leucopenia leve, moderada o grave, agranulocitosis, granulocitopenia, disminución de glóbulos blancos, trombosis venosa profunda, hemoglobina/hematocrito elevados, aumento de la velocidad de sedimentación globular (VSG), sepsis, trombocitosis y trombocitopenia.
Trastornos de la visión
Glaucoma de ángulo estrecho.
Misceláneas
Elevación de creatina fosfoquinasa, hiperuricemia, hiponatremia, poliserositis y pérdida de peso.
INTERACCIONES CON LA DROGAS
Potencial de que otras drogas afecten a CLOZARIL
La clozapina es un sustrato para muchas isoenzimas del citocromo P450, en particular CYP1A2, CYP3A4 y CYP2D6. Tenga precaución cuando administre CLOZARIL 100 mg concomitantemente con medicamentos que sean inductores o inhibidores de estas enzimas.
Inhibidores de CYP1A2
El uso concomitante de CLOZARIL y los inhibidores de CYP1A2 puede aumentar los niveles plasmáticos de clozapina, lo que podría provocar reacciones adversas. Reduzca la dosis de CLOZARIL a un tercio de la dosis original cuando se coadministre CLOZARIL con inhibidores potentes de CYP1A2 (p. ej., fluvoxamina, ciprofloxacina o enoxacina). La dosis de CLOZARIL debe aumentarse a la dosis original cuando se interrumpa la coadministración de inhibidores potentes de CYP1A2 [ver DOSIFICACIÓN Y ADMINISTRACIÓN , FARMACOLOGÍA CLÍNICA ].
Los inhibidores moderados o débiles de CYP1A2 incluyen anticonceptivos orales y cafeína. Vigile de cerca a los pacientes cuando CLOZARIL se coadministre con estos inhibidores. Considere reducir la dosis de CLOZARIL 25 mg si es necesario [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Inhibidores de CYP2D6 y CYP3A4
El tratamiento concomitante con CLOZARIL e inhibidores de CYP2D6 o CYP3A4 (p. ej., cimetidina, escitalopram, eritromicina, paroxetina, bupropión, fluoxetina, quinidina, duloxetina, terbinafina o sertralina) puede aumentar los niveles de clozapina y provocar reacciones adversas [ver FARMACOLOGÍA CLÍNICA ]. Tenga cuidado y vigile de cerca a los pacientes cuando use tales inhibidores. Considere reducir la dosis de CLOZARIL 100mg [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Inductores CYP1A2 y CYP3A4
El tratamiento concomitante con medicamentos que inducen CYP1A2 o CYP3A4 puede disminuir la concentración plasmática de clozapina, lo que resulta en una disminución de la eficacia de CLOZARIL. El humo del tabaco es un inductor moderado de CYP1A2. Los inductores fuertes de CYP3A4 incluyen carbamazepina, fenitoína, hierba de San Juan y rifampicina. Puede ser necesario aumentar la dosis de CLOZARIL 50 mg si se usa concomitantemente con inductores de estas enzimas. Sin embargo, no se recomienda el uso concomitante de CLOZARIL e inductores potentes de CYP3A4 [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Considere reducir la dosis de CLOZARIL 50 mg cuando suspenda los inductores enzimáticos coadministrados; porque la interrupción de los inductores puede dar lugar a un aumento de los niveles plasmáticos de clozapina y un aumento del riesgo de reacciones adversas [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Fármacos anticolinérgicos
El tratamiento concomitante con clozapina y otros fármacos con actividad anticolinérgica (p. ej., benztropina, ciclobenzaprina, difenhidramina) puede aumentar el riesgo de toxicidad anticolinérgica y reacciones adversas gastrointestinales graves relacionadas con la hipomotilidad. Evite el uso concomitante de CLOZARIL con medicamentos anticolinérgicos cuando sea posible [ver ADVERTENCIAS Y PRECAUCIONES ].
Medicamentos que causan la prolongación del intervalo QT
Tenga cuidado cuando administre medicamentos concomitantes que prolonguen el intervalo QT o inhiban el metabolismo de la clozapina. Los medicamentos que causan la prolongación del intervalo QT incluyen: antipsicóticos específicos (p. ej., ziprasidona, iloperidona, clorpromazina, tioridazina, mesoridazina, droperidol y pimozida), antibióticos específicos (p. ej., eritromicina, gatifloxacina, moxifloxacina, esparfloxacina), antiarrítmicos de clase 1A (p. ej., quinidina, procainamida) o antiarrítmicos de Clase III (p. ej., amiodarona, sotalol) y otros (p. ej., pentamidina, acetato de levometadilo, metadona, halofantrina, mefloquina, mesilato de dolasetrón, probucol o tacrolimus) [ver ADVERTENCIAS Y PRECAUCIONES ].
Potencial de CLOZARIL para afectar a otras drogas
El uso concomitante de CLOZARIL 25 mg con otros fármacos metabolizados por CYP2D6 puede aumentar los niveles de estos sustratos de CYP2D6. Tenga cuidado cuando coadministre CLOZARIL 50 mg con otros medicamentos que son metabolizados por CYP2D6. Puede ser necesario usar dosis más bajas de tales medicamentos que las prescritas habitualmente. Estos fármacos incluyen antidepresivos específicos, fenotiazinas, carbamazepina y antiarrítmicos de tipo 1C (p. ej., propafenona, flecainida y encainida).
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Neutropenia severa
Fondo
CLOZARIL puede causar neutropenia (un recuento absoluto bajo de neutrófilos (ANC)), definido como una reducción por debajo de los niveles normales de neutrófilos en sangre antes del tratamiento. El ANC generalmente está disponible como un componente del conteo sanguíneo completo (CBC), incluido el diferencial, y es más relevante para la neutropenia inducida por fármacos que el conteo de glóbulos blancos (WBC). El ANC también se puede calcular mediante la siguiente fórmula: ANC es igual al recuento total de glóbulos blancos multiplicado por el porcentaje total de neutrófilos obtenido del diferencial ("segs" de neutrófilos más "bandas" de neutrófilos). Otros granulocitos (basófilos y eosinófilos) contribuyen mínimamente a la neutropenia y no es necesaria su medición [ver REACCIONES ADVERSAS ]. La neutropenia puede ser leve, moderada o grave (consulte las tablas 2 y 3). Para mejorar y estandarizar la comprensión, “neutropenia severa” reemplaza los términos anteriores leucopenia severa, granulocitopenia severa o agranulocitosis.
La neutropenia severa, ANC inferior a (
A continuación se proporcionan dos algoritmos de manejo separados, el primero para pacientes de la población general y el segundo para pacientes identificados con neutropenia inicial.
Tratamiento y seguimiento de CLOZARIL en la población general de pacientes (ver Tabla 2)
Obtenga un CBC, incluido el valor de ANC, antes de iniciar el tratamiento con CLOZARIL 25 mg para garantizar la presencia de un recuento de neutrófilos basal normal (igual o superior a 1500/μL) y permitir comparaciones posteriores. Los pacientes de la población general con un RAN igual o superior a (≥) 1500/μl se consideran dentro del rango normal (tabla 2) y son elegibles para iniciar el tratamiento. Se requiere un control semanal del RAN para todos los pacientes durante los primeros 6 meses de tratamiento. Si el ANC de un paciente permanece igual o superior a 1500/μL durante los primeros 6 meses de tratamiento, la frecuencia de control puede reducirse a cada 2 semanas durante los próximos 6 meses. Si el ANC permanece igual o superior a 1500/μL durante los segundos 6 meses de terapia continua, la frecuencia de control del ANC puede reducirse a una vez cada 4 semanas a partir de entonces.
Tratamiento y seguimiento de CLOZARIL en pacientes con neutropenia étnica benigna (ver Tabla 3)
La neutropenia étnica benigna (BEN, por sus siglas en inglés) es una afección que se observa en ciertos grupos étnicos cuyos valores promedio de ANC son más bajos que los rangos de laboratorio "estándar" para los neutrófilos. Se observa más comúnmente en personas de ascendencia africana (prevalencia aproximada de 25-50%), algunos grupos étnicos del Medio Oriente y en otros grupos étnicos no caucásicos con piel más oscura. BEN es más común en los hombres. Los pacientes con BEN tienen un número normal de células madre hematopoyéticas y una maduración mieloide, están sanos y no sufren infecciones repetidas o graves. No tienen mayor riesgo de desarrollar neutropenia inducida por CLOZARIL. Es posible que se necesite una evaluación adicional para determinar si la neutropenia inicial se debe a BEN. Considere la consulta de hematología antes de iniciar o durante el tratamiento con CLOZARIL 50 mg según sea necesario.
Los pacientes con BEN requieren un algoritmo ANC diferente para el manejo de CLOZARIL debido a sus niveles basales de ANC más bajos. La Tabla 3 proporciona pautas para el manejo del tratamiento con CLOZARIL 100 mg y el control del RAN en pacientes con BEN.
Pautas generales para el manejo de todos los pacientes con fiebre o con neutropenia
- Fiebre: Interrumpir CLOZARIL como medida de precaución en cualquier paciente que desarrolle fiebre, definida como una temperatura de 38.5°C [101.3°F] o más, y obtener un nivel de ANC. La fiebre es a menudo el primer signo de infección neutropénica.
- ANC inferior a 1000/μL: si se presenta fiebre en cualquier paciente con un ANC inferior a 1000/μL, inicie el estudio y el tratamiento apropiados para la infección y consulte las Tablas 2 o 3 para el manejo.
- Considere la consulta de hematología.
- Consulte Síndrome neuroléptico maligno [SNM] y fiebre en ADVERTENCIAS Y PRECAUCIONES e Instrucciones para Pacientes, bajo INFORMACIÓN DEL PACIENTE .
Reexposición después de un ANC inferior a 500/μL (neutropenia grave)
Para algunos pacientes que experimentan neutropenia grave relacionada con CLOZARIL, el riesgo de enfermedad psiquiátrica grave por interrumpir el tratamiento con CLOZARIL puede ser mayor que el riesgo de volver a exponerlo (p. ej., pacientes con enfermedad esquizofrénica grave que no tienen opciones de tratamiento distintas a CLOZARIL). Una consulta de hematología puede ser útil para decidir volver a desafiar a un paciente. Sin embargo, en general, no vuelva a tratar a los pacientes que desarrollan neutropenia grave con CLOZARIL o un producto de clozapina.
Si un paciente será reexpuesto, el médico debe considerar los umbrales proporcionados en las Tablas 2 y 3, el historial médico y psiquiátrico del paciente, una discusión con el paciente y su cuidador sobre los beneficios y riesgos de la reexposición de CLOZARIL 50 mg, y la severidad y características del episodio neutropénico.
Uso de CLOZARIL con otros medicamentos asociados con la neutropenia
No está claro si el uso concomitante de otros medicamentos que se sabe que causan neutropenia aumenta el riesgo o la gravedad de la neutropenia inducida por CLOZARIL. No existe una justificación científica sólida para evitar el tratamiento con CLOZARIL en pacientes tratados simultáneamente con estos medicamentos. Si CLOZARIL 100 mg se usa junto con un agente que se sabe que causa neutropenia (por ejemplo, algunos agentes quimioterapéuticos), considere monitorear a los pacientes más de cerca que las pautas de tratamiento proporcionadas en las Tablas 2 y 3. Consulte con el oncólogo tratante en pacientes que reciben quimioterapia concomitante.
Programa REMS de clozapina
CLOZARIL solo está disponible a través de un programa restringido bajo un REMS llamado Clozapine REMS Program debido al riesgo de neutropenia severa.
Los requisitos notables del programa REMS de clozapina incluyen:
- Los profesionales de la salud que prescriben CLOZARIL 25 mg deben estar certificados con el programa al inscribirse y completar la capacitación.
- Los pacientes que reciben CLOZARIL 100 mg deben estar inscritos en el programa y cumplir con los requisitos de control y pruebas de atención prenatal.
- Las farmacias que dispensan CLOZARIL 50 mg deben estar certificadas con el programa inscribiéndose y completando la capacitación y solo deben dispensar a los pacientes que son elegibles para recibir CLOZARIL
Más información está disponible en www.clozapinerems.com o 1-844-267-8678.
Hipotensión ortostática, bradicardia y síncope
Se han producido hipotensión, bradicardia, síncope y paro cardíaco con el tratamiento con clozapina. El riesgo es mayor durante el período de titulación inicial, particularmente con un aumento rápido de la dosis. Estas reacciones pueden ocurrir con la primera dosis, a dosis tan bajas como 12,5 mg. Estas reacciones pueden ser fatales. El síndrome es compatible con bradicardia refleja mediada neuralmente (NMRB).
El tratamiento debe comenzar con una dosis máxima de 12,5 mg una o dos veces al día. La dosis diaria total se puede aumentar en incrementos de 25 mg a 50 mg por día, si se tolera bien, hasta una dosis objetivo de 300 mg a 450 mg por día (administrada en dosis divididas) al final de 2 semanas. Posteriormente, la dosis puede incrementarse semanalmente o dos veces por semana, en incrementos de hasta 100 mg. La dosis máxima es de 900 mg por día. Use una titulación cuidadosa y un programa de dosificación dividido para minimizar el riesgo de reacciones cardiovasculares graves [ver DOSIFICACIÓN Y ADMINISTRACIÓN ]. Considere reducir la dosis si ocurre hipotensión. Cuando reinicie el tratamiento en pacientes que han tenido incluso un breve intervalo sin CLOZARIL (es decir, 2 días o más desde la última dosis), reinicie el tratamiento con 12,5 mg una o dos veces al día [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Use CLOZARIL con precaución en pacientes con enfermedad cardiovascular (antecedentes de infarto de miocardio o isquemia, insuficiencia cardíaca o anomalías de la conducción), enfermedad cerebrovascular y condiciones que predispondrían a los pacientes a la hipotensión (p. ej., uso concomitante de antihipertensivos, deshidratación e hipovolemia).
Caídas
CLOZARIL 25 mg puede causar somnolencia, hipotensión postural, inestabilidad motora y sensorial, lo que puede conducir a caídas y, en consecuencia, fracturas u otras lesiones. Para los pacientes con enfermedades, afecciones o medicamentos que podrían exacerbar estos efectos, complete las evaluaciones de riesgo de caídas al iniciar el tratamiento antipsicótico y de manera recurrente para los pacientes que reciben terapia antipsicótica a largo plazo.
convulsiones
Se ha estimado que ocurren convulsiones en asociación con el uso de clozapina con una incidencia acumulada en un año de aproximadamente 5%, con base en la aparición de una o más convulsiones en 61 de 1743 pacientes expuestos a clozapina durante sus pruebas clínicas antes de la comercialización nacional (es decir, , una tasa bruta del 3,5%). El riesgo de convulsiones está relacionado con la dosis. Inicie el tratamiento con una dosis baja (12,5 mg), titule lentamente y utilice dosis divididas.
Tenga cuidado al administrar CLOZARIL 50 mg a pacientes con antecedentes de convulsiones u otros factores de riesgo predisponentes para convulsiones (p. ej., traumatismo craneoencefálico u otra patología del SNC, uso de medicamentos que reducen el umbral convulsivo o abuso de alcohol). Debido al riesgo sustancial de convulsiones asociado con el uso de CLOZARIL, advierta a los pacientes sobre la participación en cualquier actividad en la que la pérdida repentina del conocimiento pueda causar un riesgo grave para ellos mismos o para otros (p. ej., conducir un automóvil, operar maquinaria compleja, nadar, escalar).
Miocarditis, miocardiopatía e insuficiencia de la válvula mitral
Se han producido miocarditis y cardiomiopatía con el uso de CLOZARIL. Estas reacciones pueden ser fatales. Suspender CLOZARIL 25 mg y obtener una evaluación cardíaca ante la sospecha de miocarditis o cardiomiopatía. En general, los pacientes con antecedentes de miocarditis o miocardiopatía asociada con clozapina no deben volver a recibir CLOZARIL. Sin embargo, si se considera que el beneficio del tratamiento con CLOZARIL 25 mg supera los riesgos potenciales de miocarditis o miocardiopatía recurrentes, el médico puede considerar una nueva provocación con CLOZARIL en consulta con un cardiólogo, después de una evaluación cardíaca completa y bajo estrecha vigilancia.
Considere la posibilidad de miocarditis o cardiomiopatía en pacientes que reciben CLOZARIL que presentan dolor torácico, disnea, taquicardia persistente en reposo, palpitaciones, fiebre, síntomas gripales, hipotensión, otros signos o síntomas de insuficiencia cardíaca o hallazgos electrocardiográficos (bajos voltajes, alteraciones del ST-T, arritmias, desviación del eje a la derecha y mala progresión de la onda R). La miocarditis se presenta con mayor frecuencia dentro de los primeros 2 meses de tratamiento con clozapina. Los síntomas de la miocardiopatía generalmente ocurren más tarde que la miocarditis asociada con la clozapina y generalmente después de 8 semanas de tratamiento. Sin embargo, la miocarditis y la cardiomiopatía pueden ocurrir en cualquier momento durante el tratamiento con CLOZARIL. Es común que los síntomas inespecíficos similares a los de la gripe, como malestar general, mialgia, dolor torácico pleurítico y febrícula, precedan a signos más evidentes de insuficiencia cardíaca. Los hallazgos típicos de laboratorio incluyen troponina I o T elevada, creatinina quinasa-MB elevada, eosinofilia periférica y proteína C reactiva (PCR) elevada. La radiografía de tórax puede demostrar agrandamiento de la silueta cardíaca y las imágenes cardíacas (ecocardiograma, estudios con radionucleótidos o cateterismo cardíaco) pueden revelar evidencia de disfunción ventricular izquierda. En pacientes a los que se les diagnosticó cardiomiopatía mientras tomaban CLOZARIL 50 mg, se ha informado insuficiencia de la válvula mitral. Estos casos informaron insuficiencia mitral leve o moderada en la ecocardiografía bidimensional. En pacientes con sospecha de miocardiopatía, considere un examen de eco-Doppler 2D para identificar la incompetencia de la válvula mitral.
Aumento de la mortalidad en pacientes ancianos con psicosis relacionada con demencia
Los pacientes de edad avanzada con psicosis relacionada con la demencia tratados con medicamentos antipsicóticos tienen un mayor riesgo de muerte. Los análisis de 17 ensayos controlados con placebo (duración modal de 10 semanas), principalmente en pacientes que tomaban fármacos antipsicóticos atípicos, revelaron un riesgo de muerte en pacientes tratados con fármacos de entre 1,6 y 1,7 veces el riesgo de muerte en pacientes tratados con placebo. En el transcurso de un ensayo controlado típico de 10 semanas, la tasa de muerte en los pacientes tratados con medicamentos fue de alrededor del 4,5 %, en comparación con una tasa de alrededor del 2,6 % en el grupo de placebo. Aunque las causas de muerte fueron variadas, la mayoría de las muertes parecían ser de naturaleza cardiovascular (p. ej., insuficiencia cardíaca, muerte súbita) o infecciosa (p. ej., neumonía). Los estudios observacionales sugieren que, al igual que los fármacos antipsicóticos atípicos, el tratamiento con fármacos antipsicóticos convencionales puede aumentar la mortalidad en esta población. No está claro hasta qué punto los hallazgos de aumento de la mortalidad en los estudios observacionales pueden atribuirse al fármaco antipsicótico en contraposición a algunas características de los pacientes. CLOZARIL no está aprobado para el tratamiento de pacientes con psicosis relacionada con demencia [ver ADVERTENCIA EN CAJA ].
Hipomotilidad gastrointestinal con complicaciones graves
Se han producido reacciones adversas gastrointestinales graves con el uso de CLOZARIL, principalmente debido a sus potentes efectos anticolinérgicos y la hipomotilidad gastrointestinal resultante. En la experiencia posterior a la comercialización, los efectos informados van desde el estreñimiento hasta el íleo paralítico. La mayor frecuencia de estreñimiento y el diagnóstico y tratamiento tardíos aumentaron el riesgo de complicaciones graves de hipomotilidad gastrointestinal, lo que resultó en obstrucción intestinal, impactación fecal, megacolon e isquemia intestinal o infarto [ver REACCIÓN ADVERSA ]. Estas reacciones han resultado en hospitalización, cirugía y muerte. El riesgo de reacciones adversas graves aumenta aún más con medicamentos anticolinérgicos (y otros medicamentos que disminuyen el peristaltismo gastrointestinal); por lo tanto, se debe evitar el uso concomitante cuando sea posible [ver ADVERTENCIAS Y PRECAUCIONES , INTERACCIONES CON LA DROGAS ].
Antes de iniciar CLOZARIL 50 mg, evalúe el estreñimiento y trate según sea necesario. Es posible que los síntomas subjetivos de estreñimiento no reflejen con precisión el grado de hipomotilidad gastrointestinal en los pacientes tratados con CLOZARIL. Por lo tanto, reevalúe con frecuencia la función intestinal prestando especial atención a cualquier cambio en la frecuencia o el carácter de las deposiciones, así como a los signos y síntomas de complicaciones de la hipomotilidad (p. ej., náuseas, vómitos, distensión abdominal, dolor abdominal). Si se identifica estreñimiento o hipomotilidad gastrointestinal, controle de cerca y trate de inmediato con los laxantes apropiados, según sea necesario, para prevenir complicaciones graves. Considere laxantes profilácticos en pacientes de alto riesgo.
eosinofilia
Se ha producido eosinofilia, definida como un recuento de eosinófilos en sangre superior a 700/μL, con el tratamiento con CLOZARIL 100 mg. En ensayos clínicos, aproximadamente el 1% de los pacientes desarrollaron eosinofilia. La eosinofilia relacionada con la clozapina generalmente ocurre durante el primer mes de tratamiento. En algunos pacientes se ha asociado con miocarditis, pancreatitis, hepatitis, colitis y nefritis. Tal compromiso de órganos podría ser consistente con una reacción a medicamentos con eosinofilia y síndrome de síntomas sistémicos (DRESS), también conocido como síndrome de hipersensibilidad inducida por medicamentos (DIHS). Si se desarrolla eosinofilia durante el tratamiento con CLOZARIL, evalúe de inmediato los signos y síntomas de reacciones sistémicas, como sarpullido u otros síntomas alérgicos, miocarditis u otra enfermedad específica de órganos asociada con la eosinofilia. Si se sospecha una enfermedad sistémica relacionada con CLOZARIL, suspenda CLOZARIL 50 mg de inmediato.
Si se identifica una causa de eosinofilia no relacionada con CLOZARIL 50 mg (p. ej., asma, alergias, enfermedad vascular del colágeno, infecciones parasitarias y neoplasias específicas), trate la causa subyacente y continúe con CLOZARIL.
La eosinofilia relacionada con la clozapina también ha ocurrido en ausencia de afectación de órganos y puede resolverse sin intervención. Hay informes de reexposición exitosa después de la interrupción de la clozapina, sin recurrencia de la eosinofilia. En ausencia de afectación de órganos, continuar con CLOZARIL bajo cuidadosa vigilancia. Si el recuento total de eosinófilos continúa aumentando durante varias semanas en ausencia de enfermedad sistémica, la decisión de interrumpir el tratamiento con CLOZARIL 25 mg y volver a administrarlo después de que disminuya el recuento de eosinófilos debe basarse en la evaluación clínica general, en consulta con un internista o hematólogo.
Prolongación del intervalo QT
Se han producido prolongación del intervalo QT, Torsade de Pointes y otras arritmias ventriculares potencialmente mortales, paro cardíaco y muerte súbita con el tratamiento con CLOZARIL 100 mg. Al prescribir CLOZARIL, considere la presencia de factores de riesgo adicionales para la prolongación del intervalo QT y reacciones cardiovasculares graves. Las condiciones que aumentan estos riesgos incluyen las siguientes: antecedentes de prolongación del intervalo QT, síndrome de QT prolongado, antecedentes familiares de síndrome de QT prolongado o muerte súbita cardíaca, arritmia cardíaca significativa, infarto de miocardio reciente, insuficiencia cardíaca no compensada, tratamiento con otros medicamentos que provoquen la prolongación del intervalo QT, tratamiento con medicamentos que inhiben el metabolismo de la clozapina y anomalías electrolíticas.
Antes de iniciar el tratamiento con CLOZARIL 25mg, realice un examen físico cuidadoso, historial médico y antecedentes de medicación concomitante. Considere obtener un ECG de referencia y un panel de química sérica. Corregir anomalías electrolíticas. Suspender CLOZARIL 25 mg si el intervalo QTc supera los 500 mseg. Si los pacientes experimentan síntomas compatibles con Torsades de Pointes u otras arritmias (p. ej., síncope, presíncope, mareos o palpitaciones), obtenga una evaluación cardíaca y suspenda CLOZARIL.
Tenga cuidado al administrar medicamentos concomitantes que prolonguen el intervalo QT o inhiban el metabolismo de CLOZARIL. Los medicamentos que causan la prolongación del intervalo QT incluyen: antipsicóticos específicos (p. ej., ziprasidona, iloperidona, clorpromazina, tioridazina, mesoridazina, droperidol, pimozida), antibióticos específicos (p. ej., eritromicina, gatifloxacina, moxifloxacina, esparfloxacina), medicamentos antiarrítmicos de Clase 1A (p. ej., quinidina, procainamida) o antiarrítmicos de Clase III (p. ej., amiodarona, sotalol), y otros (p. ej., pentamidina, acetato de levometadilo, metadona, halofantrina, mefloquina, mesilato de dolasetrón, probucol o tacrolimus). La clozapina se metaboliza principalmente por las isoenzimas CYP 1A2, 2D6 y 3A4. El tratamiento concomitante con inhibidores de estas enzimas puede aumentar la concentración de CLOZARIL [ver INTERACCIONES CON LA DROGAS y FARMACOLOGÍA CLÍNICA ].
La hipopotasemia y la hipomagnesemia aumentan el riesgo de prolongación del intervalo QT. La hipopotasemia puede resultar de la terapia con diuréticos, diarrea y otras causas. Tenga cuidado cuando trate a pacientes con riesgo de alteraciones electrolíticas significativas, particularmente hipopotasemia. Obtenga mediciones de referencia de los niveles séricos de potasio y magnesio, y controle periódicamente los electrolitos. Corregir las alteraciones electrolíticas antes de iniciar el tratamiento con CLOZARIL.
Cambios metabólicos
Los fármacos antipsicóticos atípicos, incluido CLOZARIL 50 mg, se han asociado con cambios metabólicos que pueden aumentar el riesgo cardiovascular y cerebrovascular. Estos cambios metabólicos incluyen hiperglucemia, dislipidemia y aumento de peso corporal. Si bien los fármacos antipsicóticos atípicos pueden producir algunos cambios metabólicos, cada fármaco de la clase tiene su propio perfil de riesgo específico.
Hiperglucemia y Diabetes Mellitus
Se ha informado hiperglucemia, en algunos casos extrema y asociada con cetoacidosis o coma hiperosmolar o muerte, en pacientes tratados con antipsicóticos atípicos, incluido CLOZARIL. La evaluación de la relación entre el uso de antipsicóticos atípicos y las anomalías de la glucosa se complica por la posibilidad de un mayor riesgo de diabetes mellitus en pacientes con esquizofrenia y la creciente incidencia de diabetes mellitus en la población general. Dados estos factores de confusión, la relación entre el uso de antipsicóticos atípicos y las reacciones adversas relacionadas con la hiperglucemia no se comprende por completo. Sin embargo, los estudios epidemiológicos sugieren un mayor riesgo de reacciones adversas relacionadas con la hiperglucemia emergentes del tratamiento en pacientes tratados con antipsicóticos atípicos. No se dispone de estimaciones precisas del riesgo de reacciones adversas relacionadas con la hiperglucemia en pacientes tratados con antipsicóticos atípicos.
Los pacientes con un diagnóstico establecido de diabetes mellitus que comienzan con CLOZARIL 100 mg deben ser monitoreados regularmente para detectar un empeoramiento del control de la glucosa. Los pacientes con factores de riesgo de diabetes mellitus (p. ej., obesidad, antecedentes familiares de diabetes) que inician un tratamiento con antipsicóticos atípicos deben someterse a pruebas de glucosa en sangre en ayunas al comienzo del tratamiento y periódicamente durante el tratamiento. Cualquier paciente tratado con antipsicóticos atípicos debe ser monitoreado por síntomas de hiperglucemia que incluyen polidipsia, poliuria, polifagia y debilidad. Los pacientes que desarrollan síntomas de hiperglucemia durante el tratamiento con antipsicóticos atípicos deben someterse a pruebas de glucosa en sangre en ayunas. En algunos casos, la hiperglucemia se resolvió cuando se suspendió el antipsicótico atípico; sin embargo, algunos pacientes requirieron la continuación del tratamiento antidiabético a pesar de la interrupción del fármaco sospechoso.
En un análisis de datos agrupados de 8 estudios en sujetos adultos con esquizofrenia, los cambios medios en la concentración de glucosa en ayunas en los grupos de CLOZARIL 50 mg y clorpromazina fueron +11 mg/dL y +4 mg/dL respectivamente. Una mayor proporción del grupo de CLOZARIL demostró aumentos categóricos desde el inicio en las concentraciones de glucosa en ayunas, en comparación con el grupo de clorpromazina (Tabla 4). Las dosis de CLOZARIL de 25 mg fueron de 100 a 900 mg por día (dosis modal media: 512 mg por día). La dosis máxima de clorpromazina fue de 1800 mg por día (dosis modal media: 1029 mg por día). La mediana de duración de la exposición fue de 42 días para CLOZARIL y clorpromazina.
dislipidemia
Se han producido alteraciones indeseables en los lípidos en pacientes tratados con antipsicóticos atípicos, incluido CLOZARIL. Se recomienda el monitoreo clínico, incluidas las evaluaciones de lípidos de seguimiento periódicas y de referencia en pacientes que usan CLOZARIL.
En un análisis de datos agrupados de 10 estudios en sujetos adultos con esquizofrenia, el tratamiento con CLOZARIL se asoció con aumentos en el colesterol total sérico. No se recopilaron datos sobre el colesterol LDL y HDL. El aumento medio del colesterol total fue de 13 mg/dl en el grupo de 25 mg de CLOZARIL y de 15 mg/dl en el grupo de clorpromazina. En un análisis de datos agrupados de 2 estudios en sujetos adultos con esquizofrenia, el tratamiento con CLOZARIL 50 mg se asoció con aumentos en los triglicéridos séricos en ayunas. El aumento medio de triglicéridos en ayunas fue de 71 mg/dL (54 %) en el grupo de CLOZARIL 100 mg y de 39 mg/dL (35 %) en el grupo de clorpromazina (Tabla 5). Además, el tratamiento con CLOZARIL se asoció con aumentos categóricos del colesterol total y los triglicéridos séricos, como se ilustra en la Tabla 6. La proporción de pacientes con aumentos categóricos del colesterol total o los triglicéridos en ayunas aumentó con la duración de la exposición. La mediana de duración de la exposición a CLOZARIL 50 mg y clorpromazina fue de 45 y 38 días, respectivamente. El rango de dosis de CLOZARIL fue de 100 mg a 900 mg diarios; la dosis máxima de clorpromazina fue de 1800 mg diarios.
Aumento de peso
Se ha producido aumento de peso con el uso de antipsicóticos, incluido CLOZARIL. Controlar el peso durante el tratamiento con CLOZARIL. La Tabla 7 resume los datos sobre el aumento de peso por la duración de la exposición agrupados de 11 estudios con CLOZARIL y comparadores activos. La mediana de duración de la exposición fue de 609, 728 y 42 días, en el grupo de CLOZARIL 25 mg, olanzapina y clorpromazina, respectivamente.
La Tabla 8 resume los datos agrupados de 11 estudios en sujetos adultos con esquizofrenia que demostraron un aumento de peso ≥7 % del peso corporal en relación con el valor inicial. La mediana de duración de la exposición fue de 609, 728 y 42 días, en el grupo de CLOZARIL, olanzapina y clorpromazina, respectivamente.
Síndrome neuroléptico maligno
Los medicamentos antipsicóticos, incluido CLOZARIL 50 mg, pueden causar un complejo de síntomas potencialmente mortal denominado síndrome neuroléptico maligno (SNM). Las manifestaciones clínicas del SNM incluyen hiperpirexia, rigidez muscular, estado mental alterado e inestabilidad autonómica (pulso o presión arterial irregulares, taquicardia, diaforesis y arritmias cardíacas). Los hallazgos asociados pueden incluir creatina fosfoquinasa elevada (CPK), mioglobinuria, rabdomiolisis e insuficiencia renal aguda.
La evaluación diagnóstica de los pacientes con este síndrome es complicada. Es importante considerar la presencia de otras afecciones médicas graves (p. ej., neutropenia grave, infección, golpe de calor, patología primaria del SNC, toxicidad anticolinérgica central, síntomas extrapiramidales y fiebre medicamentosa).
El manejo del SNM debe incluir (1) la interrupción inmediata de los medicamentos antipsicóticos y otros medicamentos que no sean esenciales para la terapia concurrente, (2) tratamiento sintomático intensivo y control médico, y (3) tratamiento de condiciones médicas comórbidas. No existe un acuerdo general sobre los tratamientos farmacológicos específicos para el SNM.
Si un paciente requiere tratamiento con medicamentos antipsicóticos después de la recuperación del SNM, se debe considerar cuidadosamente la posible reintroducción de la terapia con medicamentos. El NMS puede reaparecer. Vigilar de cerca si se reinicia el tratamiento con antipsicóticos.
Ha ocurrido SNM con la monoterapia con CLOZARIL y con medicamentos activos en el SNC concomitantes, incluido el litio.
hepatotoxicidad
En estudios posteriores a la comercialización en pacientes tratados con clozapina [ver REACCIONES ADVERSAS ]. Vigilar la aparición de signos y síntomas de hepatotoxicidad como fatiga, malestar general, anorexia, náuseas, ictericia, bilirrubinemia, coagulopatía y encefalopatía hepática. Realice pruebas de suero para detectar daño hepático y considere suspender el tratamiento de forma permanente si la hepatitis o las elevaciones de transaminasas combinadas con otros síntomas sistémicos se deben a la clozapina.
Fiebre
Durante la terapia con clozapina, los pacientes han experimentado fiebre transitoria relacionada con la clozapina. La incidencia máxima es dentro de las primeras 3 semanas de tratamiento. Si bien esta fiebre es generalmente benigna y autolimitada, puede requerir la interrupción del tratamiento. La fiebre puede estar asociada con un aumento o disminución en el recuento de glóbulos blancos. Evalúe cuidadosamente a los pacientes con fiebre para descartar neutropenia grave o infección. Considere la posibilidad de NMS [ver ADVERTENCIAS Y PRECAUCIONES ].
Embolia pulmonar
Se ha producido embolia pulmonar y trombosis venosa profunda en pacientes tratados con CLOZARIL. Considere la posibilidad de embolia pulmonar en pacientes que presentan trombosis venosa profunda, disnea aguda, dolor torácico u otros signos y síntomas respiratorios. No está claro si la embolia pulmonar y la trombosis venosa profunda se pueden atribuir a la clozapina oa algunas características de los pacientes.
Toxicidad anticolinérgica
CLOZARIL 50mg tiene potentes efectos anticolinérgicos. El tratamiento con CLOZARIL puede resultar en toxicidad anticolinérgica periférica y del SNC, especialmente en dosis más altas, o en situaciones de sobredosis [ver SOBREDOSIS ]. Usar con precaución en pacientes con un diagnóstico actual o antecedentes de estreñimiento, retención urinaria, hipertrofia prostática clínicamente significativa u otras afecciones en las que los efectos anticolinérgicos pueden provocar reacciones adversas significativas. Cuando sea posible, evite el uso concomitante con otros medicamentos anticolinérgicos porque aumenta el riesgo de toxicidad anticolinérgica o reacciones adversas gastrointestinales graves [ver ADVERTENCIAS Y PRECAUCIONES , INTERACCIONES CON LA DROGAS ].
Interferencia con el rendimiento cognitivo y motor
CLOZARIL puede causar sedación y deterioro del desempeño cognitivo y motor. Advierta a los pacientes sobre el manejo de maquinaria peligrosa, incluidos los automóviles, hasta que estén razonablemente seguros de que CLOZARIL no los afecta negativamente. Estas reacciones pueden estar relacionadas con la dosis. Considere reducir la dosis si ocurren.
Discinesia tardía
Se ha producido discinesia tardía (TD) en pacientes tratados con medicamentos antipsicóticos, incluido CLOZARIL. El síndrome consiste en movimientos discinéticos involuntarios potencialmente irreversibles. Se cree que el riesgo de DT y la probabilidad de que se vuelva irreversible aumentan con la mayor duración del tratamiento y las dosis acumuladas totales más altas. Sin embargo, el síndrome puede desarrollarse después de períodos de tratamiento relativamente breves con dosis bajas. Prescriba CLOZARIL de la manera que sea más probable que minimice el riesgo de desarrollar DT. Use la dosis efectiva más baja y la duración más corta necesaria para controlar los síntomas. Evaluar periódicamente la necesidad de continuar el tratamiento. Considere suspender el tratamiento si ocurre DT. Sin embargo, algunos pacientes pueden requerir tratamiento con CLOZARIL 100mg a pesar de la presencia del síndrome.
No existe un tratamiento conocido para la TD. Sin embargo, el síndrome puede remitir parcial o completamente si se interrumpe el tratamiento. El tratamiento antipsicótico, en sí mismo, puede suprimir (o suprimir parcialmente) los signos y síntomas, y tiene el potencial de enmascarar el proceso subyacente. Se desconoce el efecto de la supresión de los síntomas en el curso a largo plazo de la DT.
Reacciones adversas cerebrovasculares
En ensayos controlados, los pacientes de edad avanzada con psicosis relacionada con la demencia tratados con algunos antipsicóticos atípicos tuvieron un mayor riesgo (en comparación con el placebo) de reacciones adversas cerebrovasculares (p. ej., accidente cerebrovascular, ataque isquémico transitorio), incluidas muertes. Se desconoce el mecanismo de este aumento del riesgo. No se puede excluir un mayor riesgo para CLOZARIL u otros antipsicóticos u otras poblaciones de pacientes. CLOZARIL 50 mg debe usarse con precaución en pacientes con factores de riesgo de reacciones adversas cerebrovasculares.
Recurrencia de psicosis y rebote colinérgico tras suspensión brusca de CLOZARIL
Si es necesaria la interrupción abrupta de CLOZARIL (debido a neutropenia severa u otra condición médica, por ejemplo) [ver DOSIFICACIÓN Y ADMINISTRACIÓN , ADVERTENCIAS Y PRECAUCIONES ], vigile cuidadosamente la recurrencia de síntomas psicóticos y reacciones adversas relacionadas con el rebote colinérgico, como sudoración profusa, dolor de cabeza, náuseas, vómitos y diarrea.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
Carcinogénesis
No se demostró potencial carcinogénico en estudios a largo plazo en ratones y ratas a dosis de hasta 0,3 veces y 0,4 veces, respectivamente, la dosis máxima recomendada en humanos (MRHD) de 900 mg/día sobre la base de mg/m² de área de superficie corporal.
mutagénesis
La clozapina no fue genotóxica cuando se probó en las siguientes pruebas de mutaciones genéticas y aberraciones cromosómicas: la prueba bacteriana de Ames, el V79 de mamífero in vitro en células de hámster chino, la síntesis de ADN no programada in vitro en hepatocitos de rata o el ensayo de micronúcleo in vivo en ratones.
Deterioro de la fertilidad
La clozapina no tuvo efecto sobre ningún parámetro de fertilidad, embarazo, peso fetal o desarrollo posnatal cuando se administró por vía oral a ratas macho 70 días antes del apareamiento y a ratas hembra durante 14 días antes del apareamiento en dosis de hasta 0,4 veces la MRHD de 900 mg/día en una base de área de superficie corporal mg/m².
Uso en poblaciones específicas
El embarazo
Embarazo Categoría B
Resumen de riesgos
No hay estudios adecuados o bien controlados de clozapina en mujeres embarazadas.
Se han realizado estudios de reproducción en ratas y conejos a dosis de hasta 0,4 y 0,9 veces, respectivamente, la dosis máxima recomendada en humanos (DMRH) de 900 mg/día sobre la base de mg/m² de superficie corporal. Los estudios no revelaron evidencia de alteración de la fertilidad o daño al feto debido a la clozapina. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, CLOZARIL debe usarse durante el embarazo solo si es claramente necesario.
Consideraciones clínicas
Considere el riesgo de exacerbación de la psicosis al suspender o cambiar el tratamiento con medicamentos antipsicóticos durante el embarazo y el posparto. Considere la detección temprana de diabetes gestacional para pacientes tratadas con medicamentos antipsicóticos [ver ADVERTENCIAS Y PRECAUCIONES ]. Los recién nacidos expuestos a fármacos antipsicóticos durante el tercer trimestre del embarazo corren el riesgo de presentar síntomas extrapiramidales y/o de abstinencia después del parto. Vigile a los recién nacidos para detectar síntomas de agitación, hipertonía, hipotonía, temblor, somnolencia, dificultad respiratoria y dificultades para alimentarse. La gravedad de las complicaciones puede variar desde síntomas autolimitados hasta algunos recién nacidos que requieren apoyo en la unidad de cuidados intensivos y hospitalización prolongada.
Datos de animales
En estudios de desarrollo embriofetal, la clozapina no tuvo efectos sobre los parámetros maternos, el tamaño de las camadas o los parámetros fetales cuando se administró por vía oral a ratas y conejas preñadas durante el período de organogénesis en dosis de hasta 0,4 y 0,9 veces, respectivamente, la MRHD de 900 mg/día. sobre la base de mg/m² de superficie corporal.
En estudios de desarrollo peri/postnatal, se administró clozapina a ratas hembra preñadas durante el último tercio del embarazo y hasta el día 21 posparto. Se realizaron observaciones de fetos al nacer y durante el período posnatal; se permitió que las crías alcanzaran la madurez sexual y se aparearon. La clozapina provocó una disminución en el peso corporal materno, pero no tuvo efectos sobre el tamaño de la camada o el peso corporal de las generaciones F1 o F2 en dosis de hasta 0,4 veces la MRHD de 900 mg/día sobre la base de mg/m² de área de superficie corporal.
Madres lactantes
CLOZARIL 50mg está presente en la leche humana. Debido a la posibilidad de que CLOZARIL produzca reacciones adversas graves en lactantes, se debe tomar la decisión de suspender la lactancia o suspender el fármaco, teniendo en cuenta la importancia del fármaco para la madre.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos.
Uso geriátrico
No ha habido un número suficiente de pacientes geriátricos en estudios clínicos que utilizan CLOZARIL 50 mg para determinar si los mayores de 65 años difieren de los sujetos más jóvenes en su respuesta a CLOZARIL.
Puede ocurrir hipotensión ortostática y taquicardia con el tratamiento con CLOZARIL 50 mg [ver ADVERTENCIA EN CAJA y ADVERTENCIAS Y PRECAUCIONES ]. Los pacientes de edad avanzada, en particular aquellos con un funcionamiento cardiovascular comprometido, pueden ser más susceptibles a estos efectos.
Los pacientes de edad avanzada pueden ser particularmente susceptibles a los efectos anticolinérgicos de CLOZARIL, como retención urinaria y estreñimiento [ver ADVERTENCIAS Y PRECAUCIONES ].
Seleccione cuidadosamente las dosis de CLOZARIL 50 mg en pacientes de edad avanzada, teniendo en cuenta su mayor frecuencia de disminución de la función hepática, renal o cardíaca, así como otras enfermedades concomitantes y otra terapia con medicamentos. La experiencia clínica sugiere que la prevalencia de la discinesia tardía parece ser mayor entre los ancianos; especialmente mujeres mayores [ver ADVERTENCIAS Y PRECAUCIONES ].
Pacientes con insuficiencia renal o hepática
Puede ser necesaria una reducción de la dosis en pacientes con deterioro significativo de la función renal o hepática. Las concentraciones de clozapina pueden aumentar en estos pacientes, porque la clozapina se metaboliza casi por completo y luego se excreta [ver DOSIFICACIÓN Y ADMINISTRACIÓN , FARMACOLOGÍA CLÍNICA ].
Metabolizadores deficientes CYP2D6
Puede ser necesaria una reducción de la dosis en pacientes que son metabolizadores lentos de CYP2D6. Las concentraciones de clozapina pueden aumentar en estos pacientes, porque la clozapina se metaboliza casi por completo y luego se excreta [ver DOSIFICACIÓN Y ADMINISTRACIÓN , FARMACOLOGÍA CLÍNICA ].
Pacientes de hospicio
Para los pacientes de cuidados paliativos (es decir, pacientes con enfermedades terminales con una esperanza de vida estimada de seis meses o menos), el prescriptor puede reducir la frecuencia de monitoreo ANC a una vez cada 6 meses, después de hablar con el paciente y su cuidador. Las decisiones de tratamiento individuales deben sopesar la importancia de monitorear la atención prenatal en el contexto de la necesidad de controlar los síntomas psiquiátricos y la enfermedad terminal del paciente.
SOBREDOSIS
Experiencia de sobredosis
Los signos y síntomas asociados con la sobredosis de clozapina informados con mayor frecuencia son: sedación, delirio, coma, taquicardia, hipotensión, depresión o insuficiencia respiratoria; e hipersalivación. Hay informes de neumonía por aspiración, arritmias cardíacas y convulsiones. Se han informado sobredosis fatales con clozapina, generalmente en dosis superiores a 2500 mg. También ha habido informes de pacientes que se recuperan de sobredosis muy superiores a 4 g.
Manejo de sobredosis
No existe un antídoto específico disponible para una sobredosis de CLOZARIL. Establecer y mantener una vía aérea; garantizar una adecuada oxigenación y ventilación. Vigilar el estado cardíaco y los signos vitales. Use medidas generales sintomáticas y de apoyo. Considere la posibilidad de participación de múltiples drogas.
Comuníquese con un centro de control de envenenamiento certificado para obtener la información más actualizada sobre el manejo de sobredosis (1-800Â222-1222).
CONTRAINDICACIONES
CLOZARIL está contraindicado en pacientes con antecedentes de hipersensibilidad grave a la clozapina (p. ej., fotosensibilidad, vasculitis, eritema multiforme o síndrome de Stevens-Johnson) o cualquier otro componente de CLOZARIL [ver REACCIONES ADVERSAS ].
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
Se desconoce el mecanismo de acción de la clozapina. Sin embargo, se ha propuesto que la eficacia terapéutica de la clozapina en la esquizofrenia está mediada por el antagonismo de los receptores de dopamina tipo 2 (D2) y serotonina tipo 2A (5ÂHT2A). CLOZARIL también actúa como antagonista de los receptores adrenérgicos, colinérgicos, histaminérgicos y otros receptores dopaminérgicos y serotoninérgicos.
Farmacodinámica
La clozapina demostró afinidad de unión a los siguientes receptores: histamina H1 (Ki 1,1 nM), adrenérgico α1A (Ki 1,6 nM), serotonina 5-HT6 (Ki 4 nM), serotonina 5-HT2A (Ki 5,4 nM), muscarínico M1 (Ki 6,2 nM), serotonina 5-HT7 (Ki 6,3 nM), serotonina 5-HT2C (Ki 9,4 nM), dopamina D4 (Ki 24 nM), adrenérgico α2A (Ki 90 nM), serotonina 5-HT3 (Ki 95 nM), serotonina 5-HT1A (Ki 120 nM), dopamina D2 (Ki 160 nM), dopamina D1 (Ki 270 nM), dopamina D5 (Ki 454 nM) y dopamina D3 (Ki 555 nM).
La clozapina provoca poca o ninguna elevación de la prolactina.
Los estudios clínicos de electroencefalograma (EEG) demostraron que la clozapina aumenta la actividad delta y theta y reduce las frecuencias alfa dominantes. Se produce una sincronización mejorada. También pueden desarrollarse actividad de ondas agudas y complejos de puntas y ondas. Los pacientes han notificado una intensificación de la actividad onírica durante el tratamiento con clozapina. Se encontró que el sueño REM aumentó al 85% del tiempo total de sueño. En estos pacientes, el inicio del sueño REM ocurrió casi inmediatamente después de conciliar el sueño.
Farmacocinética
Absorción
En humanos, las tabletas de CLOZARIL (25 mg y 100 mg) tienen la misma biodisponibilidad que una solución de CLOZARIL. Luego de la administración oral de CLOZARIL 100 mg dos veces al día, la concentración plasmática máxima promedio en el estado estacionario fue de 319 ng/mL (rango: 102 a 771 ng/mL), ocurriendo en un promedio de 2.5 horas (rango: 1 a 6 horas) después de dosificación La concentración mínima promedio en el estado estacionario fue de 122 ng/mL (rango: 41 a 343 ng/mL), después de una dosificación de 100 mg dos veces al día. Los alimentos no parecen afectar la biodisponibilidad sistémica de CLOZARIL. Así, CLOZARIL 50mg puede administrarse con o sin alimentos.
Distribución
La clozapina se une aproximadamente en un 97 % a las proteínas séricas. La interacción entre la clozapina y otros fármacos altamente ligados a proteínas no ha sido completamente evaluada pero puede ser importante [ver INTERACCIONES CON LA DROGAS ].
Metabolismo y excreción
La clozapina se metaboliza casi por completo antes de la excreción y solo se detectan trazas de fármaco inalterado en la orina y las heces. La clozapina es un sustrato para muchas isoenzimas del citocromo P450, en particular CYP1A2, CYP2D6 y CYP3A4. Aproximadamente el 50% de la dosis administrada se excreta en la orina y el 30% en las heces. Los derivados desmetilados, hidroxilados y N-óxido son componentes tanto de la orina como de las heces. Las pruebas farmacológicas han demostrado que el metabolito desmetilado (norclozapina) tiene solo una actividad limitada, mientras que los derivados hidroxilados y N-óxido estaban inactivos. La vida media de eliminación media de clozapina después de una dosis única de 75 mg fue de 8 horas (rango: 4 a 12 horas), en comparación con una vida media de eliminación media de 12 horas (rango: 4 a 66 horas), después de alcanzar el estado de equilibrio con dosis de 100 mg dos veces al día.
Una comparación de la administración de dosis única y dosis múltiples de clozapina demostró que la vida media de eliminación aumentó significativamente después de dosis múltiples en relación con la administración de dosis única, lo que sugiere la posibilidad de una farmacocinética dependiente de la concentración. Sin embargo, en el estado estacionario, se observaron cambios aproximadamente proporcionales a la dosis con respecto al AUC (área bajo la curva), las concentraciones plasmáticas máximas y mínimas de clozapina después de la administración de 37,5, 75 y 150 mg dos veces al día.
Estudios de interacción fármaco-fármaco
fluvoxamina
Se realizó un estudio farmacocinético en 16 pacientes esquizofrénicos que recibieron clozapina en condiciones de estado estacionario. Después de la coadministración de fluvoxamina durante 14 días, las concentraciones mínimas medias de clozapina y sus metabolitos, N-desmetilclozapina y N-óxido de clozapina, se elevaron aproximadamente tres veces en comparación con las concentraciones basales en estado estacionario.
paroxetina, fluoxetina y sertralina
En un estudio de pacientes esquizofrénicos (n=14) que recibieron clozapina en condiciones de estado estacionario, la coadministración de paroxetina produjo solo cambios menores en los niveles de clozapina y sus metabolitos. Sin embargo, otros informes publicados describen elevaciones modestas (menos del doble) de las concentraciones de clozapina y metabolitos cuando se toma clozapina con paroxetina, fluoxetina y sertralina.
Estudios Poblacionales Específicos
Insuficiencia renal o hepática
No se realizaron estudios farmacocinéticos específicos para investigar los efectos de la insuficiencia renal o hepática en la farmacocinética de la clozapina. Es probable que las concentraciones plasmáticas de clozapina sean más altas en pacientes con insuficiencia renal o hepática significativa cuando se les administran las dosis habituales.
Metabolizadores deficientes CYP2D6
Un subconjunto (3%-10%) de la población tiene actividad reducida de CYP2D6 (metabolizadores lentos de CYP2D6). Estos individuos pueden desarrollar concentraciones plasmáticas de clozapina más altas de lo esperado cuando se les administran las dosis habituales.
Estudios clínicos
Esquizofrenia resistente al tratamiento
La eficacia de CLOZARIL 100 mg en la esquizofrenia resistente al tratamiento se estableció en un estudio multicéntrico, aleatorizado, doble ciego, con control activo (clorpromazina) en pacientes con un diagnóstico de esquizofrenia según el DSM-III que tenían respuestas inadecuadas a al menos 3 antipsicóticos diferentes ( de al menos 2 clases químicas diferentes) durante los 5 años anteriores. Los ensayos con antipsicóticos deben haberse juzgado adecuados; las dosis de antipsicóticos deben haber sido equivalentes o superiores a 1000 mg por día de clorpromazina durante un período de al menos 6 semanas, cada una sin una reducción significativa de los síntomas. No debe haber habido ningún período de buen funcionamiento dentro de los 5 años anteriores. Los pacientes deben haber tenido una puntuación inicial de al menos 45 en la escala de calificación psiquiátrica breve calificada por el investigador (BPRS). En la BPRS de 18 ítems, 1 indica ausencia de síntomas y 7 indica síntomas graves; la puntuación total potencial máxima de la BPRS es 126. Al inicio del estudio, la puntuación media de la BPRS fue de 61. Además, los pacientes deben haber obtenido una puntuación de al menos 4 en al menos dos de los siguientes cuatro elementos individuales de la BPRS: desorganización conceptual, suspicacia, alucinaciones. comportamiento y contenido inusual del pensamiento. Los pacientes deben haber tenido una puntuación en la escala de gravedad de impresiones clínicas globales de al menos 4 (moderadamente enfermos).
En la fase preliminar prospectiva del ensayo, todos los pacientes (N=305) recibieron inicialmente un tratamiento simple ciego con haloperidol (la dosis media fue de 61 mg al día) durante 6 semanas. Más del 80% de los pacientes completaron el ensayo de 6 semanas. Los pacientes con una respuesta inadecuada al haloperidol (n=268) fueron aleatorizados a tratamiento doble ciego con CLOZARIL (N=126) o clorpromazina (N=142). La dosis máxima diaria de CLOZARIL fue de 900 mg; la dosis diaria media fue >600 mg. La dosis máxima diaria de clorpromazina fue de 1800 mg; la dosis diaria media fue >1200 mg.
El criterio principal de valoración fue la respuesta al tratamiento, predefinida como una disminución en la puntuación BPRS de al menos un 20 % y (1) una puntuación CGI-S de
Comportamiento suicida recurrente en esquizofrenia o trastorno esquizoafectivo
La eficacia de CLOZARIL para reducir el riesgo de conducta suicida recurrente se evaluó en el Ensayo Internacional de Prevención del Suicidio (InterSePT™, una marca comercial de Novartis Pharmaceuticals Corporation). Esta fue una comparación prospectiva, aleatorizada, abierta, con control activo, multicéntrica, internacional, de grupos paralelos de CLOZARIL versus olanzapina (*Zyprexa®, una marca registrada de Eli Lilly and Company) en 956 pacientes con esquizofrenia o trastorno esquizoafectivo ( DSM-IV) que se consideró que estaban en riesgo de conducta suicida recurrente. Solo alrededor de una cuarta parte de estos pacientes (27%) se consideraron resistentes al tratamiento estándar con medicamentos antipsicóticos. Para participar en el ensayo, los pacientes deben haber cumplido uno de los siguientes criterios:
- Habían intentado suicidarse en los tres años anteriores a su evaluación inicial.
- Habían sido hospitalizados para prevenir un intento de suicidio dentro de los tres años anteriores a su evaluación inicial.
- Demostraron ideación suicida de moderada a severa con un componente depresivo dentro de una semana antes de su evaluación inicial.
- Demostraron ideas suicidas de moderadas a graves acompañadas de alucinaciones de órdenes para autolesionarse una semana antes de su evaluación inicial.
Los regímenes de dosificación para cada grupo de tratamiento fueron determinados por investigadores individuales y fueron individualizados por paciente. La posología fue flexible, con un rango de dosis de 200 a 900 mg/día para CLOZARIL y de 5 a 20 mg/día para olanzapina. Para los 956 pacientes que recibieron CLOZARIL u olanzapina en este estudio, hubo un uso extenso de psicotrópicos concomitantes: 84 % con antipsicóticos, 65 % con ansiolíticos, 53 % con antidepresivos y 28 % con estabilizadores del estado de ánimo. Hubo un uso significativamente mayor de medicamentos psicotrópicos concomitantes entre los pacientes del grupo de olanzapina.
La medida de eficacia primaria fue el tiempo hasta (1) un intento de suicidio significativo, incluido un suicidio consumado; (2) hospitalización debido al riesgo inminente de suicidio, incluido un mayor nivel de vigilancia de las tendencias suicidas para los pacientes que ya están hospitalizados; o (3) empeoramiento de la severidad de las tendencias suicidas como se demuestra por "mucho empeoramiento" o "mucho empeoramiento" desde el inicio en la Impresión clínica global de la gravedad de las tendencias suicidas según lo evaluado por la escala Blinded Psychiatrist  (CGI-SS-BP). La Junta de Supervisión del Suicidio (SMB, por sus siglas en inglés), un grupo de expertos que desconocían los datos de los pacientes, determinó si un evento informado cumplía o no con los criterios 1 o 2 anteriores.
Un total de 980 pacientes fueron asignados aleatoriamente al estudio y 956 recibieron la medicación del estudio. Sesenta y dos por ciento de los pacientes fueron diagnosticados con esquizofrenia, y el resto (38%) fueron diagnosticados con trastorno esquizoafectivo. Solo alrededor de una cuarta parte de la población total de pacientes (27 %) se identificó como "resistente al tratamiento" al inicio del estudio. Hubo más hombres que mujeres en el estudio (61% de todos los pacientes eran hombres). La edad media de los pacientes que ingresaron al estudio fue de 37 años (rango 18-69). La mayoría de los pacientes eran caucásicos (71 %), el 15 % eran negros, el 1 % eran asiáticos y el 13 % se clasificaron como de “otras” razas.
Los pacientes tratados con CLOZARIL 100 mg tuvieron un retraso más largo estadísticamente significativo en el tiempo hasta la conducta suicida recurrente en comparación con la olanzapina. Este resultado debe interpretarse solo como evidencia de la eficacia de CLOZARIL para retrasar el tiempo hasta la conducta suicida recurrente y no como una demostración de la eficacia superior de CLOZARIL 50 mg sobre la olanzapina.
La probabilidad de experimentar (1) un intento de suicidio significativo, incluido un suicidio consumado, o (2) hospitalización debido a un riesgo de suicidio inminente, incluido un mayor nivel de vigilancia de las tendencias suicidas para los pacientes que ya estaban hospitalizados, fue menor para los pacientes con CLOZARIL que para los pacientes con olanzapina al principio. Semana 104: CLOZARIL 24% versus olanzapina 32%; IC del 95% de la diferencia: 2%, 14% (Figura 1).
Figura 1: Probabilidad acumulada de un intento de suicidio significativo u hospitalización para prevenir el suicidio en pacientes con esquizofrenia o trastorno esquizoafectivo con alto riesgo de suicidio
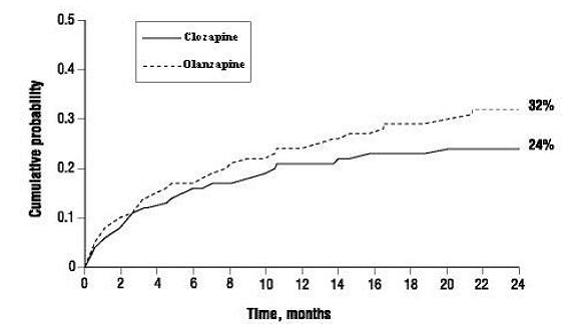
INFORMACIÓN DEL PACIENTE
Discuta los siguientes temas con los pacientes y los cuidadores:
- Neutropenia severa:
- Instruya a los pacientes (y cuidadores) que comienzan el tratamiento con CLOZARIL sobre el riesgo de desarrollar neutropenia e infección graves.
- Indique a los pacientes que informen de inmediato a su médico cualquier síntoma o signo de infección (p. ej., enfermedad similar a la gripe, fiebre, letargo, debilidad o malestar general, ulceración de la membrana mucosa, infección cutánea, faríngea, vaginal, urinaria o pulmonar, o debilidad extrema o letargo) que ocurren en cualquier momento durante la terapia con CLOZARIL 100 mg, para ayudar en la evaluación de la neutropenia y para instituir un manejo rápido y apropiado. [ver ADVERTENCIAS Y PRECAUCIONES ].
- Informe a los pacientes y cuidadores que CLOZARIL 25 mg está disponible solo a través de un programa restringido llamado Programa REMS de clozapina diseñado para garantizar el monitoreo de sangre requerido, a fin de reducir el riesgo de desarrollar neutropenia severa. Aconseje a los pacientes y cuidadores sobre la importancia de hacerse análisis de sangre de la siguiente manera:
- Se requieren análisis de sangre semanales durante los primeros 6 meses.
- Se requiere un ANC cada 2 semanas durante los próximos 6 meses si se mantiene un ANC aceptable durante los primeros 6 meses de terapia continua,
- partir de entonces, se requiere un ANC una vez cada 4 semanas si se mantiene un ANC aceptable durante los segundos 6 meses de terapia continua.
- CLOZARIL 50mg está disponible solo en farmacias certificadas que participan en el programa. Proporcione a los pacientes (y cuidadores) la información del sitio web y el número de teléfono sobre cómo obtener el producto (www.clozapinerems.com o 1-844-267-8678) [ver ADVERTENCIAS Y PRECAUCIONES ].
- Hipotensión ortostática, bradicardia y síncope: informe a los pacientes y cuidadores sobre el riesgo de hipotensión ortostática y síncope, especialmente durante el período de titulación inicial de la dosis. Indíqueles que sigan estrictamente las instrucciones del médico para la dosificación y la administración. Aconseje a los pacientes que consulten a su médico de inmediato si se sienten mareados, pierden el conocimiento o tienen signos o síntomas que sugieran bradicardia o arritmia [ver DOSIFICACIÓN Y ADMINISTRACIÓN , ADVERTENCIAS Y PRECAUCIONES ].
- Convulsiones: Informe a los pacientes y cuidadores sobre el riesgo significativo de convulsiones durante el tratamiento con CLOZARIL 100 mg. Adviértales sobre la conducción y cualquier otra actividad potencialmente peligrosa mientras toman CLOZARIL [ver ADVERTENCIAS Y PRECAUCIONES ].
- Hipomotilidad gastrointestinal con complicaciones graves: educar a los pacientes y cuidadores sobre los riesgos, la prevención y el tratamiento del estreñimiento inducido por clozapina, incluidos los medicamentos que se deben evitar cuando sea posible (p. ej., medicamentos con actividad anticolinérgica). Fomente la hidratación, la actividad física y el consumo de fibra apropiados, y enfatice que la atención y el tratamiento inmediatos del desarrollo de estreñimiento u otros síntomas gastrointestinales son fundamentales para prevenir complicaciones graves. Aconseje a los pacientes y cuidadores que se comuniquen con su proveedor de atención médica si experimentan síntomas de estreñimiento (p. ej., dificultad para defecar, defecación incompleta, disminución de la frecuencia de las deposiciones) u otros síntomas asociados con hipomotilidad gastrointestinal (p. ej., náuseas, distensión o dolor abdominal, vómitos) [ver ADVERTENCIAS Y PRECAUCIONES , INTERACCIONES CON LA DROGAS ].
- Prolongación del intervalo QT: Aconseje a los pacientes que consulten a su médico de inmediato si se sienten mareados, pierden el conocimiento o tienen signos o síntomas que sugieren arritmia. Indique a los pacientes que no tomen CLOZARIL con otros medicamentos que causen la prolongación del intervalo QT. Indique a los pacientes que informen a sus médicos que están tomando CLOZARIL 25 mg antes de cualquier medicamento nuevo [ver ADVERTENCIAS Y PRECAUCIONES , INTERACCIONES CON LA DROGAS ].
- Alteraciones Metabólicas (hiperglucemia y diabetes mellitus, dislipidemia, aumento de peso): Educar a pacientes y cuidadores sobre el riesgo de alteraciones metabólicas y la necesidad de un seguimiento específico. Los riesgos incluyen hiperglucemia y diabetes mellitus, dislipidemia, aumento de peso y reacciones cardiovasculares. Educar a los pacientes y cuidadores sobre los síntomas de hiperglucemia (azúcar alta en la sangre) y diabetes mellitus (p. ej., polidipsia, poliuria, polifagia y debilidad). Supervise a todos los pacientes para detectar estos síntomas. Los pacientes a los que se les diagnostica diabetes o tienen factores de riesgo de diabetes (obesidad, antecedentes familiares de diabetes) deben controlar su glucosa en sangre en ayunas antes de comenzar el tratamiento y periódicamente durante el tratamiento. Los pacientes que desarrollan síntomas de hiperglucemia deben tener evaluaciones de glucosa en ayunas. Se recomienda el control clínico del peso [ver ADVERTENCIAS Y PRECAUCIONES ].
- Interferencia con el rendimiento cognitivo y motor: Debido a que CLOZARIL puede tener el potencial de afectar el juicio, el pensamiento o las habilidades motoras, se debe advertir a los pacientes sobre el manejo de maquinaria peligrosa, incluidos los automóviles, hasta que estén razonablemente seguros de que la terapia con CLOZARIL no los afecta de manera adversa [ver ADVERTENCIAS Y PRECAUCIONES ].
- Dosis olvidadas y reinicio del tratamiento: informe a los pacientes y cuidadores que si el paciente olvida tomar CLOZARIL 50 mg durante más de 2 días, no debe reiniciar su medicamento con la misma dosis, pero debe comunicarse con su médico para obtener instrucciones de dosificación [ver DOSIFICACIÓN Y ADMINISTRACIÓN , ADVERTENCIAS Y PRECAUCIONES ].
- Embarazo: Los pacientes y cuidadores deben notificar al médico si la paciente queda embarazada o tiene la intención de quedar embarazada durante la terapia [ver Uso en poblaciones específicas ].
- Enfermería: Aconseje a los pacientes y cuidadores que el paciente no debe amamantar a un bebé si está tomando CLOZARIL [ver Uso en poblaciones específicas ].
- Medicamentos concomitantes: Aconseje a los pacientes que informen a su proveedor de atención médica si están tomando o planean tomar algún medicamento recetado o de venta libre; existe la posibilidad de interacciones farmacológicas significativas [ver DOSIFICACIÓN Y ADMINISTRACIÓN , INTERACCIONES CON LA DROGAS ].
