Estrace 1mg, 2mg Estradiol Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Estrace y cómo se usa?
Estrace es un medicamento recetado que se usa para tratar los síntomas del cáncer de mama metastásico, la osteoporosis, los niveles bajos de estrógeno (hipoestrogenismo), la atrofia vulvar y vaginal en la menopausia. Estrace 1 mg se puede usar solo o con otros medicamentos.
Estrace 1 mg pertenece a una clase de medicamentos llamados Derivados de estrógeno.
No se sabe si Estrace 1mg es seguro y efectivo en niños.
¿Cuáles son los posibles efectos secundarios de Estrace 1 mg?
Estrace puede causar efectos secundarios graves que incluyen:
- dolor o presión en el pecho,
- dolor que se extiende a la mandíbula o al hombro,
- náuseas,
- transpiración,
- entumecimiento o debilidad repentinos (especialmente en un lado del cuerpo),
- dolor de cabeza repentino e intenso,
- dificultad para hablar,
- problemas con su visión o equilibrio,
- pérdida repentina de la visión,
- dolor punzante en el pecho,
- sensación de falta de aliento,
- tosiendo sangre,
- dolor o calor en una o ambas piernas,
- hinchazón o sensibilidad en el estómago,
- coloración amarillenta de la piel o los ojos (ictericia),
- problemas de memoria,
- confusión,
- comportamiento inusual,
- sangrado vaginal inusual,
- dolor pélvico,
- bulto en tu pecho,
- vómitos,
- estreñimiento,
- aumento de la sed o la micción,
- debilidad muscular,
- dolor de huesos, un
- d
- falta de energía
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Estrace incluyen:
- náuseas,
- vómitos,
- Diarrea,
- calambres en el estómago,
- cambios de humor,
- problemas para dormir (insomnio),
- dolor de cabeza,
- dolor de espalda,
- dolor en los senos,
- síntomas de resfriado (nariz tapada, dolor de sinusitis, dolor de garganta),
- aumento de peso,
- adelgazamiento del cabello del cuero cabelludo,
- picazón o secreción vaginal,
- cambios en sus periodos menstruales, y
- sangrado por disrupción
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Estrace. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
LOS ESTRÓGENOS AUMENTAN EL RIESGO DE CÁNCER DE ENDOMETRIO
Es importante una estrecha vigilancia clínica de todas las mujeres que toman estrógenos. Se deben tomar las medidas de diagnóstico adecuadas, incluido el muestreo endometrial cuando esté indicado, para descartar malignidad en todos los casos de sangrado vaginal anormal persistente o recurrente no diagnosticado. No hay evidencia de que el uso de estrógenos “naturales” resulte en un perfil de riesgo endometrial diferente al de los estrógenos “sintéticos” en dosis de estrógeno equivalentes. (Ver ADVERTENCIAS , Neoplasmas malignos , Cáncer endometrial .)
RIESGOS CARDIOVASCULARES Y OTROS
Los estrógenos con o sin progestágenos no deben utilizarse para la prevención de enfermedades cardiovasculares. (Ver ADVERTENCIAS , Desordenes cardiovasculares .)
El estudio Women's Health Initiative (WHI) informó un aumento del riesgo de infarto de miocardio, accidente cerebrovascular, cáncer de mama invasivo, embolia pulmonar y trombosis venosa profunda en mujeres posmenopáusicas (de 50 a 79 años de edad) durante 5 años de tratamiento con estrógenos conjugados (CE 0,625 mg) combinados con acetato de medroxiprogesterona (MPA 2,5 mg) en relación con el placebo. (Ver FARMACOLOGÍA CLÍNICA , Estudios clínicos .)
El Estudio de Memoria de la Iniciativa de Salud de la Mujer (WHIMS), un subestudio de WHI, informó un mayor riesgo de desarrollar demencia probable en mujeres posmenopáusicas de 65 años o más durante 4 años de tratamiento con estrógenos conjugados orales más acetato de medroxiprogesterona en comparación con el placebo . Se desconoce si este hallazgo se aplica a mujeres posmenopáusicas más jóvenes oa mujeres que toman terapia con estrógeno solo. (Ver FARMACOLOGÍA CLÍNICA , Estudios clínicos .)
Otras dosis de estrógenos conjugados orales con acetato de medroxiprogesterona y otras combinaciones y formas de dosificación de estrógenos y progestágenos no se estudiaron en los ensayos clínicos de la WHI y, en ausencia de datos comparables, se debe suponer que estos riesgos son similares. Debido a estos riesgos, los estrógenos con o sin progestágenos se deben recetar en las dosis efectivas más bajas y durante el período más breve que sea compatible con los objetivos del tratamiento y los riesgos para cada mujer.
DESCRIPCIÓN
ESTRACE ® (tabletas de estradiol, USP) para administración oral contiene 0,5, 1 ó 2 mg de estradiol micronizado por tableta. El estradiol (17ß-estradiol) es un sólido cristalino blanco, descrito químicamente como estra-1,3,5,(10)-trieno-3, 17ß-diol. La fórmula estructural es:
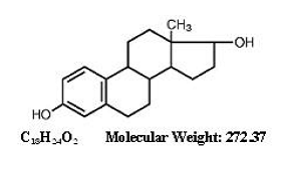
Ingredientes inactivos : Dióxido de silicio coloidal, almidón de maíz, fosfato de calcio dibásico, monohidrato de lactosa, estearato de magnesio y glicolato de almidón de sodio. Además, el 1 mg también contiene FD&C azul no. 1 laca de aluminio y rojo D&C no. 27 lago de aluminio. El 2 mg también contiene FD&C azul no. 1 laca de aluminio y amarillo FD&C no. 5 (tartrazina) laca de aluminio.
INDICACIONES
ESTRACE (tabletas de estradiol, USP) está indicado en el:
DOSIFICACIÓN Y ADMINISTRACIÓN
Cuando se recetan estrógenos a una mujer posmenopáusica con útero, también se debe iniciar un progestágeno para reducir el riesgo de cáncer de endometrio. Una mujer sin útero no necesita progestina. El uso de estrógeno, solo o en combinación con un progestágeno, debe realizarse con la dosis efectiva más baja y durante el período más breve compatible con los objetivos del tratamiento y los riesgos para la mujer individual. Los pacientes deben ser reevaluados periódicamente según sea clínicamente apropiado (p. ej., intervalos de 3 a 6 meses) para determinar si el tratamiento aún es necesario (ver ADVERTENCIAS EN CAJA y ADVERTENCIAS ). Para las mujeres que tienen útero, se deben tomar medidas de diagnóstico adecuadas, tales como muestreo endometrial, cuando esté indicado, para descartar malignidad en casos de sangrado vaginal anormal persistente o recurrente no diagnosticado.
Los pacientes deben comenzar con la dosis más baja para la indicación.
1. Para el tratamiento de síntomas vasomotores de moderados a graves, atrofia vulvar y vaginal asociada con la menopausia, se debe elegir la dosis y el régimen más bajos que controlen los síntomas y se debe suspender la medicación lo antes posible.
Los intentos de discontinuar o disminuir la medicación deben hacerse a intervalos de 3 meses a 6 meses. El rango de dosificación inicial habitual es de 1 a 2 mg diarios de estradiol ajustado según sea necesario para controlar los síntomas de presentación. La dosis efectiva mínima para la terapia de mantenimiento debe determinarse mediante titulación. La administración debe ser cíclica (p. ej., 3 semanas sí y 1 semana no).
2. Para el tratamiento del hipoestrogenismo femenino debido a hipogonadismo, castración o insuficiencia ovárica primaria.
El tratamiento suele iniciarse con una dosis de 1 a 2 mg diarios de estradiol, ajustada según sea necesario para controlar los síntomas de presentación; la dosis efectiva mínima para la terapia de mantenimiento debe determinarse mediante titulación.
3. Para el tratamiento del cáncer de mama, solo como paliación, en mujeres y hombres con enfermedad metastásica adecuadamente seleccionados.
La dosis sugerida es de 10 mg tres veces al día durante un período de al menos tres meses.
4. Para el tratamiento del carcinoma de próstata avanzado dependiente de andrógenos, solo como paliación.
La dosis sugerida es de 1 a 2 mg tres veces al día. La eficacia de la terapia se puede juzgar por las determinaciones de fosfatasa así como por la mejoría sintomática del paciente.
5. Para la prevención de la osteoporosis.
Cuando se prescribe únicamente para la prevención de la osteoporosis posmenopáusica, la terapia debe considerarse solo para mujeres con un riesgo significativo de osteoporosis y para quienes los medicamentos sin estrógeno no se consideran apropiados.
No se ha determinado la dosis eficaz más baja de ESTRACE 2 mg.
CÓMO SUMINISTRADO
ESTRACE® (tabletas de estradiol, USP) están disponibles como:
0,5 miligramos Comprimido ranurado de color blanco a blanquecino, ovalado, de caras planas y con bordes biselados. Repujado con 720 / ½ en el lado ranurado y WC Por otro lado. Disponible en botellas de:
100 tabletas CDN 0430-0720-24
1 mg : Comprimido ranurado, de color púrpura claro, ovalado, de caras planas y con los bordes biselados. Grabado con 721 / 1 en el lado ranurado y WC Por otro lado. Disponible en botellas de:
100 tabletas CDN 0430-0721-24
2 miligramos : Comprimido ranurado, verde, ovalado, de caras planas y con los bordes biselados. Grabado con 722 / 2 en el lado ranurado y WC Por otro lado. Disponible en botellas de:
100 tabletas CDN 0430-0722-24
Almacenar a 20° a 25° C (68° a 77°F) [Ver Temperatura ambiente controlada por USP ].
Dispense en un recipiente hermético resistente a la luz como se define en la USP, con un cierre a prueba de niños (según se requiera).
MANTENGA ESTE Y TODOS LOS MEDICAMENTOS FUERA DEL ALCANCE DE LOS NIÑOS.
Fabricado por: TEVA PHARMACEUTICALS USA Sellersville, PA 18960. Comercializado por: Warner Chilcott (US), LLC, Rockaway, NJ 07866, 1-800-521-8813. Revisado: septiembre de 2013
EFECTOS SECUNDARIOS
Ver ADVERTENCIAS EN CAJA , ADVERTENCIAS y PRECAUCIONES .
Se han informado las siguientes reacciones adversas adicionales con la terapia con estrógenos y/o progestágenos.
Sistema genitourinario
Cambios en el patrón de sangrado vaginal y flujo o sangrado por deprivación anormal; sangrado intermenstrual, manchado, dismenorrea Aumento del tamaño de los leiomiomas uterinos Vaginitis, incluida la candidiasis vaginal Cambios en la cantidad de secreción cervical Cambios en el ectropión cervical Cáncer de ovario; hiperplasia endometrial; cáncer endometrial
Pechos
Sensibilidad, agrandamiento, dolor, secreción del pezón, galactorrea; cambios fibroquísticos en las mamas; cáncer de mama
Cardiovascular
Trombosis venosa profunda y superficial; embolia pulmonar; tromboflebitis; infarto de miocardio; carrera; aumento de la presión arterial
Gastrointestinal
Náuseas, vómitos Calambres abdominales, hinchazón Ictericia colestásica Mayor incidencia de enfermedad de la vesícula biliar Pancreatitis Agrandamiento de hemangiomas hepáticos
Piel
Cloasma o melasma que puede persistir cuando se suspende el fármaco Eritema multiforme Eritema nodoso Erupción hemorrágica Pérdida del cabello del cuero cabelludo Hirsutismo Prurito, erupción cutánea
Ojos
Trombosis vascular retinal Intensificación de la curvatura corneal Intolerancia a las lentes de contacto
Sistema nervioso central
Dolor de cabeza, migraña, mareos Depresión mental Corea Nerviosismo, alteraciones del estado de ánimo, irritabilidad Exacerbación de la epilepsia Demencia
Misceláneas
Aumento o disminución de peso Reducción de la tolerancia a los hidratos de carbono Empeoramiento de la porfiria Edema Artralgias; calambres en las piernas Cambios en la libido Urticaria Angioedema Reacciones anafilactoides/anafilácticas Hipocalcemia Exacerbación del asma Aumento de triglicéridos
INTERACCIONES CON LA DROGAS
Interacciones entre medicamentos y pruebas de laboratorio
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
Ver ADVERTENCIAS EN CAJA .
Desordenes cardiovasculares
La terapia con estrógeno y estrógeno/progestina se ha asociado con un mayor riesgo de eventos cardiovasculares como infarto de miocardio y accidente cerebrovascular, así como trombosis venosa y embolia pulmonar (tromboembolia venosa o TEV). Si cualquiera de estos ocurre o se sospecha, los estrógenos deben suspenderse inmediatamente.
Los factores de riesgo de enfermedad vascular arterial (p. ej., hipertensión, diabetes mellitus, tabaquismo, hipercolesterolemia y obesidad) y/o tromboembolismo venoso (p. ej., antecedentes personales o familiares de TEV, obesidad y lupus eritematoso sistémico) deben manejarse adecuadamente.
Enfermedad coronaria y accidente cerebrovascular
En el estudio Women's Health Initiative (WHI), se observó un aumento en el número de infartos de miocardio y accidentes cerebrovasculares en mujeres que recibieron CE en comparación con el placebo. Estas observaciones son preliminares y el estudio continúa. (Ver FARMACOLOGÍA CLÍNICA , Estudios clínicos .)
En el subestudio CE/MPA de WHI, se observó un mayor riesgo de eventos de enfermedad coronaria (CHD) (definidos como infarto de miocardio no fatal y muerte por CHD) en mujeres que recibieron CE/MPA en comparación con mujeres que recibieron placebo (37 frente a 30 por cada 10 000 personas). años). El aumento del riesgo se observó en el primer año y persistió.
En el mismo subestudio de WHI, se observó un mayor riesgo de accidente cerebrovascular en mujeres que recibieron CE/MPA en comparación con mujeres que recibieron placebo (29 frente a 21 por 10 000 años-mujer). El aumento del riesgo se observó después del primer año y persistió.
En mujeres posmenopáusicas con cardiopatía documentada (n = 2763, edad promedio 66,7 años), un ensayo clínico controlado de prevención secundaria de enfermedades cardiovasculares (Heart and Estrogen/Progestin Replacement Study; HERS) de tratamiento con CE/MPA (0,625 mg/2,5 mg por día) no demostró ningún beneficio cardiovascular. Durante un seguimiento promedio de 4,1 años, el tratamiento con CE/MPA no redujo la tasa general de eventos de cardiopatía coronaria en mujeres posmenopáusicas con enfermedad coronaria establecida. Hubo más eventos de cardiopatía coronaria en el grupo tratado con CE/MPA que en el grupo de placebo en el año 1, pero no durante los años siguientes. Dos mil trescientas veintiuna mujeres del ensayo HERS original aceptaron participar en una extensión abierta de HERS, HERS II. El seguimiento promedio en HERS II fue de 2,7 años adicionales, para un total de 6,8 años en general. Las tasas de eventos de cardiopatía coronaria fueron comparables entre las mujeres del grupo CE/MPA y el grupo placebo en HERS, HERS II y en general.
Grandes dosis de estrógeno (5 mg de estrógenos conjugados por día), comparables a las que se usan para tratar el cáncer de próstata y de mama, han demostrado en un gran ensayo clínico prospectivo en hombres que aumentan los riesgos de infarto de miocardio no mortal, embolia pulmonar y tromboflebitis.
Tromboembolismo venoso (TEV).
En el estudio Women's Health Initiative (WHI), se observó un aumento de TEV en mujeres que recibieron CE en comparación con el placebo. Estas observaciones son preliminares y el estudio continúa. (Ver FARMACOLOGÍA CLÍNICA , Estudios clínicos .)
En el subestudio CE/MPA de WHI, se observó una tasa dos veces mayor de TEV, incluida la trombosis venosa profunda y la embolia pulmonar, en mujeres que recibieron CE/MPA en comparación con las mujeres que recibieron placebo. La tasa de TEV fue de 34 por 10 000 mujeres por año en el grupo CE/MPA en comparación con 16 por 10 000 mujeres por año en el grupo de placebo. El aumento del riesgo de TEV se observó durante el primer año y persistió.
Si es factible, los estrógenos deben suspenderse al menos 4 a 6 semanas antes de una cirugía del tipo asociado con un mayor riesgo de tromboembolismo, o durante períodos de inmovilización prolongada.
Neoplasmas malignos
Cáncer endometrial
El uso de estrógenos sin oposición en mujeres con útero intacto se ha asociado con un mayor riesgo de cáncer de endometrio. El riesgo informado de cáncer de endometrio entre las usuarias de estrógenos sin oposición es aproximadamente de 2 a 12 veces mayor que entre las no usuarias, y parece depender de la duración del tratamiento y de la dosis de estrógenos. La mayoría de los estudios no muestran un aumento significativo del riesgo asociado con el uso de estrógenos durante menos de un año. El mayor riesgo parece estar asociado con el uso prolongado, con riesgos aumentados de 15 a 24 veces durante cinco a diez años o más, y este riesgo persiste durante 8 a más de 15 años después de suspender la terapia con estrógenos.
Es importante la vigilancia clínica de todas las mujeres que toman combinaciones de estrógeno/progestágeno (ver PRECAUCIONES ). Se deben tomar las medidas de diagnóstico adecuadas, incluido el muestreo endometrial cuando esté indicado, para descartar malignidad en todos los casos de sangrado vaginal anormal persistente o recurrente no diagnosticado. No hay evidencia de que el uso de estrógenos naturales resulte en un perfil de riesgo endometrial diferente al de los estrógenos sintéticos de dosis de estrógeno equivalente. Se ha demostrado que agregar una progestina a la terapia de estrógeno reduce el riesgo de hiperplasia endometrial, que puede ser un precursor del cáncer de endometrio.
Cáncer de mama
Se ha informado que el uso de estrógenos y progestágenos por parte de mujeres posmenopáusicas aumenta el riesgo de cáncer de mama. El ensayo clínico aleatorizado más importante que proporciona información sobre este tema es el subestudio de la Iniciativa de Salud de la Mujer (WHI) de CE/MPA (ver FARMACOLOGÍA CLÍNICA , Estudios clínicos ). Los resultados de los estudios observacionales son generalmente consistentes con los del ensayo clínico WHI y no informan variaciones significativas en el riesgo de cáncer de mama entre diferentes estrógenos o progestágenos, dosis o vías de administración.
El subestudio CE/MPA de WHI informó un mayor riesgo de cáncer de mama en mujeres que tomaron CE/MPA durante un seguimiento medio de 5,6 años. Los estudios observacionales también han informado un mayor riesgo para la terapia de combinación de estrógeno/progestágeno y un menor riesgo aumentado para la terapia de estrógeno solo, después de varios años de uso. En el ensayo WHI y en los estudios observacionales, el exceso de riesgo aumentó con la duración del uso. A partir de estudios observacionales, el riesgo pareció volver a la línea de base en unos cinco años después de suspender el tratamiento. Además, los estudios observacionales sugieren que el riesgo de cáncer de mama fue mayor y se hizo evidente antes con la terapia de combinación de estrógeno/progestágeno en comparación con la terapia de estrógeno solo.
En el subestudio CE/MPA, el 26 % de las mujeres informó haber usado previamente estrógeno solo y/o terapia hormonal combinada de estrógeno/progestágeno. Después de un seguimiento medio de 5,6 años durante el ensayo clínico, el riesgo relativo general de cáncer de mama invasivo fue de 1,24 (intervalo de confianza del 95 %: 1,01-1,54), y el riesgo absoluto general fue de 41 frente a 33 casos por 10 000 mujeres-año, para CE/AMP en comparación con placebo. Entre las mujeres que informaron el uso previo de terapia hormonal, el riesgo relativo de cáncer de mama invasivo fue de 1,86 y el riesgo absoluto fue de 46 frente a 25 casos por 10 000 años-mujer para CE/AMP en comparación con placebo. Entre las mujeres que informaron que no habían usado terapia hormonal anteriormente, el riesgo relativo de cáncer de mama invasivo fue de 1,09 y el riesgo absoluto fue de 40 frente a 36 casos por 10 000 años-mujer para CE/AMP en comparación con placebo. En el mismo subestudio, los cánceres de mama invasivos fueron más grandes y se diagnosticaron en una etapa más avanzada en el grupo CE/MPA en comparación con el grupo placebo. La enfermedad metastásica fue rara sin diferencia aparente entre los dos grupos. Otros factores pronósticos como el subtipo histológico, el grado y el estado del receptor hormonal no difirieron entre los grupos.
Se ha informado que el uso de estrógeno más progestina da como resultado un aumento de mamografías anormales que requieren una evaluación adicional. Todas las mujeres deben someterse a exámenes de mama anuales por parte de un proveedor de atención médica y realizarse autoexámenes de mama mensuales. Además, los exámenes de mamografía deben programarse según la edad de la paciente, los factores de riesgo y los resultados de mamografías anteriores.
Demencia
En el Estudio de Memoria de la Iniciativa de Salud de la Mujer (WHIMS), se estudiaron 4532 mujeres posmenopáusicas generalmente sanas de 65 años o más, de las cuales el 35 % tenía entre 70 y 74 años y el 18 % tenía 75 años o más. Después de un seguimiento promedio de 4 años, 40 mujeres tratadas con CE/MPA (1,8 %, n = 2229) y 21 mujeres en el grupo de placebo (0,9 %, n = 2303) recibieron diagnósticos de probable demencia. El riesgo relativo de CE/MPA versus placebo fue de 2,05 (intervalo de confianza del 95 %: 1,21 a 3,48), y fue similar para las mujeres con y sin antecedentes de uso de hormonas menopáusicas antes de WHIMS. El riesgo absoluto de demencia probable para EC/MPA versus placebo fue de 45 versus 22 casos por 10 000 mujeres-año, y el exceso de riesgo absoluto para EC/MPA fue de 23 casos por 10 000 mujeres-año. Se desconoce si estos hallazgos se aplican a mujeres posmenopáusicas más jóvenes. (Ver FARMACOLOGÍA CLÍNICA , Estudios clínicos y PRECAUCIONES , Uso geriátrico .)
Se desconoce si estos hallazgos se aplican a la terapia con estrógenos solos.
Enfermedad de la vesícula
Se ha informado un aumento de 2 a 4 veces en el riesgo de enfermedad de la vesícula biliar que requiere cirugía en mujeres posmenopáusicas que reciben estrógenos.
hipercalcemia
La administración de estrógenos puede provocar hipercalcemia grave en pacientes con cáncer de mama y metástasis óseas. Si se produce hipercalcemia, se debe suspender el uso del medicamento y se deben tomar las medidas adecuadas para reducir el nivel de calcio sérico.
Anomalías Visuales
Se ha informado trombosis vascular retinal en pacientes que reciben estrógenos. Suspenda la medicación hasta que se realice un examen si hay una pérdida parcial o completa repentina de la visión, o un inicio repentino de proptosis, diplopía o migraña. Si el examen revela papiledema o lesiones vasculares en la retina, los estrógenos deben suspenderse permanentemente.
PRECAUCIONES
General
Adición de una progestina cuando una mujer no ha tenido una histerectomía
Los estudios de la adición de un progestágeno durante 10 o más días de un ciclo de administración de estrógenos, o diariamente con estrógenos en un régimen continuo, han informado una menor incidencia de hiperplasia endometrial que la inducida por el tratamiento con estrógenos solos. La hiperplasia endometrial puede ser un precursor del cáncer de endometrio.
Sin embargo, existen posibles riesgos que pueden estar asociados con el uso de progestágenos con estrógenos en comparación con los regímenes de estrógenos solos. Estos incluyen un posible aumento del riesgo de cáncer de mama.
Presión sanguínea elevada
En un pequeño número de informes de casos, los aumentos sustanciales de la presión arterial se han atribuido a reacciones idiosincrásicas a los estrógenos. En un ensayo clínico grande, aleatorizado y controlado con placebo, no se observó un efecto generalizado de los estrógenos sobre la presión arterial. La presión arterial debe controlarse a intervalos regulares con el uso de estrógenos.
Hipertrigliceridemia
En pacientes con hipertrigliceridemia preexistente, la terapia con estrógenos puede estar asociada con elevaciones de los triglicéridos plasmáticos que conducen a pancreatitis y otras complicaciones.
Deterioro de la función hepática y antecedentes de ictericia colestásica
Los estrógenos pueden metabolizarse mal en pacientes con insuficiencia hepática. Para pacientes con antecedentes de ictericia colestática asociada con el uso anterior de estrógenos o con el embarazo, se debe tener precaución y, en caso de recurrencia, se debe suspender la medicación.
hipotiroidismo
La administración de estrógeno conduce a un aumento de los niveles de globulina transportadora de tiroides (TBG). Los pacientes con función tiroidea normal pueden compensar el aumento de TBG produciendo más hormona tiroidea, manteniendo así las concentraciones séricas de T4 y T3 libres en el rango normal. Los pacientes dependientes de la terapia de reemplazo de hormonas tiroideas que también reciben estrógenos pueden requerir dosis más altas de su terapia de reemplazo de tiroides. Estos pacientes deben controlar su función tiroidea para mantener sus niveles de hormona tiroidea libre en un rango aceptable.
Retención de líquidos
Debido a que los estrógenos pueden causar cierto grado de retención de líquidos, las pacientes con afecciones que pueden estar influenciadas por este factor, como asma, epilepsia, migraña y disfunción cardíaca o renal, requieren una observación cuidadosa cuando se prescriben estrógenos.
Hipocalcemia
Los estrógenos deben usarse con precaución en personas con hipocalcemia severa.
Cáncer de ovarios
El subestudio CE/MPA de WHI informó que el estrógeno más progestina aumentaba el riesgo de cáncer de ovario. Después de un seguimiento promedio de 5,6 años, el riesgo relativo de cáncer de ovario para CE/AMP versus placebo fue de 1,58 (intervalo de confianza del 95 %: 0,77 a 3,24), pero no fue estadísticamente significativo. El riesgo absoluto de CE/MPA frente a placebo fue de 4,2 frente a 2,7 casos por 10.000 mujeres-año. En algunos estudios epidemiológicos, el uso de estrógenos solos, en particular durante diez años o más, se ha asociado con un mayor riesgo de cáncer de ovario. Otros estudios epidemiológicos no han encontrado estas asociaciones.
Exacerbación de la endometriosis
La endometriosis puede exacerbarse con la administración de estrógenos. Se han informado algunos casos de transformación maligna de implantes endometriales residuales en mujeres tratadas después de una histerectomía con terapia de estrógeno solo. Para pacientes que se sabe que tienen endometriosis residual después de la histerectomía, se debe considerar la adición de progestina.
Exacerbación de otras condiciones
Los estrógenos pueden causar una exacerbación del asma, diabetes mellitus, epilepsia, migraña o porfiria, lupus eritematoso sistémico y hemangiomas hepáticos y deben usarse con precaución en mujeres con estas afecciones.
ESTRACE (tabletas de estradiol, USP), 2 mg, contienen FD&C Yellow No. 5 (tartrazina) que puede causar reacciones de tipo alérgico (incluyendo asma bronquial) en ciertas personas susceptibles. Si bien la incidencia general de la sensibilidad al FD&C Yellow No. 5 (tartrazina) en la población general es baja, se observa con frecuencia en pacientes que también tienen hipersensibilidad a la aspirina.
Información del paciente
Se aconseja a los médicos que discutan la INFORMACIÓN DEL PACIENTE prospecto con los pacientes a quienes prescriben ESTRACE.
Pruebas de laboratorio
La administración de estrógeno debe iniciarse con la dosis más baja aprobada para la indicación y luego guiarse por la respuesta clínica en lugar de por los niveles de hormonas séricas (p. ej., estradiol, FSH). (Ver DOSIFICACIÓN Y ADMINISTRACIÓN sección.)
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
La administración continua a largo plazo de estrógeno, con y sin progestina, en mujeres con y sin útero, ha demostrado un mayor riesgo de cáncer de endometrio, cáncer de mama y cáncer de ovario. (Ver ADVERTENCIAS EN CAJA , ADVERTENCIAS y PRECAUCIONES .)
La administración continua a largo plazo de estrógenos naturales y sintéticos en ciertas especies animales aumenta la frecuencia de carcinomas de mama, útero, cuello uterino, vagina, testículo e hígado.
Embarazo Categoría X
Estrace 2 mg no debe usarse durante el embarazo. (Ver CONTRAINDICACIONES .)
Madres lactantes
Se ha demostrado que la administración de estrógenos a madres lactantes disminuye la cantidad y calidad de la leche. Se han identificado cantidades detectables de estrógenos en la leche de madres que reciben este medicamento. Se debe tener precaución cuando se administra ESTRACE 1 mg a una mujer lactante.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos. Se ha demostrado que las dosis grandes y repetidas de estrógeno durante un período prolongado aceleran el cierre de las epífisis, lo que resulta en una baja estatura en adultos si el tratamiento se inicia antes de que se complete la pubertad fisiológica en niños con un desarrollo normal. En pacientes en los que el crecimiento óseo no es completo, se recomienda el control periódico de la maduración ósea y los efectos sobre los centros epifisarios.
El tratamiento con estrógenos de los niños prepuberales también induce el desarrollo prematuro de las mamas y la cornificación vaginal, y puede inducir potencialmente sangrado vaginal en las niñas. En los niños, el tratamiento con estrógenos puede modificar el proceso puberal normal. Todas las demás reacciones adversas y fisiológicas que se ha demostrado que están asociadas con el tratamiento con estrógenos en adultos podrían ocurrir potencialmente en la población pediátrica, incluidos los trastornos tromboembólicos y la estimulación del crecimiento de ciertos tumores. Por lo tanto, los estrógenos solo deben administrarse a pacientes pediátricos cuando esté claramente indicado y siempre debe utilizarse la dosis efectiva más baja.
Uso geriátrico
No se ha establecido la seguridad y eficacia de los comprimidos de ESTRACE en pacientes geriátricos. En general, la selección de la dosis para un paciente de edad avanzada debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, reflejando la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedad concomitante u otra terapia con medicamentos.
En el Estudio de Memoria de la Iniciativa de Salud de la Mujer, que incluyó a 4532 mujeres de 65 años o más, seguidas durante un promedio de 4 años, el 82 % (n = 3729) tenía entre 65 y 74 años, mientras que el 18 % (n = 803) tenía 75 años o más. La mayoría de las mujeres (80%) no habían usado terapia hormonal previa. Se informó que las mujeres tratadas con estrógenos conjugados más acetato de medroxiprogesterona tenían un riesgo dos veces mayor de desarrollar probable demencia. La enfermedad de Alzheimer fue la clasificación más común de demencia probable tanto en el grupo de estrógenos conjugados más acetato de medroxiprogesterona como en el grupo de placebo. El 90% de los casos de probable demencia se dieron en el 54% de mujeres mayores de 70 años. (Ver ADVERTENCIAS , Demencia .)
Se desconoce si estos hallazgos se aplican a la terapia con estrógenos solos.
SOBREDOSIS
No se han informado efectos nocivos graves después de la ingestión aguda de grandes dosis de anticonceptivos orales que contienen estrógeno por parte de niños pequeños. La sobredosis de estrógeno puede causar náuseas y vómitos, y en las mujeres puede ocurrir sangrado por deprivación.
CONTRAINDICACIONES
Los estrógenos no deben usarse en personas con cualquiera de las siguientes condiciones:
FARMACOLOGÍA CLÍNICA
Los estrógenos endógenos son en gran parte responsables del desarrollo y mantenimiento del sistema reproductivo femenino y las características sexuales secundarias. Aunque los estrógenos circulantes existen en un equilibrio dinámico de interconversiones metabólicas, el estradiol es el principal estrógeno humano intracelular y es sustancialmente más potente que sus metabolitos, la estrona y el estriol a nivel de receptor.
La principal fuente de estrógeno en mujeres adultas con ciclos normales es el folículo ovárico, que secreta de 70 a 500 mcg de estradiol por día, según la fase del ciclo menstrual. Después de la menopausia, la mayor parte del estrógeno endógeno se produce por conversión de androstenediona, secretada por la corteza suprarrenal, en estrona por los tejidos periféricos. Por lo tanto, la estrona y la forma conjugada con sulfato, sulfato de estrona, son los estrógenos circulantes más abundantes en las mujeres posmenopáusicas.
Los estrógenos actúan a través de la unión a receptores nucleares en tejidos sensibles a los estrógenos. Hasta la fecha, se han identificado dos receptores de estrógeno. Estos varían en proporción de un tejido a otro.
Los estrógenos circulantes modulan la secreción pituitaria de las gonadotropinas, la hormona luteinizante (LH) y la hormona estimulante del folículo (FSH), a través de un mecanismo de retroalimentación negativa. Los estrógenos actúan para reducir los niveles elevados de estas hormonas que se observan en las mujeres posmenopáusicas.
Farmacocinética
Distribución
La distribución de los estrógenos exógenos es similar a la de los estrógenos endógenos. Los estrógenos se distribuyen ampliamente en el cuerpo y generalmente se encuentran en concentraciones más altas en los órganos diana de las hormonas sexuales. Los estrógenos circulan en la sangre unidos en gran medida a la globulina transportadora de hormonas sexuales (SHBG) y la albúmina.
Metabolismo
Los estrógenos exógenos se metabolizan de la misma manera que los estrógenos endógenos. Los estrógenos circulantes existen en un equilibrio dinámico de interconversiones metabólicas. Estas transformaciones tienen lugar principalmente en el hígado. El estradiol se convierte reversiblemente en estrona, y ambos pueden convertirse en estriol, que es el principal metabolito urinario. Los estrógenos también experimentan recirculación enterohepática a través de la conjugación de sulfato y glucurónido en el hígado, secreción biliar de conjugados en el intestino e hidrólisis en el intestino seguida de reabsorción. En las mujeres posmenopáusicas, una proporción significativa de los estrógenos circulantes existen como conjugados de sulfato, especialmente el sulfato de estrona, que sirve como reservorio circulante para la formación de estrógenos más activos.
Excreción
El estradiol, la estrona y el estriol se excretan en la orina junto con los conjugados de glucurónido y sulfato.
Poblaciones Especiales
No se realizaron estudios farmacocinéticos en poblaciones especiales, incluidos pacientes con insuficiencia renal o hepática.
Interacciones con la drogas
Estudios in vitro e in vivo han demostrado que los estrógenos son metabolizados parcialmente por el citocromo P450 3A4 (CYP3A4). Por lo tanto, los inductores o inhibidores de CYP3A4 pueden afectar el metabolismo de los estrógenos. Los inductores de CYP3A4 como las preparaciones de hierba de San Juan (Hypericum perforatum), fenobarbital, carbamazepina y rifampicina pueden reducir las concentraciones plasmáticas de estrógenos, lo que posiblemente resulte en una disminución de los efectos terapéuticos y/o cambios en el perfil de sangrado uterino. Los inhibidores de CYP3A4 como la eritromicina, la claritromicina, el ketoconazol, el itraconazol, el ritonavir y el jugo de toronja pueden aumentar las concentraciones plasmáticas de estrógenos y provocar efectos secundarios.
Estudios clínicos
Osteoporosis
La mayoría de los estudios prospectivos de eficacia para esta indicación se han llevado a cabo en mujeres menopáusicas blancas, sin estratificación por otros factores de riesgo, y tienden a mostrar un efecto universalmente saludable sobre los huesos.
Los resultados de un estudio de rango de dosis, doble ciego, aleatorizado, controlado con placebo y de dos años de duración han demostrado que el tratamiento con 0,5 mg de estradiol al día durante 23 días (de un ciclo de 28 días) previene la pérdida de masa ósea vertebral en mujeres posmenopáusicas. Cuando se interrumpe la terapia con estrógenos, la masa ósea disminuye a un ritmo comparable al del período posmenopáusico inmediato. No hay evidencia de que la terapia de reemplazo de estrógeno restaure la masa ósea a los niveles premenopáusicos.
Estudios de la iniciativa de salud de la mujer
La Iniciativa de Salud de la Mujer (WHI, por sus siglas en inglés) inscribió a un total de 27 000 mujeres posmenopáusicas predominantemente sanas para evaluar los riesgos y beneficios del uso de 0,625 mg de estrógenos conjugados (CE) orales por día solos o del uso de 0,625 mg de estrógenos conjugados orales. estrógenos más 2,5 mg de acetato de medroxiprogesterona (MPA) por día en comparación con el placebo en la prevención de ciertas enfermedades crónicas. El criterio principal de valoración fue la incidencia de cardiopatía coronaria (CHD) (infarto de miocardio no fatal y muerte por CHD), con el cáncer de mama invasivo como el principal resultado adverso estudiado. Un "índice global" incluyó la aparición más temprana de CHD, cáncer de mama invasivo, accidente cerebrovascular, embolia pulmonar (EP), cáncer de endometrio, cáncer colorrectal, fractura de cadera o muerte por otra causa. El estudio no evaluó los efectos de CE o CE/MPA sobre los síntomas de la menopausia.
El subestudio CE/MPA se detuvo antes de tiempo porque, de acuerdo con la regla de interrupción predefinida, el aumento del riesgo de cáncer de mama y eventos cardiovasculares superó los beneficios especificados incluidos en el "índice global". Los resultados del subestudio CE/MPA, que incluyó a 16 608 mujeres (edad promedio de 63 años, rango de 50 a 79; 83,9 % blancas, 6,5 % negras, 5,5 % hispanas), después de un seguimiento promedio de 5,2 años, se presentan en la Tabla 1 a continuación:
Para los resultados incluidos en el "índice global", el exceso de riesgo absoluto por 10 000 mujeres-año en el grupo tratado con CE/MPA fue de 7 eventos de cardiopatía coronaria más, 8 accidentes cerebrovasculares más, 8 EP más y 8 cánceres de mama más invasivos, mientras que las reducciones del riesgo absoluto por cada 10 000 años-mujer fueron 6 cánceres colorrectales menos y 5 fracturas de cadera menos. El exceso de riesgo absoluto de eventos incluidos en el “índice global” fue de 19 por 10.000 mujeres-año. No hubo diferencia entre los grupos en términos de mortalidad por todas las causas. (Ver ADVERTENCIAS EN CAJA , ADVERTENCIAS , y PRECAUCIONES .)
Estudio de Memoria de la Iniciativa de Salud de la Mujer
El Women's Health Initiative Memory Study (WHIMS), un subestudio de WHI, inscribió a 4532 mujeres posmenopáusicas predominantemente sanas de 65 años de edad o más (47 % tenía entre 65 y 69 años, 35 % tenía entre 70 y 74 años y 18 % tenía 75 años de edad o más) para evaluar los efectos de CE/MPA (0,625 mg de estrógenos conjugados más 2,5 mg de acetato de medroxiprogesterona) sobre la incidencia de demencia probable (resultado primario) en comparación con placebo.
Después de un seguimiento promedio de 4 años, 40 mujeres en el grupo de estrógeno/progestágeno (45 por 10 000 mujeres-año) y 21 en el grupo de placebo (22 por 10 000 mujeres-año) fueron diagnosticadas con probable demencia. El riesgo relativo de demencia probable en el grupo de terapia hormonal fue de 2,05 (IC del 95 %, 1,21 a 3,48) en comparación con el placebo. Las diferencias entre los grupos se hicieron evidentes en el primer año de tratamiento. Se desconoce si estos hallazgos se aplican a mujeres posmenopáusicas más jóvenes. (Ver ADVERTENCIA EN CAJA y ADVERTENCIAS , Demencia .)
INFORMACIÓN DEL PACIENTE
INTRODUCCIÓN
Lea esta información para el paciente antes de comenzar a tomar ESTRACE 2 mg y lea lo que recibe cada vez que vuelve a surtir ESTRACE. Es posible que haya nueva información. Esta información no reemplaza la conversación con su proveedor de atención médica sobre su condición médica o su tratamiento.
¿CUÁL ES LA INFORMACIÓN MÁS IMPORTANTE QUE DEBO SABER SOBRE ESTRACE (UNA HORMONA ESTRÓGENA)?
- Los estrógenos aumentan las posibilidades de contraer cáncer de útero.
Informe de inmediato cualquier sangrado vaginal inusual mientras esté tomando estrógenos. El sangrado vaginal después de la menopausia puede ser una señal de advertencia de cáncer de útero (matriz). Su proveedor de atención médica debe revisar cualquier sangrado vaginal inusual para averiguar la causa.
- No use estrógenos con o sin progestágenos para prevenir enfermedades cardíacas, ataques cardíacos o accidentes cerebrovasculares.
El uso de estrógenos con o sin progestágenos puede aumentar sus posibilidades de sufrir ataques cardíacos, accidentes cerebrovasculares, cáncer de mama y coágulos sanguíneos. El uso de estrógenos con progestágenos puede aumentar el riesgo de demencia. Usted y su proveedor de atención médica deben hablar regularmente sobre si aún necesita tratamiento con ESTRACE.
¿QUÉ ES ESTRACE?
ESTRACE es un medicamento que contiene hormonas de estrógeno.
¿PARA QUÉ SE UTILIZA ESTRACE?
ESTRACE 1 mg se utiliza para:
- reducir los sofocos moderados a severos
Los estrógenos son hormonas producidas por los ovarios de una mujer. Entre los 45 y los 55 años, los ovarios normalmente dejan de producir estrógenos. Esto conduce a una caída en los niveles de estrógeno en el cuerpo que provoca el "cambio de vida" o menopausia (el final de los períodos menstruales mensuales). A veces, ambos ovarios se extirpan durante una operación antes de que ocurra la menopausia natural. La caída repentina de los niveles de estrógeno provoca la “menopausia quirúrgica”.
Cuando los niveles de estrógeno comienzan a disminuir, algunas mujeres desarrollan síntomas muy incómodos, como una sensación de calor en la cara, el cuello y el pecho, o una fuerte sensación repentina de calor y sudoración ("sofocos" o "sofocos"). En algunas mujeres, los síntomas son leves y no necesitarán estrógenos. En otras mujeres, los síntomas pueden ser más graves. Usted y su proveedor de atención médica deben hablar regularmente sobre si aún necesita tratamiento con ESTRACE.
Los ejercicios con pesas, como caminar o correr, y tomar calcio con suplementos de vitamina D también pueden reducir las posibilidades de padecer osteoporosis posmenopáusica. Es importante hablar sobre el ejercicio y los suplementos con su proveedor de atención médica antes de comenzarlos.
tratar la sequedad, la picazón y el ardor en o alrededor de la vagina, la dificultad o el ardor al orinar asociados con la menopausia
Usted y su proveedor de atención médica deben hablar regularmente sobre si aún necesita tratamiento con ESTRACE para controlar estos problemas. Si usa ESTRACE solo para tratar la sequedad, la picazón y el ardor dentro y alrededor de la vagina, hable con su proveedor de atención médica acerca de si un producto vaginal tópico sería mejor para usted.
- tratar ciertas afecciones en las que los ovarios de una mujer joven no producen suficiente estrógeno de forma natural
- tratar ciertos tipos de sangrado vaginal anormal debido a un desequilibrio hormonal cuando su médico no ha encontrado una causa grave del sangrado
- tratar ciertos tipos de cáncer en situaciones especiales, en hombres y mujeres
- prevenir el adelgazamiento de los huesos
La osteoporosis de la menopausia es un adelgazamiento de los huesos que los hace más débiles y más fáciles de romper. Si usa ESTRACE 1 mg solo para prevenir la osteoporosis de la menopausia, hable con su proveedor de atención médica acerca de si un tratamiento diferente o un medicamento sin estrógenos podría ser mejor para usted. Usted y su proveedor de atención médica deben hablar regularmente sobre si debe continuar con ESTRACE.
¿QUIÉN NO DEBE USAR ESTRACE 2mg?
No empiece a tomar ESTRACE 2 mg si:
- tiene sangrado vaginal inusual que no ha sido evaluado por su médico (consulte las ADVERTENCIAS EN EL RECUADRO)
El sangrado vaginal inusual puede ser una señal de advertencia de cáncer de útero, especialmente si ocurre después de la menopausia. Su médico debe averiguar la causa del sangrado para poder recomendar el tratamiento adecuado. Tomar estrógenos sin visitar a su médico puede causarle daños graves si su sangrado vaginal es causado por cáncer de útero.
- actualmente tiene o ha tenido ciertos tipos de cáncer
Los estrógenos pueden aumentar el riesgo de ciertos tipos de cáncer, incluido el cáncer de mama o de útero. Si tiene o ha tenido cáncer, hable con su proveedor de atención médica sobre si debe tomar ESTRACE.
(Para ciertas pacientes con cáncer de mama o de próstata, los estrógenos pueden ayudar).
- tuvo un derrame cerebral o un ataque al corazón en el último año
- actualmente tiene o ha tenido coágulos de sangre
- tiene o ha tenido problemas hepáticos
- es alérgico a ESTRACE o a cualquiera de sus ingredientes
Consulte el final de este prospecto para obtener una lista de los ingredientes de ESTRACE.
Los comprimidos de 2 mg de ESTRACE contienen tartrazina, que puede provocar reacciones de tipo alérgico (incluido el asma bronquial) en determinadas personas susceptibles. Si bien la incidencia general de la sensibilidad al FD&C Yellow No. 5 (tartrazina) en la población general es baja, se observa con frecuencia en pacientes que también tienen hipersensibilidad a la aspirina.
- cree que puede estar embarazada
Dígale a su proveedor de atención médica:
- si está amamantando
La hormona en ESTRACE 1 mg puede pasar a la leche
- sobre todos sus problemas médicos
Es posible que su proveedor de atención médica deba examinarla más cuidadosamente si tiene ciertas afecciones, como asma (sibilancias), epilepsia (convulsiones), migraña, endometriosis, lupus, problemas cardíacos, hepáticos, tiroideos, renales o si tiene niveles altos de calcio. en tu sangre
- sobre todos los medicamentos que toma
Esto incluye medicamentos recetados y de venta libre, vitaminas y suplementos herbales. Algunos medicamentos pueden afectar el funcionamiento de ESTRACE 1 mg. ESTRACE 1 mg también puede afectar el funcionamiento de sus otros medicamentos.
- si va a someterse a una cirugía o estará en reposo en cama
Es posible que deba dejar de tomar estrógenos.
¿CÓMO DEBO TOMAR ESTRACE?
1. Comience con la dosis más baja y hable con su proveedor de atención médica sobre qué tan bien le está funcionando esa dosis.
2. Los estrógenos deben usarse en la dosis más baja posible para su tratamiento solo durante el tiempo que sea necesario. Usted y su proveedor de atención médica deben hablar regularmente (por ejemplo, cada 3 a 6 meses) sobre la dosis que está tomando y si todavía necesita tratamiento con ESTRACE.
¿CUÁLES SON LOS POSIBLES EFECTOS SECUNDARIOS DE LOS ESTRÓGENOS?
Los efectos secundarios menos comunes pero graves incluyen:
- Cáncer de mama
- Cáncer de útero
- Carrera
- Ataque al corazón
- coágulos de sangre
- Demencia
- Enfermedad de la vesícula
- Cáncer de ovarios
Estas son algunas de las señales de advertencia de los efectos secundarios graves:
- Bultos en los senos
- Sangrado vaginal inusual
- Mareos y desmayos
- Cambios en el habla
- Dolores de cabeza severos
- Dolor de pecho
- Dificultad para respirar
- Dolores en las piernas
- Cambios en la visión
- vómitos
Llame a su proveedor de atención médica de inmediato si tiene alguna de estas señales de advertencia o cualquier otro síntoma inusual que le preocupe.
Los efectos secundarios comunes incluyen:
- Dolor de cabeza
- Dolor en los senos
- Sangrado vaginal irregular o manchado
- Calambres estomacales/abdominales, hinchazón
- Náuseas y vómitos
- Perdida de cabello
Otros efectos secundarios incluyen:
- Alta presión sanguínea
- Problemas hepáticos
- nivel alto de azúcar en la sangre
- Retención de líquidos
- Agrandamiento de tumores benignos ("fibromas") del útero
- Un oscurecimiento irregular de la piel, particularmente en la cara.
- Candidiasis vaginal
Estos no son todos los posibles efectos secundarios de ESTRACE. Para obtener más información, consulte a su proveedor de atención médica o farmacéutico.
¿QUÉ PUEDO HACER PARA REDUCIR MIS POSIBILIDADES DE UN EFECTO SECUNDARIO GRAVE CON ESTRACE?
Si usa estrógenos, puede reducir sus riesgos haciendo lo siguiente:
- Hable con su proveedor de atención médica:
- Esté alerta a las señales de problemas
Si alguna de estas señales de advertencia (o cualquier otro síntoma inusual) ocurre mientras usa estrógenos, llame a su médico de inmediato:
Sangrado anormal de la vagina (posible cáncer de útero)
Dolores en las pantorrillas o el pecho, falta de aliento repentina o tos con sangre (posible coágulo en las piernas o los pulmones)
Dolor de cabeza intenso o vómitos, mareos, desmayos, cambios en la visión o el habla, debilidad o entumecimiento de un brazo o una pierna (posible coágulo en el cerebro o el ojo)
Bultos en los senos (posible cáncer de seno; pídale a su médico o profesional de la salud que le muestre cómo examinar sus senos mensualmente)
Coloración amarillenta de la piel o los ojos (posible problema hepático)
Dolor, hinchazón o sensibilidad en el abdomen (posible problema de la vesícula biliar)
INFORMACIÓN GENERAL SOBRE EL USO SEGURO Y EFICAZ DE ESTRACE
A veces se recetan medicamentos para afecciones que no se mencionan en los folletos de información para el paciente. No tome ESTRACE 2mg para condiciones para las cuales no fue recetado. No le dé ESTRACE 1 mg a otras personas, incluso si tienen los mismos síntomas que usted. Puede que les haga daño.
MANTENGA ESTRACE FUERA DEL ALCANCE DE LOS NIÑOS
Este folleto proporciona un resumen de la información más importante sobre ESTRACE. Si desea obtener más información, hable con su proveedor de atención médica o farmacéutico. Puede solicitar información sobre ESTRACE que está escrita para profesionales de la salud. Puede obtener más información llamando al número gratuito 1-800-521-8813.
¿CUÁLES SON LOS INGREDIENTES DE ESTRACE?
Ingredientes inactivos : Dióxido de silicio coloidal, almidón de maíz, fosfato de calcio dibásico, monohidrato de lactosa, estearato de magnesio y glicolato de almidón de sodio. Además, el 1 mg también contiene FD&C azul no. 1 laca de aluminio y rojo D&C no. 27 lago de aluminio. El 2 mg también contiene FD&C azul no. 1 laca de aluminio y amarillo FD&C no. 5 (tartrazina) laca de aluminio.
