Ponstel 250mg, 500mg Mefenamic Acid Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
PONSTEL® (ácido mefenámico) Cápsulas, USP 250 mg
Riesgo cardiovascular
- Los AINE pueden causar un mayor riesgo de eventos trombóticos cardiovasculares graves, infarto de miocardio y accidente cerebrovascular, que pueden ser fatales. Este riesgo puede aumentar con la duración del uso. Los pacientes con enfermedad cardiovascular o factores de riesgo de enfermedad cardiovascular pueden tener un mayor riesgo (Ver ADVERTENCIAS ).
- PONSTEL® (ácido mefenámico) está contraindicado para el tratamiento del dolor perioperatorio en el contexto de una cirugía de injerto de derivación de arteria coronaria (CABG, por sus siglas en inglés) (consulte ADVERTENCIAS ).
Riesgo Gastrointestinal
- Los AINE causan un mayor riesgo de eventos adversos gastrointestinales graves, como sangrado, ulceración y perforación del estómago o los intestinos, que pueden ser fatales. Estos eventos pueden ocurrir en cualquier momento durante el uso y sin síntomas de advertencia. Los pacientes de edad avanzada tienen un mayor riesgo de eventos gastrointestinales graves (Ver ADVERTENCIAS ).
DESCRIPCIÓN
Ponstel® (ácido mefenámico) es miembro del grupo fenamato de medicamentos antiinflamatorios no esteroideos (AINE). Cada cápsula de color marfil con bandas azules contiene 250 mg de ácido mefenámico para administración oral. El ácido mefenámico es un polvo microcristalino de color blanco a blanco grisáceo, inodoro, con un punto de fusión de 230°-231°C y una solubilidad en agua de 0,004% a pH 7,1. El nombre químico es ácido N-2,3-xilantranílico. El peso molecular es 241,29. Su fórmula molecular es C15H15NO2 y la fórmula estructural del ácido mefenámico es:
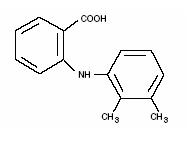
Cada cápsula también contiene lactosa, NF. La cubierta y/o la banda de la cápsula contienen ácido cítrico, USP; D&C amarillo No. 10; FD&C azul No. 1; FD&C rojo No. 3; FD&C amarillo No. 6; gelatina, NF; monooleato de glicerol; dióxido de silicio, NF; benzoato de sodio, NF; laurilsulfato de sodio, NF; dióxido de titanio, USP.
INDICACIONES
Considere detenidamente los posibles beneficios y riesgos de PONSTEL (ácido mefenámico) y otras opciones de tratamiento antes de decidir usar PONSTEL (ácido mefenámico). Utilice la dosis eficaz más baja durante el menor tiempo posible de acuerdo con los objetivos de tratamiento de cada paciente (ver ADVERTENCIAS ).
PONSTEL (ácido mefenámico) está indicado:
- Para el alivio del dolor leve a moderado en pacientes mayores de 14 años, cuando la terapia no excederá una semana (7 días).
- Para el tratamiento de la dismenorrea primaria.
DOSIFICACIÓN Y ADMINISTRACIÓN
Considere detenidamente los posibles beneficios y riesgos de PONSTEL (ácido mefenámico) y otras opciones de tratamiento antes de decidir usar PONSTEL (ácido mefenámico). Utilice la dosis eficaz más baja durante el menor tiempo posible de acuerdo con los objetivos de tratamiento de cada paciente (ver ADVERTENCIAS ).
Después de observar la respuesta a la terapia inicial con PONSTEL (ácido mefenámico), la dosis y la frecuencia deben ajustarse para adaptarse a las necesidades individuales de cada paciente.
Para el alivio del dolor agudo en adultos y adolescentes = 14 años de edad, la dosis recomendada es de 500 mg como dosis inicial seguida de 250 mg cada 6 horas según sea necesario, generalmente sin exceder una semana.4
Para el tratamiento de la dismenorrea primaria, la dosis recomendada es de 500 mg como dosis inicial seguida de 250 mg cada 6 horas, por vía oral, comenzando con la aparición del sangrado y los síntomas asociados. Los estudios clínicos indican que el tratamiento efectivo puede iniciarse con el inicio de la menstruación y no debería ser necesario por más de 2 a 3 días.5
CÓMO SUMINISTRADO
Ponstel (ácido mefenámico) está disponible en cápsulas de color marfil con bandas azules de 250 mg, impresas con "FHPC 400" y "PONSTEL® (ácido mefenámico)".
EFECTOS SECUNDARIOS
En pacientes que toman Ponstel (ácido mefenámico) u otros AINE, las experiencias adversas informadas con mayor frecuencia que ocurren en aproximadamente el 1-10 % de los pacientes son:
Experiencias gastrointestinales que incluyen: dolor abdominal, estreñimiento, diarrea, dispepsia, flatulencia, hemorragia/perforación grave, acidez estomacal, náuseas, úlceras gastrointestinales (gástricas/duodenales), vómitos, función renal anormal, anemia, mareos, edema, enzimas hepáticas elevadas, dolores de cabeza, aumento del tiempo de sangrado, prurito, erupciones, tinnitus
Las experiencias adversas adicionales informadas ocasionalmente y enumeradas aquí por sistema corporal incluyen:
cuerpo como un todo - fiebre, infección, sepsis
Sistema cardiovascular - insuficiencia cardíaca congestiva, hipertensión, taquicardia, síncope
Sistema digestivo - boca seca, esofagitis, úlceras gástricas/pépticas, gastritis, sangrado gastrointestinal, glositis, hematemesis, hepatitis, ictericia
Sistema hemático y linfático - equimosis, eosinofilia, leucopenia, melena, púrpura, rectorragia, estomatitis, trombocitopenia
Metabólico y nutricional - cambios de peso
Sistema nervioso ansiedad, astenia, confusión, depresión, alteraciones del sueño, somnolencia; insomnio, malestar general, nerviosismo, parestesia, somnolencia, temblores, vértigo
Sistema respiratorio - asma, disnea
Piel y apéndices - alopecia, fotosensibilidad, prurito, sudor
Sentidos especiales - visión borrosa
sistema urogenital - cistitis, disuria, hematuria, nefritis intersticial, oliguria/poliuria, proteinuria, insuficiencia renal
Otras reacciones adversas, que ocurren raramente son:
cuerpo como un todo - reacciones anafilactoides, cambios en el apetito, muerte
Sistema cardiovascular - arritmia, hipotensión, infarto de miocardio, palpitaciones, vasculitis
Sistema digestivo - eructos, insuficiencia hepática, pancreatitis
Sistema hemático y linfático - agranulocitosis, anemia hemolítica, anemia aplásica, linfadenopatía, pancitopenia
Metabólico y nutricional - hiperglucemia
Sistema nervioso - convulsiones, coma, alucinaciones, meningitis.
Respiratorio depresión respiratoria, neumonía
Piel y apéndices - angioedema, necrosis epidérmica tóxica, eritema multiforme, dermatitis exfoliativa, síndrome de Stevens-Johnson, urticaria
Sentidos especiales - conjuntivitis, deficiencia auditiva
INTERACCIONES CON LA DROGAS
Varios compuestos son inhibidores de CYP2C9. No se han realizado estudios de interacciones farmacológicas del ácido mefenámico y estos compuestos. Se debe considerar la posibilidad de alteración de la seguridad y la eficacia cuando Ponstel (ácido mefenámico) se usa concomitantemente con estos medicamentos.
inhibidores de la ECA
Los informes sugieren que los AINE pueden disminuir el efecto antihipertensivo de los inhibidores de la ECA. Se debe tener en cuenta esta interacción en pacientes que toman AINE concomitantemente con inhibidores de la ECA.
Aspirina
Cuando se administra PONSTEL (ácido mefenámico) con aspirina, se reduce su unión a proteínas, aunque no se altera el aclaramiento de PONSTEL (ácido mefenámico) libre. Se desconoce la importancia clínica de esta interacción; sin embargo, al igual que con otros AINE, generalmente no se recomienda la administración concomitante de ÁCIDO MEFENAMICO y aspirina debido al potencial de aumento de los efectos adversos.
diuréticos
Los estudios clínicos, así como las observaciones posteriores a la comercialización, han demostrado que PONSTEL (ácido mefenámico) puede reducir el efecto natriurético de la furosemida y las tiazidas en algunos pacientes. Esta respuesta se ha atribuido a la inhibición de la síntesis de prostaglandinas renales. Durante la terapia concomitante con AINE, se debe observar de cerca al paciente para detectar signos de insuficiencia renal (ver PRECAUCIONES, Efectos Renales ), así como para asegurar la eficacia diurética.
Litio
Los AINE han producido una elevación de los niveles plasmáticos de litio y una reducción del aclaramiento renal de litio. La concentración mínima media de litio aumentó un 15 % y el aclaramiento renal disminuyó aproximadamente un 20 %. Estos efectos se han atribuido a la inhibición de la síntesis de prostaglandinas renales por parte de los AINE. Por lo tanto, cuando los AINE y el litio se administran al mismo tiempo, los sujetos deben observarse cuidadosamente para detectar signos de toxicidad por litio.
metotrexato
Se ha informado que los AINE inhiben de forma competitiva la acumulación de metotrexato en rodajas de riñón de conejo. Esto puede indicar que podrían aumentar la toxicidad del metotrexato. Se debe tener precaución cuando los AINE se administren concomitantemente con metotrexato.
warfarina
Los efectos de la warfarina y los AINE sobre el sangrado GI son sinérgicos, de modo que los usuarios de ambos fármacos juntos tienen un riesgo de sangrado GI grave mayor que los usuarios de cualquiera de los dos fármacos por separado.
antiácidos
En un estudio de dosis única (n=6), la ingestión de un antiácido que contenía 1,7 gramos de hidróxido de magnesio con 500 mg de ácido mefenámico aumentó la Cmáx y el AUC del ácido mefenámico en un 125 % y un 36 %, respectivamente.1
Interacciones entre medicamentos y pruebas de laboratorio
Ponstel (ácido mefenámico) puede prolongar el tiempo de protrombina.4 Por lo tanto, cuando el fármaco se administra a pacientes que reciben anticoagulantes orales, es necesario controlar con frecuencia el tiempo de protrombina.
Después de la administración de ácido mefenámico, se puede producir una reacción positiva falsa para la bilis urinaria mediante la prueba de tabletas de diazo. Si se sospecha biliuria, se deben realizar otros procedimientos de diagnóstico, como la prueba de la mancha de Harrison.
REFERENCIAS @sesenta y cinco. Glazko AJ: Observaciones experimentales de los ácidos flufenámico, mefenámico y meclofenámico. Parte III. Disposición metabólica, en Fenamates en Medicina. Un Simposio, Londres, 1966. Annals of Physical Medicine, Suplemento, pp 23-36, 1967.ADVERTENCIAS
Efectos cardiovasculares
Eventos trombóticos cardiovasculares
Los ensayos clínicos de varios AINE selectivos y no selectivos de COX-2 de hasta tres años de duración han demostrado un mayor riesgo de eventos trombóticos cardiovasculares (CV) graves, infarto de miocardio y accidente cerebrovascular, que pueden ser fatales. Todos los NSAID, tanto COX-2 selectivos como no selectivos, pueden tener un riesgo similar. Los pacientes con enfermedad CV conocida o factores de riesgo de enfermedad CV pueden tener un mayor riesgo. Para minimizar el riesgo potencial de un evento CV adverso en pacientes tratados con un AINE, se debe usar la dosis efectiva más baja durante el menor tiempo posible. Los médicos y los pacientes deben permanecer alerta ante el desarrollo de tales eventos, incluso en ausencia de síntomas CV previos. Se debe informar a los pacientes sobre los signos y/o síntomas de eventos CV graves y los pasos a seguir si ocurren.
No existe evidencia consistente de que el uso concurrente de aspirina mitigue el mayor riesgo de eventos trombóticos cardiovasculares graves asociados con el uso de AINE. El uso simultáneo de aspirina y un AINE aumenta el riesgo de eventos gastrointestinales graves (ver ADVERTENCIAS GI ).
Dos grandes ensayos clínicos controlados de un AINE selectivo de la COX-2 para el tratamiento del dolor en los primeros 10 a 14 días posteriores a la cirugía de CABG encontraron una mayor incidencia de infarto de miocardio y accidente cerebrovascular (ver CONTRAINDICACIONES ).
Hipertensión
Los AINE, incluido PONSTEL (ácido mefenámico), pueden provocar la aparición de una nueva hipertensión o el empeoramiento de la hipertensión preexistente, cualquiera de los cuales puede contribuir al aumento de la incidencia de eventos cardiovasculares. Los pacientes que toman tiazidas o diuréticos de asa pueden tener una respuesta deficiente a estas terapias cuando toman AINE. Los AINE, incluido PONSTEL (ácido mefenámico), deben usarse con precaución en pacientes con hipertensión. La presión arterial (PA) debe controlarse de cerca durante el inicio del tratamiento con AINE y durante el curso de la terapia.
Insuficiencia cardíaca congestiva y edema
Se ha observado retención de líquidos y edema en algunos pacientes que toman AINE. PONSTEL (ácido mefenámico) debe usarse con precaución en pacientes con retención de líquidos o insuficiencia cardíaca.
Efectos gastrointestinales: riesgo de ulceración, sangrado y perforación
Los AINE, incluido PONSTEL (ácido mefenámico), pueden causar eventos adversos gastrointestinales (GI) graves, como inflamación, sangrado, ulceración y perforación del estómago, el intestino delgado o el intestino grueso, que pueden ser fatales. Estos eventos adversos graves pueden ocurrir en cualquier momento, con o sin síntomas de advertencia, en pacientes tratados con AINE. Solo uno de cada cinco pacientes, que desarrollan un evento adverso GI superior grave en la terapia con AINE, es sintomático. Las úlceras gastrointestinales superiores, el sangrado macroscópico o la perforación causados por los AINE ocurren en aproximadamente el 1 % de los pacientes tratados durante 3 a 6 meses y en aproximadamente el 2 al 4 % de los pacientes tratados durante un año. Estas tendencias continúan con una mayor duración del uso, lo que aumenta la probabilidad de desarrollar un evento gastrointestinal grave en algún momento durante el curso de la terapia. Sin embargo, incluso la terapia a corto plazo no está exenta de riesgos.
Los AINE deben prescribirse con extrema precaución en personas con antecedentes de enfermedad ulcerosa o hemorragia gastrointestinal. Los pacientes con antecedentes de úlcera péptica y/o sangrado gastrointestinal que usan AINE tienen un riesgo mayor de 10 veces mayor de desarrollar sangrado GI en comparación con los pacientes que no tienen ninguno de estos factores de riesgo. Otros factores que aumentan el riesgo de hemorragia gastrointestinal en pacientes tratados con AINE incluyen el uso concomitante de corticosteroides orales o anticoagulantes, una mayor duración de la terapia con AINE, tabaquismo, consumo de alcohol, edad avanzada y mal estado general de salud. La mayoría de los informes espontáneos de eventos gastrointestinales fatales ocurren en pacientes ancianos o debilitados y, por lo tanto, se debe tener especial cuidado al tratar a esta población.
Para minimizar el riesgo potencial de un evento gastrointestinal adverso en pacientes tratados con un AINE, se debe usar la dosis efectiva más baja durante el menor tiempo posible. Los pacientes y los médicos deben permanecer atentos a los signos y síntomas de ulceración y hemorragia GI durante el tratamiento con AINE e iniciar de inmediato una evaluación y un tratamiento adicionales si se sospecha un evento adverso GI grave. Esto debe incluir la interrupción del AINE hasta que se descarte un evento adverso GI grave. Para pacientes de alto riesgo, se deben considerar terapias alternativas que no involucren AINE.
Efectos renales
La administración a largo plazo de AINE ha resultado en necrosis papilar renal y otras lesiones renales. También se ha observado toxicidad renal en pacientes en los que las prostaglandinas renales tienen un papel compensatorio en el mantenimiento de la perfusión renal. En estos pacientes, la administración de un fármaco antiinflamatorio no esteroideo puede causar una reducción dependiente de la dosis en la formación de prostaglandinas y, secundariamente, en el flujo sanguíneo renal, lo que puede precipitar una descompensación renal manifiesta. Los pacientes con mayor riesgo de esta reacción son aquellos con insuficiencia renal, insuficiencia cardíaca, disfunción hepática, aquellos que toman diuréticos e inhibidores de la ECA y los ancianos. La interrupción del tratamiento con AINE suele ir seguida de la recuperación al estado previo al tratamiento.
Enfermedad Renal Avanzada
No hay información disponible para estudios controlados sobre el uso de PONSTEL (ácido mefenámico) en pacientes con enfermedad renal avanzada. Por lo tanto, no se recomienda el tratamiento con PONSTEL (ácido mefenámico) en estos pacientes con enfermedad renal avanzada (ver CONTRAINDICACIONES ).
Reacciones anafilactoides
Al igual que con otros AINE, pueden ocurrir reacciones anafilactoides en pacientes sin exposición previa conocida a PONSTEL (ácido mefenámico). PONSTEL (ácido mefenámico) no debe administrarse a pacientes con la tríada de la aspirina. Este complejo de síntomas generalmente ocurre en pacientes asmáticos que experimentan rinitis con o sin pólipos nasales, o que presentan broncoespasmo grave y potencialmente fatal después de tomar aspirina u otros AINE (ver CONTRAINDICACIONES y PRECAUCIONES - Asma preexistente ). Se debe buscar ayuda de emergencia en los casos en que ocurra una reacción anafilactoide.
Reacciones de la piel
Los AINE, incluido PONSTEL (ácido mefenámico), pueden causar efectos adversos graves en la piel, como dermatitis exfoliativa, síndrome de Stevens-Johnson (SJS) y necrólisis epidérmica tóxica (NET), que pueden ser fatales. Estos eventos graves pueden ocurrir sin previo aviso. Se debe informar a los pacientes acerca de los signos y síntomas de manifestaciones cutáneas graves y se debe suspender el uso del medicamento ante la primera aparición de erupción cutánea o cualquier otro signo de hipersensibilidad.
El embarazo
Al final del embarazo, al igual que con otros AINE, debe evitarse PONSTEL (ácido mefenámico) porque puede provocar el cierre prematuro del conducto arterioso.
PRECAUCIONES
General
No se puede esperar que PONSTEL (ácido mefenámico) sustituya a los corticosteroides o que trate la insuficiencia de corticosteroides. Una abrupta interrupción de los corticosteroides puede llevar a una exacerbación de la enfermedad. Los pacientes que reciben una terapia prolongada con corticosteroides deben reducir gradualmente su terapia si se toma la decisión de suspender los corticosteroides.
La actividad farmacológica de PONSTEL (ácido mefenámico) para reducir la fiebre y la inflamación puede disminuir la utilidad de estos signos de diagnóstico para detectar complicaciones de condiciones dolorosas presuntamente no infecciosas.
Efectos hepáticos
Pueden ocurrir elevaciones limítrofes de una o más pruebas hepáticas en hasta el 15 % de los pacientes que toman AINE, incluido PONSTEL (ácido mefenámico). Estas anomalías de laboratorio pueden progresar, permanecer sin cambios o ser transitorias con la continuación del tratamiento. Se han informado elevaciones notables de ALT o AST (aproximadamente tres o más veces el límite superior normal) en aproximadamente el 1% de los pacientes en ensayos clínicos con AINE. Además, se han notificado casos raros de reacciones hepáticas graves, que incluyen ictericia y hepatitis fulminante mortal, necrosis hepática e insuficiencia hepática, algunos de ellos con desenlace mortal.
Un paciente con síntomas y/o signos que sugieran disfunción hepática, o en quien se haya producido una prueba hepática anormal, debe ser evaluado para detectar evidencia del desarrollo de una reacción hepática más grave mientras recibe tratamiento con PONSTEL (ácido mefenámico). Si se desarrollan signos y síntomas clínicos consistentes con una enfermedad hepática, o si ocurren manifestaciones sistémicas (p. ej., eosinofilia, erupción cutánea, etc.), se debe interrumpir el uso de PONSTEL (ácido mefenámico).
Efectos hematológicos
veces se observa anemia en pacientes que reciben AINE, incluido PONSTEL (ácido mefenámico). Esto puede deberse a retención de líquidos, pérdida de sangre GI o un efecto descrito de forma incompleta sobre la eritropoyesis. Los pacientes en tratamiento a largo plazo con AINE, incluido PONSTEL (ácido mefenámico), deben controlar su hemoglobina o hematocrito si presentan signos o síntomas de anemia. Los AINE inhiben la agregación plaquetaria y se ha demostrado que prolongan el tiempo de sangrado en algunos pacientes. A diferencia de la aspirina, su efecto sobre la función plaquetaria es cuantitativamente menor, de menor duración y reversible. Los pacientes que reciben PONSTEL (ácido mefenámico) que pueden verse afectados negativamente por alteraciones en la función plaquetaria, como aquellos con trastornos de la coagulación o pacientes que reciben anticoagulantes, deben ser monitoreados cuidadosamente.
Asma preexistente
Los pacientes con asma pueden tener asma sensible a la aspirina. El uso de aspirina en pacientes con asma sensible a la aspirina se ha asociado con broncoespasmo severo que puede ser fatal. Dado que se ha informado de reactividad cruzada, incluido broncoespasmo, entre la aspirina y otros medicamentos antiinflamatorios no esteroideos en pacientes sensibles a la aspirina, PONSTEL (ácido mefenámico) no debe administrarse a pacientes con esta forma de sensibilidad a la aspirina y debe usarse con precaución en pacientes con asma preexistente.
Información para pacientes
Los pacientes deben ser informados de la siguiente información antes de iniciar la terapia con un AINE y periódicamente durante el curso de la terapia en curso. También se debe alentar a los pacientes a leer el AINE Guía de medicamentos que acompaña a cada receta dispensada.
Pruebas de laboratorio
Debido a que las ulceraciones y el sangrado graves del tracto GI pueden ocurrir sin síntomas de advertencia, los médicos deben controlar los signos o síntomas de sangrado GI. Los pacientes en tratamiento a largo plazo con AINE deben tener un CBC y un perfil químico controlados periódicamente. Si se desarrollan signos y síntomas clínicos consistentes con enfermedad hepática o renal, se presentan manifestaciones sistémicas (p. ej., eosinofilia, erupción cutánea, etc.) o si las pruebas hepáticas anormales persisten o empeoran, se debe interrumpir el tratamiento con Ponstel (ácido mefenámico).
El embarazo
Efectos teratogénicos
Embarazo Categoría C
Los estudios reproductivos realizados en ratas y conejos no han demostrado evidencia de anomalías en el desarrollo. Sin embargo, los estudios de reproducción animal no siempre predicen la respuesta humana. No existen estudios adecuados o bien controlados en mujeres embarazadas. Postel debe usarse durante el embarazo solo si el beneficio potencial justifica el riesgo potencial para el feto.
Efectos no teratogénicos
Debido a los efectos conocidos de los fármacos antiinflamatorios no esteroideos sobre el sistema cardiovascular fetal (cierre del conducto arterioso), debe evitarse su uso durante el embarazo (particularmente al final del embarazo).
Trabajo y entrega
En estudios con ratas con AINE, al igual que con otros medicamentos que se sabe que inhiben la síntesis de prostaglandinas, se produjo una mayor incidencia de distocia, retraso en el parto y disminución de la supervivencia de las crías. Se desconocen los efectos de Ponstel (ácido mefenámico) sobre el trabajo de parto y el parto en mujeres embarazadas.
Madres lactantes
Trazas de Ponstel (ácido mefenámico) pueden estar presentes en la leche materna y transmitirse al lactante.7 Debido al potencial de reacciones adversas graves en los lactantes de PONSTEL (ácido mefenámico), se debe tomar la decisión de interrumpir la lactancia o suspender el fármaco, teniendo en cuenta la importancia del fármaco para la madre.
Uso pediátrico
No se ha establecido la seguridad y eficacia en pacientes pediátricos menores de 14 años.
Uso geriátrico
Los estudios clínicos de Ponstel (ácido mefenámico) no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. Al igual que con cualquier AINE, se debe tener precaución al tratar a los ancianos (65 años o más).
Se sabe que este fármaco se excreta sustancialmente por vía renal, y el riesgo de reacciones tóxicas a este fármaco puede ser mayor en pacientes con insuficiencia renal. Debido a que es más probable que los pacientes de edad avanzada tengan una función renal disminuida, se debe tener cuidado al seleccionar la dosis y puede ser útil monitorear la función renal (ver FARMACOLOGÍA CLÍNICA y EVENTOS ADVERSOS).
REFERENCIAS @sesenta y cinco. Buchanan RA, et al. La excreción de la leche materna de ácido mefenámico. Curr Ther Res. 10:592, 1968.SOBREDOSIS
Los síntomas que siguen a las sobredosis agudas de AINE generalmente se limitan a letargo, somnolencia, náuseas, vómitos y dolor epigástrico, que generalmente son reversibles con atención de apoyo. Puede ocurrir hipertensión gastrointestinal, insuficiencia renal aguda, depresión respiratoria y coma, pero son raros. Se han informado reacciones anafilactoides con la ingestión terapéutica de AINE y pueden ocurrir después de una sobredosis.
Los pacientes deben recibir atención sintomática y de apoyo después de una sobredosis de AINE. No hay antídotos específicos. Emesis y/o carbón activado (60 a 100 g en adultos, 1 a 2 g/kg en niños) y/o catártico osmótico pueden estar indicados en pacientes atendidos dentro de las 4 horas de la ingestión con síntomas o después de una sobredosis grande (5 a 10 veces la dosis habitual). La diuresis forzada, la alcalinización de la orina, la hemodiálisis o la hemoperfusión pueden no ser útiles debido a la alta unión a proteínas.
CONTRAINDICACIONES
PONSTEL (ácido mefenámico) está contraindicado en pacientes con hipersensibilidad conocida al ácido mefenámico.
PONSTEL (ácido mefenámico) no debe administrarse a pacientes que hayan experimentado asma, urticaria o reacciones de tipo alérgico después de tomar aspirina u otros AINE. En estos pacientes se han notificado reacciones de tipo anafiláctico graves, rara vez mortales, a los AINE (ver ADVERTENCIAS - Reacciones anafilactoides y PRECAUCIONES - Asma preexistente ).
PONSTEL (ácido mefenámico) está contraindicado para el tratamiento del dolor perioperatorio en el contexto de una cirugía de bypass de arteria coronaria (CABG) (ver ADVERTENCIAS ).
Ponstel (ácido mefenámico) está contraindicado en pacientes con ulceración activa aguda o inflamación crónica del tracto gastrointestinal superior o inferior.
Ponstel (ácido mefenámico) no debe usarse en pacientes con enfermedad renal preexistente.
FARMACOLOGÍA CLÍNICA
Farmacodinámica
Ponstel (ácido mefenámico) es un fármaco antiinflamatorio no esteroideo (AINE) que exhibe actividades antiinflamatorias, analgésicas y antipiréticas en modelos animales. El mecanismo de acción de Ponstel (ácido mefenámico), al igual que el de otros AINE, no se comprende por completo, pero puede estar relacionado con la inhibición de la prostaglandina sintetasa.
Farmacocinética
Absorción
El ácido mefenámico se absorbe rápidamente después de la administración oral. En dos estudios de dosis oral única de 500 mg, el grado medio de absorción fue de 30,5 mcg/h/mL (17 % CV).1,2 No se ha estudiado la biodisponibilidad de la cápsula en relación con una dosis IV o una solución oral.
Después de una dosis oral única de 1 gramo, se han informado niveles plasmáticos máximos medios que oscilan entre 10 y 20 mcg/mL3. Los niveles plasmáticos máximos se alcanzan en 2 a 4 horas y la vida media de eliminación se aproxima a las 2 horas. Después de múltiples dosis, los niveles plasmáticos son proporcionales a la dosis sin evidencia de acumulación del fármaco. En un ensayo de dosis múltiples de sujetos adultos normales (n = 6) que recibieron dosis de 1 gramo de ácido mefenámico cuatro veces al día, se alcanzaron concentraciones de estado estacionario de 20 mcg/mL en el segundo día de administración, en consonancia con el corto medio vida.
No se ha estudiado el efecto de los alimentos sobre la velocidad y el grado de absorción del ácido mefenámico. Se ha demostrado que la ingestión concomitante de antiácidos que contienen hidróxido de magnesio aumenta significativamente la tasa y el grado de absorción del ácido mefenámico (ver PRECAUCIONES: INTERACCIONES MEDICAMENTOSAS ).1
Distribución
Se ha informado que el ácido mefenámico se une a la albúmina en más del 90 %9. No se ha estudiado la relación entre la fracción no unida y la concentración del fármaco. El volumen aparente de distribución (Vzss/F) estimado después de una dosis oral de 500 mg de ácido mefenámico fue de 1,06 l/kg.2
En base a sus propiedades físicas y químicas, se espera que Ponstel (ácido mefenámico) se excrete en la leche materna humana.
Metabolismo
El ácido mefenámico es metabolizado por la enzima CYP2C9 del citocromo P450 a ácido 3-hidroximetilmefenámico (Metabolito I). Puede ocurrir una oxidación adicional a un ácido 3-carboximefenámico (Metabolito II).10 No se ha estudiado la actividad de estos metabolitos. Los metabolitos pueden sufrir glucuronidación y el ácido mefenámico también se glucuronida directamente. Se observó un nivel plasmático máximo de aproximadamente 20 mcg/mL a las 3 horas para el metabolito hidroxi y su glucurónido (n=6) después de una dosis única de 1 gramo. De manera similar, se observó un nivel plasmático máximo de 8 mcg/mL a las 6-8 horas para el metabolito carboxi y su glucurónido.3
Excreción
Aproximadamente el cincuenta y dos por ciento de una dosis de ácido mefenámico se excreta en la orina principalmente como glucurónidos de ácido mefenámico (6 %), ácido 3-hidroximefenámico (25 %) y ácido 3-carboximefenámico (21 %). La vía de eliminación fecal representa hasta el 20% de la dosis, principalmente en forma de ácido 3-carboximefenámico no conjugado.3
La vida media de eliminación del ácido mefenámico es de aproximadamente dos horas. Las vidas medias de los metabolitos I y II no se informaron con precisión, pero parecen ser más prolongadas que las del compuesto original.3 Los metabolitos pueden acumularse en pacientes con insuficiencia renal o hepática. El glucurónido de ácido mefenámico puede unirse irreversiblemente a las proteínas plasmáticas. Debido a que tanto la excreción renal como la hepática son vías importantes de eliminación, puede ser necesario ajustar la dosis en pacientes con disfunción renal o hepática. Ponstel (ácido mefenámico) no debe administrarse a pacientes con enfermedad renal preexistente o en pacientes con insuficiencia renal significativa.
TABLA 1: Estimaciones de parámetros farmacocinéticos para el ácido mefenámico
Poblaciones Especiales
Pediátrico
Ponstel (ácido mefenámico) no se ha investigado adecuadamente en pacientes pediátricos menores de 14 años. Un estudio en 17 bebés prematuros a los que se les administró 2 mg/kg indicó que la vida media era aproximadamente cinco veces mayor que la de los adultos, lo que concuerda con la baja actividad de las enzimas metabólicas en los bebés recién nacidos. La Cmax media en este estudio fue de 4 mcg/mL (rango 2.9-6.1). El tiempo medio hasta la concentración máxima (Tmax) fue de 8 horas (rango 2-18 horas).11
La raza
No se han identificado diferencias farmacocinéticas debidas a la raza.
insuficiencia hepática
No se ha estudiado la farmacocinética del ácido mefenámico en pacientes con disfunción hepática. Dado que el metabolismo hepático es una vía importante de eliminación del ácido mefenámico, los pacientes con enfermedad hepática aguda y crónica pueden necesitar dosis reducidas de Ponstel (ácido mefenámico) en comparación con los pacientes con función hepática normal.
Insuficiencia renal
No se ha investigado la farmacocinética del ácido mefenámico en sujetos con insuficiencia renal. Dado que el ácido mefenámico, sus metabolitos y conjugados se excretan principalmente por los riñones, existe la posibilidad de que se acumulen los metabolitos del ácido mefenámico. Ponstel (ácido mefenámico) no debe administrarse a pacientes con enfermedad renal preexistente o en pacientes con insuficiencia renal significativa.
Estudios clínicos
En ensayos clínicos controlados, doble ciego, se evaluó Ponstel (ácido mefenámico) para el tratamiento de la dismenorrea espasmódica primaria. Los parámetros utilizados para determinar la eficacia incluyeron la evaluación del dolor tanto por parte del paciente como del investigador; la necesidad de medicación analgésica concurrente; y evaluación del cambio en la frecuencia y severidad de los síntomas característicos de la dismenorrea espasmódica. Los pacientes recibieron Ponstel (ácido mefenámico), 500 mg (2 cápsulas) como una dosis inicial de 250 mg cada 6 horas, o placebo al inicio del sangrado o del dolor, lo que comenzara primero. Después de tres ciclos menstruales, las pacientes pasaron al tratamiento alternativo durante tres ciclos adicionales. Ponstel (ácido mefenámico) fue significativamente superior al placebo en todos los parámetros, y ambos tratamientos (fármaco y placebo) fueron igualmente tolerados.
REFERENCIAS @sesenta y cinco. Neuvonen PJ, Kivisto KT: Mejora de la absorción de fármacos por antiácidos. Una interacción farmacológica no reconocida. Clin Pharmacokinet. 27:120-8, agosto de 1994. @sesenta y cinco. Tall AR, Mistilits SP: Estudios sobre Ponstan (ácido mefenámico): I. Pérdida de sangre gastrointestinal; II. Absorción y excreción de una nueva formulación. J Int Med Res (Reino Unido). 1975, 3 (3) p176-82. @sesenta y cinco. Winder CV, Kaump DH, Glazko et al: Observaciones experimentales de los ácidos flufenámico, mefenámico y meclofenámico. AnnPhys Med (inglés), suplemento p7-49.1967. @sesenta y cinco. Champion GD, Graham GG: Farmacocinética de agentes antiinflamatorios no esteroideos. Aust NZ J Med. 8 (Suplemento 1): 94-100, junio de 1978. @sesenta y cinco. McGurk KA, Remmel RP, Hosagrahara VP, Tosh D, Burchell B: Reactividad del ácido mefenámico 1-o-acil glucurónido con proteínas in vitro y ex vivo. Eliminación de metab de drogas. agosto de 1996, 24 (8) p842-9. @sesenta y cinco. Ito K, Niida Y, Sato J et al: Farmacocinética del ácido mefenámico en bebés prematuros con conducto arterioso permeable. Acta Pediatr JPN. 36 (4): 387-91, 1994.INFORMACIÓN DEL PACIENTE
Guía de medicamentos para medicamentos antiinflamatorios no esteroideos (AINE)
(Consulte el final de esta Guía del medicamento para obtener una lista de medicamentos AINE recetados).
¿Cuál es la información más importante que debo saber sobre los medicamentos denominados antiinflamatorios no esteroideos (AINE)?
Los medicamentos AINE pueden aumentar la posibilidad de sufrir un ataque al corazón o un derrame cerebral que puede provocar la muerte. Esta probabilidad aumenta:
- con un uso más prolongado de medicamentos AINE
- en personas que tienen enfermedades del corazón
Los medicamentos AINE nunca deben usarse justo antes o después de una cirugía cardíaca llamada "injerto de derivación de arteria coronaria (CABG)".
Los medicamentos AINE pueden causar úlceras y sangrado en el estómago y los intestinos en cualquier momento durante el tratamiento.
Úlceras y sangrado:
- puede ocurrir sin síntomas de advertencia
- puede causar la muerte
La posibilidad de que una persona tenga una úlcera o sangrado aumenta con:
- tomando medicamentos llamados "corticosteroides" y "anticoagulantes"
- uso más prolongado
- de fumar
- bebiendo alcohol
- mayor edad
- tener mala salud
Los medicamentos AINE solo deben usarse:
- exactamente como se prescribe
- a la dosis más baja posible para su tratamiento
- por el menor tiempo necesario
¿Qué son los medicamentos antiinflamatorios no esteroideos (AINE)?
Los medicamentos AINE se usan para tratar el dolor y el enrojecimiento, la hinchazón y el calor (inflamación) de afecciones médicas como:
- diferentes tipos de artritis
- cólicos menstruales y otros tipos de dolor a corto plazo
¿Quién no debe tomar un medicamento antiinflamatorio no esteroideo (AINE)?
No tome un medicamento AINE:
- si tuvo un ataque de asma, urticaria u otra reacción alérgica con aspirina o cualquier otro medicamento AINE
- para el dolor justo antes o después de la cirugía de derivación cardíaca
Dígale a su proveedor de atención médica:
- sobre todas sus condiciones médicas.
- sobre todos los medicamentos que toma. Los AINE y algunos otros medicamentos pueden interactuar entre sí y causar efectos secundarios graves. Mantenga una lista de sus medicamentos para mostrársela a su proveedor de atención médica y farmacéutico.
- sí estas embarazada. Los medicamentos AINE no deben ser utilizados por mujeres embarazadas al final de su embarazo.
- si está amamantando. Hable con su médico.
¿Cuáles son los posibles efectos secundarios de los medicamentos antiinflamatorios no esteroideos (AINE)?
Obtenga ayuda de emergencia de inmediato si tiene alguno de los siguientes síntomas:
- dificultad para respirar o dificultad para respirar
- Dolor de pecho
- debilidad en una parte o lado de su cuerpo
- dificultad para hablar
- hinchazón de la cara o la garganta
Suspenda su medicamento AINE y llame a su proveedor de atención médica de inmediato si tiene alguno de los siguientes síntomas:
Estos no son todos los efectos secundarios de los medicamentos AINE. Hable con su proveedor de atención médica o farmacéutico para obtener más información sobre los medicamentos AINE.
Otra información sobre los medicamentos antiinflamatorios no esteroideos (AINE)
- La aspirina es un medicamento AINE, pero no aumenta la posibilidad de sufrir un ataque al corazón. La aspirina puede causar sangrado en el cerebro, el estómago y los intestinos. La aspirina también puede causar úlceras en el estómago y los intestinos.
- Algunos de estos medicamentos AINE se venden en dosis más bajas sin receta (de venta libre). Hable con su proveedor de atención médica antes de usar AINE de venta libre durante más de 10 días.
Medicamentos AINE que necesitan receta médica
Esta Guía de medicamentos ha sido aprobada por la Administración de Drogas y Alimentos de los Estados Unidos. Fecha de vigencia: 19/02/2008