Luvox 100mg, 50mg Fluvoxamine Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Luvox (maleato de fluvoxamina) y cómo se usa?
Luvox 100 mg es un medicamento recetado que se usa para tratar los síntomas del trastorno obsesivo-compulsivo. Luvox se puede usar solo o con otros medicamentos.
Luvox 100 mg pertenece a una clase de medicamentos llamados antidepresivos, ISRS.
No se sabe si Luvox 100 mg es seguro y eficaz en niños menores de 8 años.
¿Cuáles son los posibles efectos secundarios de Luvox?
Luvox puede causar efectos secundarios graves que incluyen:
- ansiedad,
- pensamientos acelerados,
- comportamiento de riesgo,
- problemas para dormir (insomnio),
- sentimientos de extrema felicidad o irritabilidad,
- visión borrosa,
- visión de túnel,
- dolor o hinchazón de los ojos,
- viendo halo de luces redondas,
- convulsiones (ataques),
- cambios en el peso o el apetito,
- moretones fáciles o sangrado inusual,
- dolor de cabeza,
- confusión,
- problemas de memoria,
- severa debilidad,
- pérdida de coordinación,
- sintiéndose inestable,
- músculos muy rígidos (rígidos),
- fiebre alta,
- transpiración,
- confusión,
- latidos cardíacos rápidos o irregulares,
- temblores,
- aturdimiento,
- agitación,
- alucinaciones,
- transpiración,
- temblando
- frecuencia cardíaca rápida,
- rigidez muscular,
- retorciéndose,
- náuseas,
- vómitos y
- Diarrea
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Luvox 50 mg incluyen:
- somnolencia,
- mareo,
- sacudida,
- sentirse ansioso,
- estado de ánimo deprimido,
- problemas para dormir (insomnio),
- dolor de barriga,
- gas,
- pérdida de apetito,
- náuseas,
- vómitos,
- Diarrea,
- boca seca,
- bostezando,
- dolor de garganta,
- dolor muscular,
- transpiración,
- sarpullido,
- periodos menstruales abundantes,
- disminución del deseo sexual,
- eyaculación anormal y
- problemas para tener un orgasmo
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Luvox. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
SUICIDALIDAD Y MEDICAMENTOS ANTIDEPRESIVOS
Los antidepresivos aumentaron el riesgo de pensamientos y conductas suicidas (tendencia suicida) en comparación con placebo en niños, adolescentes y adultos jóvenes en estudios a corto plazo de trastorno depresivo mayor (TDM) y otros trastornos psiquiátricos. Cualquiera que esté considerando el uso de tabletas de maleato de amina de 50 mg de Fluvox o cualquier otro antidepresivo en un niño, adolescente o adulto joven debe sopesar este riesgo con la necesidad clínica. Los estudios a corto plazo no mostraron un aumento en el riesgo de tendencias suicidas con antidepresivos en comparación con placebo en adultos mayores de 24 años; hubo una reducción del riesgo con los antidepresivos en comparación con el placebo en adultos de 65 años o más. La depresión y ciertos otros trastornos psiquiátricos están asociados con aumentos en el riesgo de suicidio. Los pacientes de todas las edades que comienzan con la terapia antidepresiva deben ser monitoreados apropiadamente y observados de cerca para detectar empeoramiento clínico, tendencias suicidas o cambios inusuales en el comportamiento. Se debe advertir a las familias y cuidadores de la necesidad de una estrecha observación y comunicación con el prescriptor. Las tabletas de maleato de amina de 50 mg de Fluvox no están aprobadas para su uso en pacientes pediátricos, excepto en pacientes con trastorno obsesivo compulsivo (TOC). [Ver ADVERTENCIAS Y PRECAUCIONES - Empeoramiento clínico y riesgo de suicidio ].
DESCRIPCIÓN
El maleato de fluvoxamina es un inhibidor selectivo de la recaptación de serotonina (5-HT) (ISRS) que pertenece a la serie química, los éteres de 2-aminoetiloxima de las aralquilcetonas.
Se designa químicamente como maleato de 5-metoxi-4'-(trifluorometil)valerofenona-(E)-O-(2-aminoetil)oxima (1:1) y tiene la fórmula empírica C15H21O2N2F3•C4H4O4. Su peso molecular es 434,41. La fórmula estructural es:
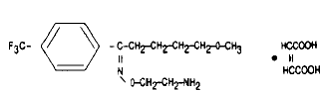
El maleato de amina Fluvox 100 mg es un polvo cristalino, inodoro, de color blanco a blanquecino, escasamente soluble en agua, muy soluble en etanol y cloroformo y prácticamente insoluble en éter dietílico.
Las tabletas de maleato de fluvoxamina están disponibles en concentraciones de 25 mg, 50 mg y 100 mg para administración oral. Además del ingrediente activo, fluvox 100 mg de maleato de amina, cada tableta contiene los siguientes ingredientes inactivos: cera de carnauba, hipromelosa, manitol, polietilenglicol, polisorbato 80, almidón pregelatinizado (papa), dióxido de silicio, estearilfumarato de sodio, almidón (maíz), y dióxido de titanio. Los comprimidos de 50 mg y 100 mg también contienen óxidos de hierro sintéticos.
INDICACIONES
Desorden obsesivo compulsivo
Las tabletas de maleato de fluvoxamina están indicadas para el tratamiento de obsesiones y compulsiones en pacientes con trastorno obsesivo compulsivo (TOC), tal como se define en el DSM-III-R o DSM-IV. Las obsesiones o compulsiones causan una angustia marcada, consumen mucho tiempo o interfieren significativamente con el funcionamiento social o laboral.
El trastorno obsesivo compulsivo se caracteriza por ideas, pensamientos, impulsos o imágenes recurrentes y persistentes (obsesiones) que son egodistónicos y/o comportamientos repetitivos, intencionales e intencionales (compulsiones) que la persona reconoce como excesivos o irrazonables.
La eficacia de Fluvox 100mgamine Maleate Tablets se estableció en cuatro ensayos en pacientes ambulatorios con TOC: dos ensayos de 10 semanas en adultos, un ensayo de 10 semanas en pacientes pediátricos (de 8 a 17 años) y un ensayo de mantenimiento en adultos [ver Estudios clínicos ].
DOSIFICACIÓN Y ADMINISTRACIÓN
Adultos
La dosis inicial recomendada de Fluvox 50 mg comprimidos de maleato de amina en pacientes adultos es de 50 mg, administrados como dosis única diaria a la hora de acostarse. En los ensayos clínicos controlados que establecieron la eficacia de las tabletas de maleato de fluvoxamina en el TOC, los pacientes fueron titulados dentro de un rango de dosis de 100 a 300 mg/día. En consecuencia, la dosis debe aumentarse en incrementos de 50 mg cada 4 a 7 días, según se tolere, hasta lograr el máximo beneficio terapéutico, sin exceder los 300 mg por día. Es aconsejable que una dosis diaria total de más de 100 mg se administre dividida en dos tomas. Si las dosis no son iguales, la dosis mayor debe administrarse a la hora de acostarse.
Población pediátrica (niños y adolescentes)
La dosis inicial recomendada de tabletas de maleato de fluvoxamina en poblaciones pediátricas (edades de 8 a 17 años) es de 25 mg, administrados como una dosis diaria única a la hora de acostarse. En un ensayo clínico controlado que estableció la eficacia de las tabletas de maleato de fluvoxamina en el TOC, los pacientes pediátricos (de 8 a 17 años) fueron titulados dentro de un rango de dosis de 50 a 200 mg/día. Los médicos deben tener en cuenta las diferencias de edad y sexo al administrar la dosis a los pacientes pediátricos. La dosis máxima en niños de hasta 11 años no debe exceder los 200 mg/día. El efecto terapéutico en niñas puede lograrse con dosis más bajas. Puede estar indicado el ajuste de la dosis en adolescentes (hasta la dosis máxima para adultos de 300 mg) para lograr un beneficio terapéutico. La dosis debe aumentarse en incrementos de 25 mg cada 4 a 7 días, según se tolere, hasta lograr el máximo beneficio terapéutico. Es aconsejable que una dosis diaria total de más de 50 mg se administre dividida en dos tomas. Si las dos dosis divididas no son iguales, la dosis mayor debe administrarse a la hora de acostarse.
Pacientes de edad avanzada o con insuficiencia hepática
Se ha observado que los pacientes de edad avanzada y aquellos con insuficiencia hepática tienen una disminución del aclaramiento de maleato de fluvoxamina. En consecuencia, puede ser apropiado modificar la dosis inicial y la posterior titulación de la dosis para estos grupos de pacientes.
Cambio de un paciente a o desde un inhibidor de la monoaminooxidasa (IMAO) destinado a tratar trastornos psiquiátricos
Deben transcurrir al menos 14 días entre la interrupción de un IMAO destinado a tratar trastornos psiquiátricos y el inicio de la terapia con tabletas de maleato de amina Fluvox de 50 mg. Por el contrario, se deben permitir al menos 14 días después de dejar de tomar Fluvox 100 mg comprimidos de maleato de amina antes de comenzar un IMAO destinado a tratar trastornos psiquiátricos [ver CONTRAINDICACIONES ].
Uso de tabletas de maleato de fluvoxamina con otros IMAO como linezolid o azul de metileno
No comience a tomar tabletas de maleato de fluvoxamina en un paciente que está siendo tratado con linezolida o azul de metileno por vía intravenosa porque existe un mayor riesgo de síndrome serotoninérgico. En un paciente que requiere un tratamiento más urgente de una condición psiquiátrica, se deben considerar otras intervenciones, incluida la hospitalización [ver CONTRAINDICACIONES ].
En algunos casos, un paciente que ya esté recibiendo tratamiento con Fluvox 50mgamine Maleate Tablets puede requerir un tratamiento urgente con linezolid o azul de metileno intravenoso. Si no hay disponibles alternativas aceptables al tratamiento con linezolid o azul de metileno intravenoso y se considera que los beneficios potenciales del tratamiento con linezolid o azul de metileno intravenoso superan los riesgos del síndrome serotoninérgico en un paciente en particular, los comprimidos de maleato de fluvoxamina deben suspenderse de inmediato, y linezolid o el tratamiento con azul de metileno intravenoso deben suspenderse de inmediato. Se puede administrar azul de metileno. Se debe monitorear al paciente para detectar síntomas del síndrome serotoninérgico durante dos semanas o hasta 24 horas después de la última dosis de linezolid o azul de metileno intravenoso, lo que ocurra primero. El tratamiento con Fluvox 100mgamine Maleate Tablets se puede reanudar 24 horas después de la última dosis de linezolid o azul de metileno intravenoso [ver ADVERTENCIAS Y PRECAUCIONES ].
No está claro el riesgo de administrar azul de metileno por vías no intravenosas (como comprimidos orales o inyección local) o en dosis intravenosas mucho más bajas que 1 mg/kg con Fluvox 100 mg comprimidos de maleato de amina. No obstante, el médico debe ser consciente de la posibilidad de síntomas emergentes del síndrome serotoninérgico con dicho uso [ver ADVERTENCIAS Y PRECAUCIONES ].
Tratamiento prolongado de mantenimiento/continuación
En general, se acepta que el trastorno obsesivo compulsivo requiere varios meses o más de terapia farmacológica sostenida. El beneficio de mantener a los pacientes con TOC con tabletas de maleato de fluvoxamina después de lograr una respuesta durante una duración promedio de aproximadamente 4 semanas en una fase simple ciego de 10 semanas durante la cual se tituló a los pacientes según el efecto se demostró en un ensayo controlado [ver Ensayos clínicos ].
El médico que decida usar las tabletas de maleato de fluvoxamina durante períodos prolongados debe reevaluar periódicamente la utilidad a largo plazo del fármaco para el paciente individual.
Interrupción del tratamiento con comprimidos de maleato de fluvoxamina
Se han informado síntomas asociados con la suspensión de otros ISRS o IRSN [ver ADVERTENCIAS Y PRECAUCIONES ]. Los pacientes deben ser monitoreados por estos síntomas al suspender el tratamiento. Siempre que sea posible, se recomienda una reducción gradual de la dosis en lugar de una interrupción brusca. Si aparecen síntomas intolerables tras una disminución de la dosis o tras la interrupción del tratamiento, se puede considerar la reanudación de la dosis prescrita anteriormente. Posteriormente, el médico puede continuar disminuyendo la dosis pero a un ritmo más gradual.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
Las tabletas de maleato de fluvoxamina USP están disponibles como:
Comprimidos de 25 mg: sin ranurar, blancos, elípticos, recubiertos con película (grabados “1222” en un lado)
Comprimidos de 50 mg: ranurados, amarillos, elípticos, recubiertos con película (grabados “1225” en un lado y ranurados en el otro)
Comprimidos de 100 mg: ranurados, beige, elípticos, recubiertos con película (grabados “1221” en un lado y ranurados en el otro)
Almacenamiento y manipulación
Fluvox 50mgamine Maleate Tablets USP están disponibles en las siguientes concentraciones, colores, impresiones y presentaciones:
sin ranurar, blanco, elíptico, recubierto con película (grabado “1222” en un lado)
Botellas de 100 ............. CDN 62559-158-01
ranurado, amarillo, elíptico, recubierto con película (grabado “1225” en un lado y ranurado en el otro)
Botellas de 100 ............. CDN 62559-159-01
ranurado, beige, elíptico, recubierto con película (grabado “1221” en un lado y ranurado en el otro)
Botellas de 100 ............. CDN 62559-160-01
Mantener fuera del alcance de los niños.
Las tabletas de maleato de fluvoxamina deben protegerse de la humedad alta y almacenarse a una temperatura de 20° a 25°C (68° a 77°F); excursiones permitidas a 15° a 30°C (59° a 86°F) [ver Temperatura ambiente controlada por USP ].
Dispensar en recipientes herméticos.
Fabricado por: ANI Pharmaceuticals, Inc., Baudette, MN 56623. Revisado: julio de 2021
EFECTOS SECUNDARIOS
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy diversas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica.
Reacciones adversas que conducen a la interrupción del tratamiento
De los 1087 pacientes con TOC y depresión tratados con maleato de fluvoxamina en ensayos clínicos controlados en América del Norte, el 22 % interrumpió el tratamiento debido a una reacción adversa. Las reacciones adversas que dieron lugar a la suspensión en al menos el 2 % de los pacientes tratados con maleato de fluvoxamina en estos ensayos fueron: náuseas (9 %), insomnio (4 %), somnolencia (4 %), dolor de cabeza (3 %) y astenia, vómitos. , nerviosismo, agitación y mareos (2% cada uno).
Incidencia en ensayos controlados
Reacciones adversas comúnmente observadas en ensayos clínicos controlados
Las tabletas de maleato de amina de 100 mg de Fluvox se han estudiado en ensayos controlados a corto plazo de 10 semanas de TOC (N=320) y depresión (N=1350). En general, las tasas de reacciones adversas fueron similares en los dos conjuntos de datos, así como en el estudio de TOC pediátrico. Las reacciones adversas observadas con mayor frecuencia asociadas con el uso de tabletas de maleato de fluvoxamina y que probablemente estén relacionadas con el fármaco (incidencia del 5% o más y al menos el doble que para el placebo) derivadas de la Tabla 2 fueron: náuseas, somnolencia, insomnio, astenia, nerviosismo, dispepsia, eyaculación anormal, sudoración, anorexia, temblor y vómitos. En un conjunto de dos estudios en los que solo participaron pacientes con TOC, se identificaron las siguientes reacciones adicionales utilizando la regla anterior: anorgasmia, disminución de la libido, sequedad de boca, rinitis, alteración del gusto y polaquiuria. En un estudio de pacientes pediátricos con TOC, se identificaron las siguientes reacciones adicionales utilizando la regla anterior: agitación, depresión, dismenorrea, flatulencia, hipercinesia y erupción cutánea.
Reacciones adversas que ocurren con una incidencia del 1 %
La Tabla 2 enumera las reacciones adversas que ocurrieron en adultos con una frecuencia del 1 % o más, y que fueron más frecuentes que en el grupo de placebo, entre pacientes tratados con tabletas de maleato de fluvoxamina en dos ensayos de TOC controlados con placebo a corto plazo (10 semanas) y depresión ensayos (6 semanas) en los que los pacientes recibieron dosis en un rango de generalmente 100 a 300 mg/día. Esta tabla muestra el porcentaje de pacientes en cada grupo que tuvieron al menos una aparición de una reacción en algún momento durante su tratamiento. Las reacciones adversas notificadas se clasificaron utilizando una terminología de diccionario estándar basada en COSTART.
El prescriptor debe ser consciente de que estas cifras no pueden utilizarse para predecir la incidencia de efectos secundarios en el curso de la práctica médica habitual, donde las características del paciente y otros factores pueden diferir de los que prevalecieron en los ensayos clínicos. Del mismo modo, las frecuencias citadas no pueden compararse con cifras obtenidas de otras investigaciones clínicas que involucran diferentes tratamientos, usos e investigadores. Las cifras citadas, sin embargo, proporcionan al médico prescriptor alguna base para estimar la contribución relativa de los factores farmacológicos y no farmacológicos a la tasa de incidencia de efectos secundarios en la población estudiada.
TABLA 2: TASAS DE INCIDENCIA DE REACCIONES ADVERSAS EMERGENTES DEL TRATAMIENTO POR SISTEMA CORPORAL EN POBLACIONES ADULTAS CON TOC Y DEPRESIÓN COMBINADAS1
Reacciones adversas en estudios controlados con placebo para TOC que son marcadamente diferentes (definidas como al menos una diferencia de dos veces) en la tasa de las tasas de reacción agrupadas en estudios controlados con placebo para TOC y depresión
Las reacciones en los estudios de TOC con una disminución del doble en la tasa en comparación con las tasas de reacción en los estudios de TOC y depresión fueron disfagia y ambliopía (principalmente visión borrosa). Además, hubo una disminución aproximada del 25 % en las náuseas.
Las reacciones en los estudios de TOC con un aumento del doble en la tasa en comparación con las tasas de reacción en los estudios de TOC y depresión fueron: astenia, eyaculación anormal (principalmente eyaculación retardada), ansiedad, rinitis, anorgasmia (en hombres), depresión, disminución de la libido, faringitis , agitación, impotencia, mioclonías/contracciones, sed, pérdida de peso, calambres en las piernas, mialgia y retención urinaria. Estas reacciones se enumeran en orden de tasas decrecientes en los ensayos de TOC.
Otras reacciones adversas en población pediátrica con TOC
En pacientes pediátricos (N=57) tratados con tabletas de maleato de amina de 100 mg de Fluvox, el perfil general de reacciones adversas fue generalmente similar al observado en estudios en adultos, como se muestra en la Tabla 2. Sin embargo, las siguientes reacciones adversas, que no aparecen en la Tabla 2, Se informaron en dos o más de los pacientes pediátricos y fueron más frecuentes con las tabletas de maleato de fluvoxamina que con el placebo: aumento de la tos, dismenorrea, equimosis, labilidad emocional, epistaxis, hipercinesia, reacción maníaca, erupción cutánea, sinusitis y disminución de peso.
Disfunción sexual masculina y femenina con ISRS
Aunque los cambios en el deseo sexual, el desempeño sexual y la satisfacción sexual a menudo ocurren como manifestaciones de un trastorno psiquiátrico y con el envejecimiento, también pueden ser consecuencia del tratamiento farmacológico. En particular, alguna evidencia sugiere que los inhibidores selectivos de la recaptación de serotonina (ISRS) pueden causar tales experiencias sexuales adversas.
Sin embargo, es difícil obtener estimaciones confiables de la incidencia y la gravedad de las experiencias adversas relacionadas con el deseo, el rendimiento y la satisfacción sexuales, en parte porque los pacientes y los médicos pueden ser reacios a discutirlas. En consecuencia, es probable que las estimaciones de la incidencia de la experiencia y el rendimiento sexuales adversos citados en la etiqueta del producto subestimen su incidencia real.
La Tabla 3 muestra la incidencia de efectos secundarios sexuales informados por al menos el 2 % de los pacientes que toman Fluvox 100 mg en tabletas de maleato de amina en ensayos controlados con placebo en depresión y TOC.
TABLA 3: PORCENTAJE DE PACIENTES QUE INFORMARON REACCIONES ADVERSAS SEXUALES EN ENSAYOS CONTROLADOS CON PLACEBO EN ADULTOS EN TOC Y DEPRESIÓN
No existen estudios adecuados y bien controlados que examinen la disfunción sexual con el tratamiento con fluvoxamina.
El tratamiento con Fluvox 50mgamine se ha asociado con varios casos de priapismo. En aquellos casos con un resultado conocido, los pacientes se recuperaron sin secuelas y tras la suspensión de fluvox 50mgamine.
Si bien es difícil conocer el riesgo preciso de disfunción sexual asociado con el uso de los ISRS, los médicos deben preguntar de forma rutinaria acerca de tales posibles efectos secundarios.
Cambios en los signos vitales
Las comparaciones de los grupos de maleato de fluvoxamina y placebo en grupos separados de ensayos de TOC y depresión a corto plazo sobre (1) el cambio medio desde el inicio en varias variables de signos vitales y sobre (2) la incidencia de pacientes que cumplen los criterios para cambios potencialmente importantes desde el inicio en varios signos vitales. Las variables de signos no revelaron diferencias importantes entre el maleato de fluvoxamina y el placebo.
Cambios de laboratorio
Comparaciones de grupos de maleato de fluvoxamina y placebo en grupos separados de ensayos de TOC y depresión a corto plazo sobre (1) el cambio medio desde el valor inicial en varias variables de química sérica, hematología y análisis de orina y sobre (2) la incidencia de pacientes que cumplen los criterios para cambios potencialmente importantes desde el inicio en diversas variables químicas séricas, hematológicas y de análisis de orina, no se revelaron diferencias importantes entre fluvox 100 mg de maleato de amina y el placebo.
Cambios en el ECG
Comparaciones de los grupos de fluvox 50 mg de maleato de amina y placebo en grupos separados de ensayos de TOC y depresión a corto plazo sobre (1) el cambio medio desde el inicio en varias variables de ECG y sobre (2) la incidencia de pacientes que cumplen los criterios para cambios potencialmente importantes desde el inicio en varios ECG variables no revelaron diferencias importantes entre el maleato de fluvoxamina y el placebo.
Otras reacciones observadas durante la evaluación previa a la comercialización de las tabletas de maleato de amina Fluvox de 100 mg
Durante los ensayos clínicos previos a la comercialización realizados en América del Norte y Europa, se administraron dosis múltiples de maleato de fluvoxamina para un total combinado de 2737 exposiciones de pacientes que padecían TOC o trastorno depresivo mayor. Los investigadores clínicos registraron las reacciones adversas asociadas con esta exposición utilizando terminología descriptiva de su propia elección. En consecuencia, no es posible proporcionar una estimación significativa de la proporción de personas que experimentan reacciones adversas sin agrupar primero tipos similares de reacciones adversas en un número limitado (es decir, reducido) de categorías de reacción estándar.
En las siguientes tabulaciones, se ha utilizado una terminología de diccionario estándar basada en COSTART para clasificar las reacciones adversas notificadas. Si el término COSTART para una reacción era tan general como para no ser informativo, se reemplazaba por un término más informativo. Las frecuencias presentadas, por lo tanto, representan la proporción de los 2737 pacientes expuestos a múltiples dosis de fluvox 100 mg de maleato de amina que experimentaron una reacción del tipo citado en al menos una ocasión mientras recibían fluvoxamina maleato. Todas las reacciones informadas se incluyen en la lista a continuación, con las siguientes excepciones: 1) se excluyen aquellas reacciones que ya se enumeran en la Tabla 2, que tabula las tasas de incidencia de experiencias adversas comunes en ensayos clínicos de TOC y depresión controlados con placebo; 2) se omiten aquellas reacciones para las que no se consideró probable la causa de un fármaco; 3) reacciones para las cuales el término COSTART era demasiado vago para ser clínicamente significativo y no podía reemplazarse por un término más informativo; y 4) no se incluyen las reacciones que se informaron en un solo paciente y que se consideró que no eran potencialmente graves. Es importante enfatizar que, aunque las reacciones reportadas ocurrieron durante el tratamiento con maleato de fluvoxamina, no se ha establecido una relación causal con el maleato de fluvoxamina.
Las reacciones se clasifican además dentro de categorías de sistemas corporales y se enumeran en orden de frecuencia decreciente utilizando las siguientes definiciones: las reacciones adversas frecuentes se definen como aquellas que ocurren en una o más ocasiones en al menos 1/100 pacientes; las reacciones adversas poco frecuentes son las que ocurren entre 1/100 y 1/1000 pacientes; y las reacciones adversas raras son aquellas que ocurren en menos de 1/1000 pacientes.
Cuerpo como un Todo - Frecuentes: malestar general; Infrecuentes: reacción de fotosensibilidad e intento de suicidio.
Sistema cardiovascular - Frecuente: síncope.
Sistema digestivo - Infrecuentes: hemorragia gastrointestinal y melena; Raros: hematemesis.
Sistemas Hemático y Linfático - Infrecuentes: anemia y equimosis; Raros: púrpura.
Sistemas Metabólicos y Nutricionales - Frecuentes: ganancia y pérdida de peso.
Sistema nervioso - Frecuentes: hipercinesia, reacción maníaca y mioclonía; Infrecuentes: sueños anormales, acatisia, convulsiones, discinesia, distonía, euforia, síndrome extrapiramidal y espasmos; Raros: síndrome de abstinencia.
Sistema respiratorio - Infrecuentes: epistaxis. Raros: hemoptisis y laringismo.
Piel - Infrecuentes: urticaria.
Sistema urogenital* - Infrecuentes: hematuria, menorragia y hemorragia vaginal; Raros: hematospermia.
* Basado en el número de hombres o mujeres, según corresponda.
Informes posteriores a la comercialización
Se han identificado las siguientes reacciones adversas durante el uso posterior a la aprobación de las tabletas de maleato de amina Fluvox de 100 mg. Debido a que estas reacciones son informadas voluntariamente por una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Los informes voluntarios de reacciones adversas en pacientes que toman Fluvox 50 mg comprimidos de maleato de amina que se han recibido desde la introducción en el mercado y cuya relación causal desconocida con el uso de comprimidos de maleato de fluvoxamina incluyen: insuficiencia renal aguda, agranulocitosis, amenorrea, reacción anafiláctica, angioedema, anemia aplásica, erupción ampollosa , púrpura de Henoch-Schoenlein, hepatitis, íleo, pancreatitis, porfiria, síndrome de Stevens-Johnson, necrólisis epidérmica tóxica, vasculitis y taquicardia ventricular (incluyendo torsades de pointes).
INTERACCIONES CON LA DROGAS
Interacciones potenciales con fármacos que inhiben o son metabolizados por las isoenzimas del citocromo P450
Múltiples isoenzimas hepáticas del citocromo P450 están implicadas en la biotransformación oxidativa de un gran número de fármacos y compuestos endógenos estructuralmente diferentes. El conocimiento disponible sobre la relación de la fluvoxamina y el sistema de isoenzimas del citocromo P450 se ha obtenido principalmente de estudios de interacción farmacocinética realizados en voluntarios sanos, pero también se dispone de algunos datos preliminares in vitro. Basado en un hallazgo de interacciones sustanciales de fluvox 50mgamine con algunos de estos medicamentos [ver partes posteriores de esta sección y también ADVERTENCIAS Y PRECAUCIONES ] y datos in vitro limitados para CYP3A4, parece que fluvox 100 mgamina inhibe varias isoenzimas del citocromo P450 que se sabe que están implicadas en el metabolismo de otros fármacos como: CYP1A2 (p. ej., warfarina, teofilina, propranolol, tizanidina), CYP2C9 (p. ej., , warfarina), CYP3A4 (p. ej., alprazolam) y CYP2C19 (p. ej., omeprazol).
Los datos in vitro sugieren que la fluvoxamina es un inhibidor relativamente débil de CYP2D6.
Aproximadamente el 7% de la población normal tiene un código genético que conduce a niveles reducidos de actividad de CYP2D6. Se ha hecho referencia a estos individuos como “metabolizadores lentos” (PM) de fármacos como la ruinoquina, el dextrometorfano y los antidepresivos tricíclicos. Si bien ninguno de los fármacos estudiados para las interacciones farmacológicas afectó significativamente la farmacocinética de fluvox 50 mgamina, un estudio in vivo de la farmacocinética de dosis única de fluvoxamina en sujetos 13 PM demostró propiedades farmacocinéticas alteradas en comparación con 16 "metabolizadores rápidos" (EM): media de Cmax, AUC , y la vida media se incrementaron en un 52 %, 200 % y 62 %, respectivamente, en el grupo PM en comparación con el grupo EM. Esto sugiere que fluvox 100mgamine es metabolizado, al menos en parte, por CYP2D6. Se recomienda precaución en pacientes que se sabe que tienen niveles reducidos de actividad de CYP2D6 y aquellos que reciben medicamentos concomitantes que se sabe que inhiben esta isoenzima del citocromo P450 (p. ej., quinidina).
El metabolismo de la fluvoxamina no se ha caracterizado por completo y no se han estudiado los efectos de la potente inhibición de la isoenzima del citocromo P450, como la inhibición del ketoconazol de CYP3A4, sobre el metabolismo de la fluvoxamina 100 mg.
Es posible una interacción clínicamente significativa de fluvoxamina con medicamentos que tienen una relación terapéutica estrecha, como pimozida, warfarina, teofilina, ciertas benzodiazepinas, omeprazol y fenitoína. Si los comprimidos de maleato de amina de 100 mg de Fluvox se van a administrar junto con un fármaco que se elimina a través del metabolismo oxidativo y tiene una ventana terapéutica estrecha, los niveles plasmáticos y/o los efectos farmacodinámicos del último fármaco deben controlarse de cerca, al menos hasta que se alcancen las condiciones de estado estacionario. alcanzado [ver CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES ].
Fármacos activos en el SNC
Antipsicóticos: Ver ADVERTENCIAS Y PRECAUCIONES .
Benzodiazepinas: Ver ADVERTENCIAS Y PRECAUCIONES .
Alprazolam: Ver ADVERTENCIAS Y PRECAUCIONES .
diazepam: Ver ADVERTENCIAS Y PRECAUCIONES .
Lorazepam: Un estudio de dosis múltiples de maleato de fluvoxamina (50 mg dos veces al día) en voluntarios masculinos sanos (N=12) y una dosis única de lorazepam (dosis única de 4 mg) no indicó una interacción farmacocinética significativa. En promedio, tanto el lorazepam solo como el lorazepam con fluvoxamina produjeron disminuciones sustanciales en el funcionamiento cognitivo; sin embargo, la coadministración de fluvoxamina y lorazepam no produjo disminuciones medias mayores en comparación con lorazepam solo.
Alcohol: Los estudios que incluyeron dosis únicas de 40 g de etanol (administración oral en un estudio e intravenosa en el otro) y dosis múltiples con fluvox 100 mg de maleato de amina (50 mg dos veces al día) no revelaron ningún efecto de ninguno de los fármacos sobre la farmacocinética o la farmacodinámica del otro. Al igual que con otros medicamentos psicotrópicos, se debe advertir a los pacientes que eviten el alcohol mientras toman tabletas de maleato de fluvoxamina.
Carbamazepina: Se han notificado niveles elevados de carbamazepina y síntomas de toxicidad con la coadministración de fluvox 100 mg de maleato de amina y carbamazepina.
Clozapina: Ver ADVERTENCIAS Y PRECAUCIONES .
Litio: Al igual que con otros medicamentos serotoninérgicos, el litio puede aumentar los efectos serotoninérgicos de la fluvoxamina y, por lo tanto, la combinación debe usarse con precaución. Se han informado convulsiones con la coadministración de fluvox 50 mg de maleato de amina y litio.
Metadona: Ver ADVERTENCIAS Y PRECAUCIONES .
Inhibidores de la monoaminooxidasa: Ver DOSIFICACIÓN Y ADMINISTRACIÓN , CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES .
Pimozida: Ver CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES .
Ramelteón: Ver ADVERTENCIAS Y PRECAUCIONES .
Fármacos serotoninérgicos: Ver DOSIFICACIÓN Y ADMINISTRACIÓN , CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES .
tacrina: En un estudio de 13 voluntarios varones sanos, una dosis única de 40 mg de tacrina añadida a fluvox 50 mgamine 100 mg/día administrados en estado estacionario se asoció con aumentos de cinco y ocho veces en la Cmax y el AUC de tacrina, respectivamente, en comparación con la administración de tacrina sola. Cinco sujetos experimentaron náuseas, vómitos, sudoración y diarrea después de la coadministración, en consonancia con los efectos colinérgicos de la tacrina.
Tioridazina: Ver CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES .
Tizanidina: Ver CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES .
Antidepresivos tricíclicos (ATC): Se ha informado un aumento significativo de los niveles de TCA en plasma con la coadministración de maleato de fluvoxamina y amitriptilina, clomipramina o imipramina. Se recomienda precaución con la coadministración de comprimidos de maleato de fluvoxamina y TCA; Es posible que sea necesario controlar las concentraciones plasmáticas de TCA, y es posible que sea necesario reducir la dosis de TCA.
Triptanos: Ha habido raros informes posteriores a la comercialización del síndrome serotoninérgico con el uso de un ISRS y un triptán. Si el tratamiento concomitante de fluvox 50 mgamine con un triptán está clínicamente justificado, se recomienda una cuidadosa observación del paciente, particularmente durante el inicio del tratamiento y los aumentos de dosis [ver ADVERTENCIAS Y PRECAUCIONES ].
Sumatriptán: Ha habido informes posteriores a la comercialización raros que describen pacientes con debilidad, hiperreflexia y falta de coordinación después del uso de un inhibidor selectivo de la recaptación de serotonina (ISRS) y sumatriptán. Si el tratamiento concomitante con sumatriptán y un ISRS (p. ej., fluoxetina, fluvoxamina, paroxetina, sertralina) está clínicamente justificado, se recomienda la observación adecuada del paciente.
Triptófano: El triptófano puede aumentar los efectos serotoninérgicos de la fluvoxamina y, por lo tanto, la combinación debe usarse con precaución. Se han notificado vómitos intensos con la coadministración de maleato de fluvoxamina y triptófano [ver ADVERTENCIAS Y PRECAUCIONES ].
Otras drogas
alosetrón: Ver CONTRAINDICACIONES , ADVERTENCIAS Y PRECAUCIONES , y el prospecto de Lotronex™ (alosetrón).
Digoxina: La administración de fluvox 100 mg de maleato de amina, 100 mg al día durante 18 días (N=8), no afectó significativamente la farmacocinética de una dosis intravenosa única de 1,25 mg de digoxina.
diltiazem: Se ha informado bradicardia con la coadministración de maleato de fluvoxamina y diltiazem.
Mexiletina: Ver ADVERTENCIAS Y PRECAUCIONES .
Propranolol y otros bloqueadores beta: La coadministración de 100 mg de maleato de fluvoxamina por día y 160 mg de propranolol por día en voluntarios normales resultó en un aumento promedio de cinco veces (rango de 2 a 17) en las concentraciones plasmáticas mínimas de propranolol. En este estudio, hubo una ligera potenciación de la reducción de la frecuencia cardíaca inducida por propranolol y de la reducción de la presión diastólica durante el ejercicio.
Se ha notificado un caso de bradicardia e hipotensión y un segundo caso de hipotensión ortostática con la coadministración de maleato de fluvoxamina y metoprolol.
Si se coadministran propranolol o metoprolol con comprimidos de maleato de amina de 50 mg de Fluvox, se recomienda una reducción de la dosis inicial de betabloqueante y una titulación más cuidadosa de la dosis. No se requiere ajuste de dosis para las tabletas de maleato de fluvoxamina.
La coadministración de maleato de fluvoxamina 100 mg por día con atenolol 100 mg por día (N=6) no afectó las concentraciones plasmáticas de atenolol. A diferencia del propranolol y el metoprolol, que sufren metabolismo hepático, el atenolol se elimina principalmente por excreción renal.
Teofilina: Ver ADVERTENCIAS Y PRECAUCIONES .
Warfarina y otras drogas que interfieren con la hemostasia (AINE, aspirina, etc.): Ver ADVERTENCIAS Y PRECAUCIONES .
Efectos del tabaquismo sobre el metabolismo de la fluvoxamina
Los fumadores tuvieron un aumento del 25 % en el metabolismo de fluvox 100 mgamine en comparación con los no fumadores.
Terapia Electroconvulsiva (TEC)
No existen estudios clínicos que establezcan los beneficios o riesgos del uso combinado de ECT y fluvox 100mgamine maleate.
Abuso y dependencia de drogas
Sustancia controlada
Las tabletas de maleato de fluvoxamina no son una sustancia controlada.
Dependencia
El potencial de abuso, tolerancia y dependencia física con fluvox 100mgamine maleate ha sido estudiado en un modelo de primates no humanos. No se encontraron evidencias de fenómenos de dependencia. Los efectos de interrupción de las tabletas de maleato de fluvoxamina no se evaluaron sistemáticamente en ensayos clínicos controlados. Las tabletas de maleato de fluvoxamina no se estudiaron sistemáticamente en los ensayos clínicos por su potencial de abuso, pero no hubo indicios de un comportamiento de búsqueda de drogas en los ensayos clínicos. Cabe señalar, sin embargo, que los pacientes con riesgo de dependencia a las drogas fueron sistemáticamente excluidos de los estudios de investigación de fluvox 100 mg de maleato de amina. Por lo general, no es posible predecir, sobre la base de la experiencia clínica preclínica o previa a la comercialización, el grado en que un fármaco activo sobre el SNC será mal utilizado, desviado y/o abusado una vez comercializado. En consecuencia, los médicos deben evaluar cuidadosamente a los pacientes en busca de antecedentes de abuso de drogas y seguir de cerca a dichos pacientes, observándolos en busca de signos de uso indebido o abuso de maleato de fluvoxamina (es decir, desarrollo de tolerancia, aumento de la dosis, comportamiento de búsqueda de drogas).
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Empeoramiento clínico y riesgo de suicidio
Los pacientes con trastorno depresivo mayor (MDD), tanto adultos como pediátricos, pueden experimentar un empeoramiento de su depresión y/o la aparición de ideación y comportamiento suicida (suicidalidad) o cambios inusuales en el comportamiento, estén o no tomando medicamentos antidepresivos, y esto el riesgo puede persistir hasta que ocurra una remisión significativa. El suicidio es un riesgo conocido de depresión y ciertos otros trastornos psiquiátricos, y estos trastornos en sí mismos son los predictores más fuertes de suicidio. Sin embargo, desde hace mucho tiempo existe la preocupación de que los antidepresivos puedan tener un papel en la inducción del empeoramiento de la depresión y la aparición de tendencias suicidas en ciertos pacientes durante las primeras fases del tratamiento. Los análisis agrupados de ensayos controlados con placebo a corto plazo de medicamentos antidepresivos (ISRS y otros) mostraron que estos medicamentos aumentan el riesgo de pensamientos y conductas suicidas (tendencia suicida) en niños, adolescentes y adultos jóvenes (de 18 a 24 años) con trastorno depresivo mayor ( MDD) y otros trastornos psiquiátricos. Los estudios a corto plazo no mostraron un aumento en el riesgo de tendencias suicidas con antidepresivos en comparación con placebo en adultos mayores de 24 años; hubo una reducción con los antidepresivos en comparación con el placebo en adultos de 65 años o más.
Los análisis agrupados de ensayos controlados con placebo en niños y adolescentes con TDM, trastorno obsesivo compulsivo (TOC) u otros trastornos psiquiátricos incluyeron un total de 24 ensayos a corto plazo de 9 fármacos antidepresivos en más de 4400 pacientes. Los análisis agrupados de ensayos controlados con placebo en adultos con MDD u otros trastornos psiquiátricos incluyeron un total de 295 ensayos a corto plazo (duración media de 2 meses) de 11 fármacos antidepresivos en más de 77 000 pacientes. Hubo una variación considerable en el riesgo de suicidio entre los fármacos, pero una tendencia hacia un aumento en los pacientes más jóvenes para casi todos los fármacos estudiados. Hubo diferencias en el riesgo absoluto de suicidio entre las diferentes indicaciones, con la mayor incidencia en MDD. Sin embargo, las diferencias de riesgo (fármaco frente a placebo) fueron relativamente estables dentro de los estratos de edad y entre las indicaciones. Estas diferencias de riesgo (diferencia fármaco-placebo en el número de casos de tendencias suicidas por cada 1000 pacientes tratados) se proporcionan en la Tabla 1.
TABLA 1: DIFERENCIAS MEDICAMENTO-PLACEBO EN NÚMERO DE CASOS DE SUICIDALIDAD POR 1000 PACIENTES TRATADOS
No se produjeron suicidios en ninguno de los ensayos pediátricos. Hubo suicidios en los ensayos con adultos, pero el número no fue suficiente para llegar a ninguna conclusión sobre el efecto del fármaco sobre el suicidio.
Se desconoce si el riesgo de suicidio se extiende al uso a largo plazo, es decir, más allá de varios meses. Sin embargo, existe evidencia sustancial de ensayos de mantenimiento controlados con placebo en adultos con depresión de que el uso de antidepresivos puede retrasar la recurrencia de la depresión.
Todos los pacientes que reciben tratamiento con antidepresivos por cualquier indicación deben ser monitoreados adecuadamente y observados de cerca por si empeoran clínicamente, tienen tendencias suicidas y cambios inusuales en el comportamiento, especialmente durante los meses iniciales de un ciclo de terapia con medicamentos, o en momentos de cambios de dosis, ya sea aumentos o disminuye.
Los siguientes síntomas, ansiedad, agitación, ataques de pánico, insomnio, irritabilidad, hostilidad, agresividad, impulsividad, acatisia (inquietud psicomotora), hipomanía y manía, se han informado en pacientes adultos y pediátricos que también reciben tratamiento con antidepresivos para el trastorno depresivo mayor como para otras indicaciones, tanto psiquiátricas como no psiquiátricas. Aunque no se ha establecido un vínculo causal entre la aparición de tales síntomas y el empeoramiento de la depresión y/o la aparición de impulsos suicidas, existe la preocupación de que tales síntomas puedan representar precursores de tendencias suicidas emergentes.
Se debe considerar cambiar el régimen terapéutico, incluida la posibilidad de suspender el medicamento, en pacientes cuya depresión empeora persistentemente, o que están experimentando tendencias suicidas emergentes o síntomas que podrían ser precursores de un empeoramiento de la depresión o tendencias suicidas, especialmente si estos síntomas son severos, abruptos. en el inicio, o no formaban parte de los síntomas de presentación del paciente.
Si se ha tomado la decisión de suspender el tratamiento, se debe disminuir la medicación tan rápido como sea posible, pero reconociendo que la interrupción abrupta puede estar asociada con ciertos síntomas y riesgos [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Se debe alertar a las familias y cuidadores de pacientes que reciben tratamiento con antidepresivos por trastorno depresivo mayor u otras indicaciones, tanto psiquiátricas como no psiquiátricas, sobre la necesidad de monitorear a los pacientes para detectar la aparición de agitación, irritabilidad, cambios inusuales en el comportamiento y los demás síntomas descritos anteriormente. , así como el surgimiento de tendencias suicidas, e informar dichos síntomas de inmediato a los proveedores de atención médica. Dicho seguimiento debe incluir la observación diaria por parte de las familias y los cuidadores. Las recetas de tabletas de maleato de fluvoxamina deben hacerse para la cantidad más pequeña de tabletas compatible con un buen manejo del paciente, a fin de reducir el riesgo de sobredosis.
Detección de pacientes para el trastorno bipolar
Un episodio depresivo mayor puede ser la presentación inicial del trastorno bipolar. En general, se cree (aunque no se ha establecido en ensayos controlados) que tratar un episodio de este tipo con un antidepresivo solo puede aumentar la probabilidad de precipitación de un episodio mixto/maníaco en pacientes con riesgo de trastorno bipolar. Se desconoce si alguno de los síntomas descritos anteriormente representa tal conversión. Sin embargo, antes de iniciar el tratamiento con un antidepresivo, los pacientes con síntomas depresivos deben someterse a un cribado adecuado para determinar si tienen riesgo de trastorno bipolar; dicha evaluación debe incluir un historial psiquiátrico detallado, incluidos antecedentes familiares de suicidio, trastorno bipolar y depresión. Cabe señalar que las tabletas de maleato de amina de 50 mg de Fluvox no están aprobadas para su uso en el tratamiento de la depresión bipolar.
Síndrome de serotonina
Se ha informado el desarrollo de un síndrome serotoninérgico potencialmente mortal con IRSN e ISRS, incluidos los comprimidos de maleato de fluvoxamina, solos, pero particularmente con el uso concomitante de medicamentos serotoninérgicos (incluidos triptanes, antidepresivos tricíclicos, fentanilo, litio, tramadol, triptófano, busipirona, anfetaminas). , y la hierba de San Juan) y con fármacos que alteran el metabolismo de la serotonina (en particular, los IMAO, tanto los destinados a tratar trastornos psiquiátricos como también otros, como linezolid y azul de metileno intravenoso).
Los síntomas del síndrome serotoninérgico pueden incluir cambios en el estado mental (p. ej., agitación, alucinaciones, delirio y coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, mareos, diaforesis, sofocos, hipertermia), aberraciones neuromusculares (p. ej., temblor, rigidez, mioclonías, hiperreflexia, falta de coordinación), convulsiones y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea). Los pacientes deben ser monitoreados por la aparición del síndrome serotoninérgico.
Está contraindicado el uso concomitante de comprimidos de maleato de fluvoxamina con IMAO destinados a tratar trastornos psiquiátricos. Las tabletas de maleato de fluvoxamina tampoco deben iniciarse en un paciente que está siendo tratado con IMAO como linezolid o azul de metileno intravenoso. Todos los informes con azul de metileno que proporcionaron información sobre la vía de administración involucraron la administración intravenosa en el rango de dosis de 1 mg/kg a 8 mg/kg. Ningún informe involucró la administración de azul de metileno por otras vías (como tabletas orales o inyección local en tejido) o en dosis más bajas. Puede haber circunstancias en las que sea necesario iniciar el tratamiento con un IMAO como linezolida o azul de metileno intravenoso en un paciente que toma Fluvox 50 mg comprimidos de maleato de amina. Las tabletas de maleato de amina Fluvox 50 mg deben interrumpirse antes de iniciar el tratamiento con el IMAO [ver CONTRAINDICACIONES , DOSIFICACIÓN Y ADMINISTRACIÓN ].
Si está clínicamente justificado el uso concomitante de tabletas de maleato de fluvoxamina con otros medicamentos serotoninérgicos, incluidos triptanos, antidepresivos tricíclicos, fentanilo, litio, tramadol, buspirona, triptófano, anfetaminas y hierba de San Juan, se debe advertir a los pacientes sobre una aumento potencial del riesgo de síndrome serotoninérgico, particularmente durante el inicio del tratamiento y los aumentos de dosis.
El tratamiento con tabletas de maleato de fluvoxamina y cualquier agente serotoninérgico concomitante debe suspenderse inmediatamente si ocurren los eventos anteriores y debe iniciarse un tratamiento sintomático de apoyo.
Glaucoma de ángulo cerrado
La dilatación pupilar que ocurre después del uso de muchos medicamentos antidepresivos, incluidas las tabletas de maleato de fluvoxamina, puede desencadenar un ataque de ángulo cerrado en un paciente con ángulos anatómicamente estrechos que no tienen una iridectomía permeable.
Interacción potencial de tioridazina
Se evaluó el efecto de la fluvoxamina (25 mg dos veces al día durante una semana) sobre las concentraciones de tioridazina en estado estacionario en 10 pacientes masculinos hospitalizados con esquizofrenia. Las concentraciones de tioridazina y sus dos metabolitos activos, mesoridazina y sulforidazina, se triplicaron después de la coadministración de fluvox 100 mgamina.
La administración de tioridazina produce una prolongación del intervalo QTc relacionada con la dosis, que se asocia con arritmias ventriculares graves, como arritmias tipo torsades de pointes y muerte súbita. Es probable que esta experiencia subestime el grado de riesgo que podría ocurrir con dosis más altas de tioridazina. Además, el efecto de fluvox 100mgamine puede ser aún más pronunciado cuando se administra en dosis más altas. Por lo tanto, la fluvoxamina y la tioridazina no deben administrarse conjuntamente [ver CONTRAINDICACIONES ].
Interacción potencial de tizanidina
La fluvoxamina es un potente inhibidor de CYP1A2 y la tizanidina es un sustrato de CYP1A2. El efecto de fluvox 50 mgamine (100 mg al día durante 4 días) sobre la farmacocinética y la farmacodinámica de una dosis única de 4 mg de tizanidina se ha estudiado en 10 sujetos varones sanos. La Cmax de tizanidina aumentó aproximadamente 12 veces (rango de 5 a 32 veces), la vida media de eliminación aumentó casi 3 veces y el AUC aumentó 33 veces (rango de 14 a 103 veces). El efecto máximo medio sobre la presión arterial fue una disminución de 35 mm Hg en la presión arterial sistólica, una disminución de 20 mm Hg en la presión arterial diastólica y una disminución de 4 latidos/min en la frecuencia cardíaca. La somnolencia aumentó significativamente y el rendimiento en la tarea psicomotora se vio significativamente afectado. La fluvoxamina y la tizanidina no deben usarse juntas [ver CONTRAINDICACIONES ].
Interacción potencial de pimozida
La pimozida es metabolizada por la isoenzima del citocromo P4503A4 y se ha demostrado que el ketoconazol, un potente inhibidor de CYP3A4, bloquea el metabolismo de este fármaco, lo que provoca un aumento de las concentraciones plasmáticas del fármaco original. Un aumento de la concentración plasmática de pimozida provoca una prolongación del intervalo QT y se ha asociado con taquicardia ventricular tipo torsades de pointes, a veces fatal. Como se indica a continuación, se ha observado una interacción farmacocinética sustancial para fluvox 100 mgamine en combinación con alprazolam, un fármaco que se sabe que es metabolizado por CYP3A4. Aunque no se ha demostrado definitivamente que fluvox 100 mgamine es un potente inhibidor de CYP3A4, es probable que lo sea, dada la interacción sustancial de fluvox 50 mgamine con alprazolam. En consecuencia, se recomienda no usar fluvoxamina en combinación con pimozida [ver CONTRAINDICACIONES ].
Interacción potencial de alosetrón
Debido a que alosetrón es metabolizado por una variedad de enzimas metabolizadoras de fármacos CYP hepáticos, los inductores o inhibidores de estas enzimas pueden cambiar la depuración de alosetrón. Fluvox 50mgamine es un inhibidor potente conocido de CYP1A2 y también inhibe CYP3A4, CYP2C9 y CYP2C19. En un estudio farmacocinético, 40 mujeres sanas recibieron fluvox 100 mgamina en dosis crecientes de 50 mg a 200 mg al día durante 16 días, con administración conjunta de alosetrón 1 mg el último día. Fluvox 50 mgamine aumentó la concentración plasmática media de alosetrón (AUC) aproximadamente 6 veces y prolongó la vida media aproximadamente 3 veces. [Ver CONTRAINDICACIONES y Lotronex™ (alosetrón) prospecto].
Otras interacciones farmacológicas potencialmente importantes
Benzodiazepinas
Las benzodiazepinas metabolizadas por oxidación hepática (p. ej., alprazolam, midazolam, triazolam, etc.) deben usarse con precaución porque es probable que la fluvoxamina reduzca el aclaramiento de estos fármacos. Es poco probable que fluvox 100 mgamine afecte la depuración de las benzodiazepinas metabolizadas por glucuronidación (p. ej., lorazepam, oxazepam, temazepam).
alprazolam
Cuando se coadministraron maleato de fluvoxamina (100 mg una vez al día) y alprazolam (1 mg una vez al día) hasta alcanzar el estado estacionario, las concentraciones plasmáticas y otros parámetros farmacocinéticos (AUC, Cmax, T½) de alprazolam fueron aproximadamente el doble de los observados cuando se administró alprazolam solo; el aclaramiento oral se redujo en aproximadamente un 50%. Las concentraciones plasmáticas elevadas de alprazolam resultaron en una disminución del rendimiento psicomotor y de la memoria. Esta interacción, que no se ha investigado con dosis más altas de fluvoxamina, puede ser más pronunciada si se coadministra una dosis diaria de 300 mg, especialmente porque fluvox 50 mgamine muestra una farmacocinética no lineal en el rango de dosis de 100-300 mg. Si se coadministra alprazolam con tabletas de maleato de amina de 50 mg de Fluvox, la dosis inicial de alprazolam debe reducirse al menos a la mitad y se recomienda ajustar la dosis a la dosis eficaz más baja. No se requiere ajuste de dosis para las tabletas de maleato de amina Fluvox de 100 mg.
diazepam
En general, no se recomienda la administración conjunta de tabletas de maleato de fluvoxamina y diazepam. Debido a que la fluvoxamina reduce la depuración tanto del diazepam como de su metabolito activo, Ndesmetildiazepam, existe una gran probabilidad de acumulación sustancial de ambas especies durante la coadministración crónica.
La evidencia que respalda la conclusión de que no es aconsejable coadministrar fluvoxamina y diazepam se deriva de un estudio en el que a voluntarios sanos que tomaban 150 mg/día de fluvoxamina 50 mg se les administró una dosis oral única de 10 mg de diazepam. En estos sujetos (N=8), el aclaramiento de diazepam se redujo en un 65 % y el de N-desmetildiazepam a un nivel demasiado bajo para medirlo en el transcurso del estudio de 2 semanas de duración.
Es probable que esta experiencia subestime significativamente el grado de acumulación que podría ocurrir con la administración repetida de diazepam. Además, como se señaló con el alprazolam, el efecto de fluvox 50mgamine puede ser incluso más pronunciado cuando se administra en dosis más altas.
En consecuencia, el diazepam y la fluvoxamina normalmente no deben administrarse conjuntamente.
clozapina
Se han informado niveles séricos elevados de clozapina en pacientes que toman fluvox 100 mg de maleato de amina y clozapina. Dado que las convulsiones y la hipotensión ortostática relacionadas con la clozapina parecen estar relacionadas con la dosis, el riesgo de estos eventos adversos puede ser mayor cuando se administran conjuntamente fluvoxamina y clozapina. Los pacientes deben ser monitoreados de cerca cuando el maleato de fluvoxamina y la clozapina se usan al mismo tiempo.

Metadona
Se han notificado proporciones de metadona (nivel plasmático:dosis) significativamente aumentadas cuando se administró fluvox 50 mg de maleato de amina a pacientes que recibían tratamiento de mantenimiento con metadona, con síntomas de intoxicación por opioides en un paciente. Se informaron síntomas de abstinencia de opiáceos después de la suspensión del maleato de fluvoxamina en otro paciente.
mexiletina
El efecto de la fluvoxamina en estado estacionario (50 mg dos veces al día durante 7 días) sobre la farmacocinética de una dosis única de mexiletina (200 mg) se evaluó en 6 hombres japoneses sanos. El aclaramiento de mexiletina se redujo en un 38 % luego de la coadministración con fluvox 100 mgamine en comparación con mexiletina sola. Si se administran conjuntamente fluvoxamina y mexiletina, se deben controlar los niveles séricos de mexiletina.
Ramelteón
Cuando se administró fluvox 50mgamine 100 mg dos veces al día durante 3 días antes de la coadministración de una dosis única de ramelteon 16 mg y fluvoxamine, el AUC para ramelteon aumentó aproximadamente 190 veces y la Cmax aumentó aproximadamente 70 veces en comparación con ramelteon administrado solo. Ramelteon no debe usarse en combinación con fluvoxamina.
teofilina
Se evaluó el efecto de fluvox 50 mgamina en estado estacionario (50 mg dos veces al día) sobre la farmacocinética de una dosis única de teofilina (375 mg como 442 mg de aminofilina) en 12 voluntarios masculinos sanos no fumadores. El aclaramiento de teofilina se redujo aproximadamente 3 veces. Por lo tanto, si se coadministra teofilina con maleato de fluvoxamina, su dosis debe reducirse a un tercio de la dosis diaria habitual de mantenimiento y deben controlarse las concentraciones plasmáticas de teofilina. No se requiere ajuste de dosis para las tabletas de maleato de amina Fluvox de 100 mg.
Warfarina y otras drogas que interfieren con la hemostasia (AINE, aspirina, etc.)
La liberación de serotonina por las plaquetas juega un papel importante en la hemostasia. Los estudios epidemiológicos del diseño de cohortes y de casos y controles han demostrado una asociación entre el uso de fármacos psicotrópicos que interfieren con la recaptación de serotonina y la aparición de hemorragia digestiva alta. Estos estudios también han demostrado que el uso concurrente de un AINE o aspirina puede potenciar este riesgo de hemorragia. Por lo tanto, se debe advertir a los pacientes sobre el uso concomitante de estos fármacos con fluvoxamina [ver ADVERTENCIAS Y PRECAUCIONES ].
warfarina
Cuando se administró fluvox 50 mg de maleato de amina (50 mg tres veces al día) junto con warfarina durante dos semanas, las concentraciones plasmáticas de warfarina aumentaron en un 98 % y los tiempos de protrombina se prolongaron. Por lo tanto, a los pacientes que reciben anticoagulantes orales y comprimidos de maleato de fluvoxamina se les debe controlar el tiempo de protrombina y ajustar la dosis de anticoagulante en consecuencia. No se requiere ajuste de dosis para las tabletas de maleato de fluvoxamina.
Interrupción del tratamiento con tabletas de maleato de amina Fluvox 100mg
Durante la comercialización de las tabletas de maleato de fluvoxamina y otros ISRS e IRSN (inhibidores de la recaptación de serotonina y norepinefrina), ha habido informes espontáneos de eventos adversos que ocurren tras la interrupción de estos medicamentos, particularmente cuando es abrupto, incluidos los siguientes: estado de ánimo disfórico, irritabilidad, agitación, mareos , trastornos sensoriales (p. ej., parestesias, como sensaciones de descarga eléctrica), ansiedad, confusión, dolor de cabeza, letargo, labilidad emocional, insomnio e hipomanía. Si bien estos eventos generalmente son autolimitados, ha habido informes de síntomas graves de interrupción.
Se debe monitorear a los pacientes para detectar estos síntomas cuando suspendan el tratamiento con tabletas de maleato de amina Fluvox de 50 mg. Siempre que sea posible, se recomienda una reducción gradual de la dosis en lugar de una interrupción brusca. Si aparecen síntomas intolerables tras una disminución de la dosis o tras la interrupción del tratamiento, se puede considerar la reanudación de la dosis prescrita anteriormente. Posteriormente, el médico puede continuar disminuyendo la dosis pero a un ritmo más gradual [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Sangrado anormal
Los ISRS y los IRSN, incluidos los comprimidos de maleato de fluvoxamina, pueden aumentar el riesgo de eventos hemorrágicos. El uso concomitante de aspirina, medicamentos antiinflamatorios no esteroideos, warfarina y otros anticoagulantes puede aumentar este riesgo. Informes de casos y estudios epidemiológicos (casos y controles y diseño de cohortes) han demostrado una asociación entre el uso de fármacos que interfieren con la recaptación de serotonina y la aparición de hemorragia gastrointestinal. Los episodios hemorrágicos relacionados con los ISRS y los IRSN van desde equimosis, hematomas, epistaxis y petequias hasta hemorragias potencialmente mortales.
Se debe advertir a los pacientes sobre el riesgo de sangrado asociado con el uso concomitante de tabletas de maleato de amina Fluvox de 100 mg y AINE, aspirina u otros medicamentos que afectan la coagulación [ver ADVERTENCIAS Y PRECAUCIONES ].
Activación de manía/hipomanía
Durante los estudios previos a la comercialización en los que participaron principalmente pacientes deprimidos, se produjo hipomanía o manía en aproximadamente el 1 % de los pacientes tratados con fluvoxamina. En un estudio de TOC pediátrico de diez semanas, 2 de 57 pacientes (4 %) tratados con fluvoxamina experimentaron reacciones maníacas, en comparación con ninguno de los 63 pacientes que recibieron placebo. También se ha notificado activación de manía/hipomanía en una pequeña proporción de pacientes con trastorno afectivo mayor que fueron tratados con otros antidepresivos comercializados. Al igual que con todos los antidepresivos, las tabletas de maleato de fluvoxamina deben usarse con precaución en pacientes con antecedentes de manía.
convulsiones
Durante los estudios previos a la comercialización, se informaron convulsiones en el 0,2 % de los pacientes tratados con fluvoxamina. Se recomienda precaución cuando el fármaco se administre a pacientes con antecedentes de trastornos convulsivos. Fluvox 100mgamine debe evitarse en pacientes con epilepsia inestable y los pacientes con epilepsia controlada deben ser monitoreados cuidadosamente. El tratamiento con fluvoxamina debe interrumpirse si se producen convulsiones o si aumenta la frecuencia de las convulsiones.
hiponatremia
Puede ocurrir hiponatremia como resultado del tratamiento con ISRS e IRSN, incluidas las tabletas de maleato de fluvoxamina. En muchos casos, esta hiponatremia parece ser el resultado del síndrome de hormona antidiurética inadecuada (SIADH). Se han notificado casos con sodio sérico inferior a 110 mmol/L. Los pacientes de edad avanzada pueden tener un mayor riesgo de desarrollar hiponatremia con los ISRS y los IRSN [ver Uso en poblaciones específicas ]. Además, los pacientes que toman diuréticos o que tienen depleción de volumen pueden tener un mayor riesgo. En pacientes con hiponatremia sintomática, se debe considerar la suspensión de Fluvox 100mgamine Maleate Tablets y se debe instituir la intervención médica adecuada.
Los signos y síntomas de la hiponatremia incluyen dolor de cabeza, dificultad para concentrarse, deterioro de la memoria, confusión, debilidad e inestabilidad, lo que puede provocar caídas. Los signos y síntomas asociados con casos más graves y/o agudos incluyen alucinaciones, síncope, convulsiones, coma, paro respiratorio y muerte.
Uso en pacientes con enfermedades concomitantes
La experiencia clínica supervisada de cerca con Fluvox 50 mg comprimidos de maleato de amina en pacientes con enfermedades sistémicas concomitantes es limitada. Se recomienda precaución al administrar tabletas de maleato de fluvoxamina a pacientes con enfermedades o condiciones que podrían afectar las respuestas hemodinámicas o el metabolismo.
Las tabletas de maleato de fluvoxamina no han sido evaluadas ni utilizadas en una medida apreciable en pacientes con antecedentes recientes de infarto de miocardio o enfermedad cardíaca inestable. Los pacientes con estos diagnósticos fueron sistemáticamente excluidos de muchos estudios clínicos durante las pruebas previas a la comercialización del producto. La evaluación de los electrocardiogramas de pacientes con depresión o TOC que participaron en estudios previos a la comercialización no reveló diferencias entre fluvox 100 mgamine y placebo en la aparición de cambios en el ECG clínicamente importantes.
Pacientes con insuficiencia hepática
En pacientes con disfunción hepática, el aclaramiento de amina de fluvox 50 mg se redujo en aproximadamente un 30 %. Los pacientes con disfunción hepática deben comenzar con una dosis baja de tabletas de maleato de fluvoxamina y aumentarla lentamente con un control cuidadoso.
Pruebas de laboratorio
No se recomiendan pruebas de laboratorio específicas.
Disfunción sexual
El uso de ISRS, incluidas las tabletas de maleato de fluvoxamina, puede causar síntomas de disfunción sexual [ver REACCIONES ADVERSAS 4)]. En pacientes masculinos, el uso de ISRS puede provocar retraso o falla en la eyaculación, disminución de la libido y disfunción eréctil. En pacientes femeninas, el uso de ISRS puede provocar una disminución de la libido y un orgasmo retrasado o ausente.
Es importante que los prescriptores indaguen sobre la función sexual antes de iniciar el tratamiento con tabletas de maleato de fluvoxamina y que indaguen específicamente sobre los cambios en la función sexual durante el tratamiento, ya que es posible que la función sexual no se informe espontáneamente. Cuando se evalúan los cambios en la función sexual, es importante obtener una historia clínica detallada (que incluya el momento del inicio de los síntomas) porque los síntomas sexuales pueden tener otras causas, incluido el trastorno psiquiátrico subyacente. Discutir posibles estrategias de manejo para ayudar a los pacientes a tomar decisiones informadas sobre el tratamiento.
Información de asesoramiento para pacientes
Aconseje al paciente que lea la etiqueta del paciente aprobada por la FDA ( Guía de medicamentos ).
Los prescriptores u otros profesionales de la salud deben informar a los pacientes, sus familias y sus cuidadores sobre los beneficios y riesgos asociados con el tratamiento con tabletas de maleato de fluvoxamina y deben asesorarlos sobre el uso apropiado. Se encuentra disponible una Guía del medicamento para el paciente sobre "Medicamentos antidepresivos, depresión y otras enfermedades mentales graves y pensamientos o acciones suicidas" para las tabletas de maleato de amina Fluvox de 100 mg. El prescriptor o el profesional de la salud debe instruir a los pacientes, sus familias y sus cuidadores para que lean la Guía del medicamento y debe ayudarlos a comprender su contenido. Los pacientes deben tener la oportunidad de discutir el contenido de la Guía del medicamento y obtener respuestas a cualquier pregunta que puedan tener. El texto completo de la Guía del medicamento se reproduce al final de este documento.
Se debe advertir a los pacientes sobre los siguientes problemas y pedirles que alerten a su prescriptor si ocurren mientras toman Fluvox 100mg en tabletas de maleato de amina.
Empeoramiento clínico y riesgo de suicidio
Se debe alentar a los pacientes, sus familias y sus cuidadores a estar alerta ante la aparición de ansiedad, agitación, ataques de pánico, insomnio, irritabilidad, hostilidad, agresividad, impulsividad, acatisia (inquietud psicomotora), hipomanía, manía, otros cambios inusuales en el comportamiento. , empeoramiento de la depresión e ideación suicida, especialmente al principio del tratamiento con antidepresivos y cuando la dosis se ajusta hacia arriba o hacia abajo. Se debe recomendar a las familias y cuidadores de los pacientes que estén atentos a la aparición de dichos síntomas en el día a día, ya que los cambios pueden ser abruptos. Dichos síntomas deben informarse al prescriptor del paciente o al profesional de la salud, especialmente si son graves, de inicio repentino o no formaban parte de los síntomas de presentación del paciente. Síntomas como estos pueden estar asociados con un mayor riesgo de pensamientos y conductas suicidas e indican la necesidad de un control muy estricto y posiblemente cambios en la medicación [ver ADVERTENCIA EN CAJA , ADVERTENCIAS Y PRECAUCIONES ]
Síndrome de serotonina
Se debe advertir a los pacientes sobre el riesgo de síndrome serotoninérgico, particularmente con el uso concomitante de fluvoxamina con otros agentes serotoninérgicos (incluidos triptanos, antidepresivos tricíclicos, fentanilo, litio, tramadol, triptófano, buspirona, anfetaminas y hierba de San Juan). [ver ADVERTENCIAS Y PRECAUCIONES ].
Glaucoma de ángulo cerrado
Se debe advertir a los pacientes que tomar tabletas de maleato de fluvoxamina puede causar una dilatación pupilar leve, que en personas susceptibles puede provocar un episodio de glaucoma de ángulo cerrado. El glaucoma preexistente casi siempre es glaucoma de ángulo abierto porque el glaucoma de ángulo cerrado, cuando se diagnostica, se puede tratar definitivamente con iridectomía. El glaucoma de ángulo abierto no es un factor de riesgo para el glaucoma de ángulo cerrado. Es posible que los pacientes deseen ser examinados para determinar si son susceptibles al cierre angular y someterse a un procedimiento profiláctico (p. ej., iridectomía), si son susceptibles [ver ADVERTENCIAS Y PRECAUCIONES ].
Interferencia con el rendimiento cognitivo o motor
Dado que cualquier droga psicoactiva puede afectar el juicio, el pensamiento o las habilidades motoras, se debe advertir a los pacientes sobre el manejo de maquinaria peligrosa, incluidos los automóviles, hasta que estén seguros de que la terapia con tabletas de maleato de amina Fluvox 100 mg no afecta negativamente su capacidad para participar en tales actividades.
El embarazo
- Aconseje a las mujeres embarazadas que notifiquen a su proveedor de atención médica si quedan embarazadas o tienen la intención de quedar embarazadas durante el tratamiento con tabletas de maleato de fluvoxamina.
- Advierta a los pacientes que el uso de tabletas de maleato de fluvoxamina al final del embarazo puede conducir a un mayor riesgo de complicaciones neonatales que requieren hospitalización prolongada, soporte respiratorio, alimentación por sonda y/o hipertensión pulmonar persistente del recién nacido (PPHN).
- Advierta a las mujeres que existe un riesgo de recaída con la interrupción de los antidepresivos.
- Informe a las mujeres que existe un registro de exposición durante el embarazo que monitorea los resultados del embarazo en mujeres expuestas a las tabletas de maleato de fluvoxamina durante el embarazo [ver Uso en poblaciones específicas ].
Lactancia
Aconseje a las mujeres que amamantan que usan Fluvox 100 mg en tabletas de maleato de amina que vigilen a los bebés en busca de diarrea, vómitos, disminución del sueño y agitación y que busquen atención médica si notan estos signos [ver Uso en poblaciones específicas ].
Medicación concomitante
Se debe advertir a los pacientes que notifiquen a sus médicos si están tomando, o planean tomar, cualquier medicamento recetado o de venta libre, ya que existe la posibilidad de interacciones clínicamente importantes con las tabletas de maleato de amina Fluvox de 50 mg.
Se debe advertir a los pacientes sobre el uso concomitante de fluvoxamina y AINE, aspirina u otros medicamentos que afectan la coagulación, ya que el uso combinado de medicamentos psicotrópicos que interfieren con la recaptación de serotonina y estos agentes se ha asociado con un mayor riesgo de hemorragia [ver ADVERTENCIAS Y PRECAUCIONES ].
Debido a la posibilidad de un aumento del riesgo de reacciones adversas graves, incluida la disminución severa de la presión arterial y la sedación cuando se usan juntos fluvoxamina y tizanidina, no se debe usar fluvoxamina 50 mg con tizanidina [ver ADVERTENCIAS Y PRECAUCIONES ].
Debido al potencial aumento del riesgo de reacciones adversas graves cuando fluvoxamine y alosetron se usan juntos, fluvox 50mgamine no debe usarse con LotronexTM (alosetron) [ver ADVERTENCIAS Y PRECAUCIONES ].
Disfunción sexual
Advierta a los pacientes que el uso de Fluvox 50 mg en tabletas de maleato de amina puede causar síntomas de disfunción sexual tanto en pacientes masculinos como femeninos. Informe a los pacientes que deben discutir cualquier cambio en la función sexual y las posibles estrategias de manejo con su proveedor de atención médica [ver ADVERTENCIAS Y PRECAUCIONES ].
Alcohol
Al igual que con otros medicamentos psicotrópicos, se debe advertir a los pacientes que eviten el alcohol mientras toman Fluvox 50 mg comprimidos de maleato de amina.
Reacciones alérgicas
Se debe recomendar a los pacientes que notifiquen a sus médicos si desarrollan una erupción cutánea, urticaria o un fenómeno alérgico relacionado durante el tratamiento con tabletas de maleato de fluvoxamina.
Todas las marcas enumeradas son marcas comerciales registradas de sus respectivos propietarios y no son marcas comerciales de ANI Pharmaceuticals, Inc.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
Carcinogénesis
No hubo evidencia de carcinogenicidad en ratas tratadas por vía oral con maleato de fluvoxamina durante 30 meses o hámsters tratados por vía oral con maleato de 50 mg de fluvoxamina durante 20 (hembras) o 26 (machos) meses. Las dosis diarias en los grupos de dosis alta en estos estudios se aumentaron durante el transcurso del estudio desde un mínimo de 160 mg/kg hasta un máximo de 240 mg/kg en ratas, y desde un mínimo de 135 mg/kg hasta un máximo de 240 mg/kg en hámsteres. La dosis máxima de 240 mg/kg es aproximadamente 5 y 6 veces, respectivamente (en hámsteres y ratas), la MRHD administrada a niños en mg/m².
mutagénesis
No se observó evidencia de potencial genotóxico en una prueba de micronúcleo de ratón, una prueba de aberración cromosómica in vitro o la prueba de mutágeno microbiano de Ames con o sin activación metabólica.
Deterioro de la fertilidad
En un estudio en el que se administró fluvox 100 mg de amina (60, 120 o 240 mg/kg) a ratas macho y hembra antes y durante el apareamiento y la gestación, la fertilidad se vio afectada con dosis orales de 120 mg/kg (3 veces la MRHD administrada a adolescentes sobre una base de mg/m²) o más, como lo demuestra el aumento de la latencia para el apareamiento, la disminución del conteo de espermatozoides, la disminución del peso del epidídimo y la disminución de la tasa de embarazo. Además, el número de implantaciones y embriones disminuyó con la dosis más alta (6 veces la MRHD en adolescentes sobre una base de mg/m²). La dosis sin efecto para el deterioro de la fertilidad fue de 60 mg/kg (1,6 veces la MRHD administrada a adolescentes sobre una base de mg/m²).
Uso en poblaciones específicas
El embarazo
Registro de exposición durante el embarazo
Existe un registro de exposición durante el embarazo que monitorea los resultados del embarazo en mujeres expuestas a antidepresivos durante el embarazo. Se alienta a los proveedores de atención médica a registrar a los pacientes llamando al Registro Nacional de Embarazo para Antidepresivos al 1-844-405-6185 o visitando en línea https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/.
Resumen de riesgos
La experiencia prolongada con fluvox 100mgamine en mujeres embarazadas durante décadas, basada en estudios observacionales publicados, no ha identificado un riesgo claro asociado con el fármaco de defectos congénitos importantes o aborto espontáneo (ver Datos ). Existen riesgos asociados con la depresión no tratada durante el embarazo y riesgos de hipertensión pulmonar persistente del recién nacido (HPPRN) y adaptación neonatal deficiente con la exposición a los inhibidores selectivos de la recaptación de serotonina (ISRS), incluida la fluvoxamina, durante el embarazo (ver Consideraciones clínicas ).
Cuando ratas preñadas fueron tratadas por vía oral con fluvoxamina durante el período de organogénesis, se observó un aumento de la muerte embriofetal y una mayor incidencia de anomalías oculares fetales (retinas plegadas) en dosis ≥3 veces la dosis máxima recomendada en humanos (MRHD) de 300 mg/día administrada a adolescentes sobre una base de mg/m². Además, se observó una disminución del peso corporal fetal con una dosis 6 veces superior a la MRHD administrada a adolescentes sobre una base de mg/m². No hubo efectos adversos en el desarrollo en conejos tratados con fluvoxamina durante el período de organogénesis hasta una dosis de 2 veces la MRHD administrada a adolescentes sobre una base de mg/m². Cuando se administró fluvox 50 mgamine por vía oral a ratas durante el embarazo y la lactancia, se observó un aumento de la mortalidad de las crías al nacer con una dosis 2 veces superior a la MRHD administrada a los adolescentes sobre una base de mg/m². Además, se observaron disminuciones en el peso corporal de las crías y la supervivencia en dosis que son ≥0.13 veces la MRHD administrada a los adolescentes (ver Datos ).
Se desconoce el riesgo de fondo estimado de defectos congénitos importantes y aborto espontáneo para la población indicada. Todos los embarazos tienen un riesgo de fondo de defecto congénito, pérdida u otros resultados adversos. En la población general de los EE. UU., los riesgos básicos estimados de defectos congénitos importantes y aborto espontáneo en embarazos clínicamente reconocidos son del 2 al 4 % y del 15 al 20 %, respectivamente.
Consideraciones clínicas
Riesgo materno y/o embrionario/fetal asociado a la enfermedad
Las mujeres que suspenden los antidepresivos durante el embarazo tienen más probabilidades de experimentar una recaída de depresión mayor que las mujeres que continúan con los antidepresivos. Este hallazgo proviene de un estudio longitudinal prospectivo que siguió a 201 mujeres embarazadas con antecedentes de trastorno depresivo mayor que eran eutímicas y tomaban antidepresivos al comienzo del embarazo. Considere el riesgo de depresión no tratada al suspender o cambiar el tratamiento con medicamentos antidepresivos durante el embarazo y el posparto.
Reacciones adversas fetales/neonatales
Los recién nacidos expuestos a tabletas de maleato de fluvoxamina y otros ISRS o IRSN al final del tercer trimestre han desarrollado complicaciones que requieren hospitalización prolongada, soporte respiratorio y alimentación por sonda. Tales complicaciones pueden surgir inmediatamente después del parto. Los hallazgos clínicos informados incluyen dificultad respiratoria, cianosis, apnea, convulsiones, inestabilidad de la temperatura, dificultad para alimentarse, vómitos, hipoglucemia, hipotonía, hipertonía, hiperreflexia, temblor, nerviosismo, irritabilidad y llanto constante. Estas características concuerdan con un efecto tóxico directo de los ISRS y los IRSN o, posiblemente, con un síndrome de interrupción del fármaco. Cabe señalar que, en algunos casos, el cuadro clínico es compatible con el síndrome serotoninérgico [ver ADVERTENCIAS Y PRECAUCIONES ].
Datos
Datos humanos
La exposición durante la última etapa del embarazo a los ISRS puede tener un mayor riesgo de hipertensión pulmonar persistente del recién nacido (HPPRN). La HPPRN ocurre en 1 a 2 de cada 1000 nacidos vivos en la población general y se asocia con una morbilidad y mortalidad neonatal sustancial.
Datos de animales
Cuando se administraron dosis orales de fluvox 100 mgamina (60, 120 o 240 mg/kg) a ratas preñadas durante todo el período de organogénesis, se observó toxicidad del desarrollo en forma de aumento de la muerte embriofetal y aumento de la incidencia de anomalías oculares fetales (retinas plegadas) en dosis de 120 mg/kg o más (3 veces la MRHD de 300 mg/día, administrada a adolescentes sobre una base de mg/m²). Se observó una disminución del peso corporal fetal con la dosis alta de 240 mg/kg/día (6 veces la MRHD administrada a adolescentes sobre una base de mg/m²). La dosis sin efecto para la toxicidad del desarrollo en este estudio fue de 60 mg/kg/día (1,6 veces la MRHD administrada a adolescentes sobre una base de mg/m²).
En un estudio en el que a conejas preñadas se les administraron dosis de hasta 40 mg/kg (aproximadamente 2,1 veces la MRHD administrada a adolescentes en mg/m²) durante el período de organogénesis, no se observaron efectos adversos en el desarrollo embriofetal.
En otros estudios de reproducción en los que se administraron dosis orales a ratas hembra durante el embarazo y la lactancia (5, 20, 80 o 160 mg/kg), se observó un aumento de la mortalidad de las crías al nacer con dosis de 80 mg/kg/día (2 veces la MRHD administrado a adolescentes en mg/m²) o más y se observaron disminuciones en el peso corporal de las crías y la supervivencia en todas las dosis (dosis de efecto bajo aproximadamente 0,13 veces la MRHD administrada a adolescentes en mg/m²).
Lactancia
Los datos de la literatura publicada informan la presencia de fluvoxamina en la leche humana (ver Datos ). No se han informado efectos adversos en el lactante en la mayoría de los casos de uso materno de fluvox 50 mgamine durante la lactancia. Sin embargo, hay informes de diarrea, vómitos, disminución del sueño y agitación (ver Consideraciones clínicas ). No hay datos sobre el efecto de fluvox 100mgamine en la producción de leche. Los beneficios para el desarrollo y la salud de la lactancia materna deben considerarse junto con la necesidad clínica de fluvoxamina de 50 mg de la madre y cualquier efecto adverso potencial en el niño amamantado debido a la fluvoxamina oa la afección materna subyacente.
Consideraciones clínicas
Controle a los bebés expuestos a la fluvoxamina a través de la leche materna para detectar diarrea, vómitos, disminución del sueño y agitación.
Datos
Se observaron concentraciones de fármaco en la leche ≤ 425 ng/mL después de la dosificación materna de fluvox 100 mgamine de 25 mg/día a 300 mg/día en informes de casos y series de casos publicados.
Hembras y machos con potencial reproductivo
Esterilidad
Los hallazgos en animales sugieren que la fertilidad puede verse afectada mientras se toma fluvox 50 mgamine [ver Toxicología no clínica ].
Uso pediátrico
La eficacia de fluvox 100 mg de maleato de amina para el tratamiento del trastorno obsesivo compulsivo se demostró en un estudio multicéntrico controlado con placebo de 10 semanas con 120 pacientes ambulatorios de 8 a 17 años. Además, 99 de estos pacientes ambulatorios continuaron el tratamiento abierto con maleato de fluvoxamina durante uno a tres años más, lo que equivale a 94 años-paciente. El perfil de eventos adversos observado en ese estudio fue generalmente similar al observado en estudios de adultos con fluvoxamina [ver REACCIONES ADVERSAS , DOSIFICACIÓN Y ADMINISTRACIÓN ].
Se ha observado disminución del apetito y pérdida de peso en asociación con el uso de fluvoxamina y otros ISRS. En consecuencia, se recomienda un control regular del peso y el crecimiento si se va a continuar el tratamiento de un niño con un ISRS a largo plazo.
Los riesgos, si los hubiera, que pueden estar asociados con el uso prolongado de fluvox 50 mgamine en niños y adolescentes con TOC no se han evaluado sistemáticamente. El prescriptor debe tener en cuenta que la evidencia en la que se basa para concluir que la fluvoxamina es segura para su uso en niños y adolescentes se deriva de estudios clínicos a corto plazo y de la extrapolación de la experiencia adquirida con pacientes adultos. En particular, no hay estudios que evalúen directamente los efectos del uso prolongado de fluvoxamina en el crecimiento, el desarrollo cognitivo conductual y la maduración de niños y adolescentes. Aunque no hay un hallazgo afirmativo que sugiera que la fluvoxamina posee la capacidad de afectar negativamente el crecimiento, el desarrollo o la maduración, la ausencia de tales hallazgos no es una evidencia convincente de la ausencia del potencial de la fluvoxamina para tener efectos adversos en el uso crónico [ver ADVERTENCIAS Y PRECAUCIONES ].
No se ha establecido la seguridad y la eficacia en la población pediátrica distinta de los pacientes pediátricos con TOC [ver ADVERTENCIA EN CAJA ; ADVERTENCIAS Y PRECAUCIONES ]. Cualquier persona que esté considerando el uso de tabletas de maleato de amina de 100 mg de Fluvox en un niño o adolescente debe sopesar los riesgos potenciales con la necesidad clínica.
Uso geriátrico
Aproximadamente 230 pacientes que participaron en estudios controlados previos a la comercialización con tabletas de maleato de fluvoxamina tenían 65 años de edad o más. No se observaron diferencias generales en la seguridad entre estos pacientes y los pacientes más jóvenes. Otra experiencia clínica informada no ha identificado diferencias en la respuesta entre los pacientes de edad avanzada y los más jóvenes. Sin embargo, los ISRS y los IRSN, incluidos los comprimidos de maleato de fluvoxamina, se han asociado con varios casos de hiponatremia clínicamente significativa en pacientes de edad avanzada, que pueden tener un mayor riesgo de este evento adverso [ver ADVERTENCIAS Y PRECAUCIONES ]. Además, el aclaramiento de fluvoxamina se reduce en aproximadamente un 50 % en pacientes de edad avanzada en comparación con pacientes más jóvenes [ver FARMACOLOGÍA CLÍNICA ], y tampoco se puede descartar una mayor sensibilidad de algunos individuos mayores. En consecuencia, se debe considerar una dosis inicial más baja en pacientes de edad avanzada y las tabletas de maleato de amina de 50 mg de Fluvox se deben titular lentamente durante el inicio de la terapia.
SOBREDOSIS
Se ha informado lo siguiente con sobredosis de tabletas de fluvox 100mgamine:
- Convulsiones, que pueden ser tardías, y alteración del estado mental, incluido el coma.
- Toxicidad cardiovascular, que puede ser tardía, incluida la prolongación del intervalo QRS y QTc. La hipertensión se ve con mayor frecuencia, pero rara vez se puede ver hipotensión sola o con la ingesta concomitante, incluido el alcohol.
- Síndrome serotoninérgico (los pacientes con una sobredosis de múltiples fármacos con otros fármacos proserotoninérgicos pueden tener un mayor riesgo).
Se debe considerar la descontaminación gastrointestinal con carbón activado en pacientes que se presentan inmediatamente después de una sobredosis de fluvoxamina.
Considere comunicarse con un centro de envenenamiento (1-800-221-2222) o un médico toxicólogo para recomendaciones de manejo de sobredosis.
CONTRAINDICACIONES
coadministración
Está contraindicada la coadministración de tizanidina, tioridazina, alosetrón o pimozida con Fluvox 50mgamine Maleate Tablets [ver ADVERTENCIAS Y PRECAUCIONES ].
Síndrome serotoninérgico e inhibidores de la monoaminooxidasa (IMAO)
El uso de IMAO destinados a tratar trastornos psiquiátricos con tabletas de maleato de fluvoxamina o dentro de los 14 días posteriores a la interrupción del tratamiento con tabletas de maleato de fluvoxamina está contraindicado debido a un mayor riesgo de síndrome serotoninérgico. También está contraindicado el uso de Fluvox 50 mg comprimidos de maleato de amina dentro de los 14 días posteriores a la suspensión de un IMAO destinado a tratar trastornos psiquiátricos [ver DOSIFICACIÓN Y ADMINISTRACIÓN , ADVERTENCIAS Y PRECAUCIONES ].
También está contraindicado iniciar Fluvoxamine Maleate Tablets en un paciente que está siendo tratado con IMAO como linezolid o azul de metileno intravenoso debido a un mayor riesgo de síndrome serotoninérgico [ver DOSIFICACIÓN Y ADMINISTRACIÓN , ADVERTENCIAS Y PRECAUCIONES ].
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
Se presume que el mecanismo de acción de fluvox 50mgamine maleate en el trastorno obsesivo compulsivo está relacionado con su inhibición específica de la recaptación de serotonina en las neuronas cerebrales. Se ha demostrado que Fluvox 100mgamine es un potente inhibidor del transportador de recaptación de serotonina en estudios preclínicos, tanto in vitro como in vivo.
Farmacodinámica
En estudios in vitro, fluvox 100 mg de maleato de amina no tuvo una afinidad significativa por los receptores histaminérgicos, alfa o beta adrenérgicos, muscarínicos o dopaminérgicos. Se cree que el antagonismo de algunos de estos receptores está asociado con varios efectos sedantes, cardiovasculares, anticolinérgicos y extrapiramidales de algunos fármacos psicotrópicos.
Farmacocinética
Absorción
La biodisponibilidad absoluta del maleato de fluvoxamina es del 53%. La biodisponibilidad oral no se ve significativamente afectada por los alimentos.
En un estudio de proporcionalidad de dosis que involucró maleato de fluvoxamina a 100, 200 y 300 mg/día durante 10 días consecutivos en 30 voluntarios normales, se logró el estado estacionario después de aproximadamente una semana de dosificación. Las concentraciones plasmáticas máximas en el estado estacionario ocurrieron dentro de las 3 a 8 horas posteriores a la dosificación y alcanzaron concentraciones promedio de 88, 283 y 546 ng/mL, respectivamente. Por lo tanto, la fluvoxamina tuvo una farmacocinética no lineal en este rango de dosis, es decir, las dosis más altas de maleato de amina de 100 mg de fluvox produjeron concentraciones desproporcionadamente más altas que las previstas a partir de la dosis más baja.
Distribución
El volumen de distribución aparente medio de la fluvoxamina es de aproximadamente 25 l/kg, lo que sugiere una amplia distribución tisular.
Aproximadamente el 80 % de fluvox 100 mgamine se une a las proteínas plasmáticas, principalmente a la albúmina, en un rango de concentración de 20 a 2000 ng/mL.
Metabolismo
El maleato de amina Fluvox 100 mg se metaboliza extensamente en el hígado; las principales rutas metabólicas son la desmetilación oxidativa y la desaminación. Se identificaron nueve metabolitos después de una dosis radiomarcada de 5 mg de fluvox 100 mg de maleato de amina, que constituyen aproximadamente el 85 % de los productos de excreción urinaria de fluvox de 100 mg. El principal metabolito humano fue fluvox 100 mg de ácido amina que, junto con su análogo N-acetilado, representó alrededor del 60 % de los productos de excreción urinaria. Un tercer metabolito, fluvoxetanol, formado por desaminación oxidativa, representó alrededor del 10%. Fluvox 100 mg de ácido amina y fluvox 100 mg de etanol se probaron en un ensayo in vitro de inhibición de la recaptación de serotonina y norepinefrina en ratas; estaban inactivos excepto por un efecto débil del metabolito anterior sobre la inhibición de la captación de serotonina (1-2 órdenes de magnitud menos potentes que el compuesto original). Aproximadamente el 2 % de fluvox 100 mgamine se excretó en la orina sin cambios [ver INTERACCIONES CON LA DROGAS ].
Eliminación
Después de una dosis oral marcada con 14C de fluvox 50 mg de maleato de amina (5 mg), se recuperó en la orina un promedio del 94 % de los productos relacionados con el fármaco en 71 horas.
La semivida plasmática media de fluvox 100 mgamina en estado estacionario después de múltiples dosis orales de 100 mg/día en voluntarios jóvenes y sanos fue de 15,6 horas.
Sujetos de edad avanzada
En un estudio de tabletas de maleato de fluvoxamina a 50 y 100 mg en el que se compararon sujetos de edad avanzada (de 66 a 73 años) y sujetos jóvenes (de 19 a 35 años), las concentraciones plasmáticas máximas medias en los ancianos fueron un 40 % más altas. La vida media de eliminación de dosis múltiples de fluvox 50 mgamina fue de 17,4 y 25,9 horas en los ancianos en comparación con 13,6 y 15,6 horas en los sujetos jóvenes en estado estacionario para dosis de 50 y 100 mg, respectivamente. En pacientes de edad avanzada, el aclaramiento de fluvox 100 mgamine se redujo en aproximadamente un 50 % y, por lo tanto, los comprimidos de maleato de fluvox 100 mgamine deben titularse lentamente durante el inicio de la terapia [ver DOSIFICACIÓN Y ADMINISTRACIÓN ].
Sujetos pediátricos
La farmacocinética de dosis múltiples de fluvox 50 mgamina se determinó en niños y niñas (de 6 a 11 años) y adolescentes (de 12 a 17 años). Las concentraciones plasmáticas de 100 mg de fluvox en estado estacionario fueron 2-3 veces más altas en niños que en adolescentes. El AUC y la Cmax en niños fueron de 1,5 a 2,7 veces mayores que en adolescentes. (Consulte la Tabla 4). Al igual que en los adultos, tanto los niños como los adolescentes exhibieron una farmacocinética no lineal de dosis múltiples. Las niñas mostraron un AUC (0-12) y una Cmax significativamente mayores en comparación con los niños varones y, por lo tanto, las dosis más bajas de tabletas de maleato de fluvoxamina pueden producir un beneficio terapéutico. (Ver Tabla 5). No se observaron diferencias de género en los adolescentes. Las concentraciones plasmáticas de fluvoxamina en estado estacionario fueron similares en adultos y adolescentes a una dosis de 300 mg/día, lo que indica que la exposición a fluvoxamina de 100 mg fue similar en estas dos poblaciones. (Consulte la Tabla 4). Puede estar indicado el ajuste de la dosis en adolescentes (hasta la dosis máxima para adultos de 300 mg) para lograr un beneficio terapéutico [consulte DOSIFICACIÓN Y ADMINISTRACIÓN ].
TABLA 4: COMPARACIÓN DE LOS PARÁMETROS FARMACOCINÉTICOS MEDIOS (DE) DE FLUVOX 50 mg DE AMINA ENTRE NIÑOS, ADOLESCENTES Y ADULTOS
TABLA 5: COMPARACIÓN DE LOS PARÁMETROS FARMACOCINÉTICOS MEDIOS (DE) DE FLUVOX 50 mg AMINE ENTRE NIÑOS Y NIÑAS (6-11 AÑOS)
Enfermedad hepática y renal
Una comparación de estudios cruzados (sujetos sanos versus pacientes con disfunción hepática) sugirió una disminución del 30 % en el aclaramiento de amina de fluvox 50 mg en asociación con la disfunción hepática. Las concentraciones plasmáticas mínimas medias en pacientes con insuficiencia renal (aclaramiento de creatinina de 5 a 45 ml/min) después de 4 y 6 semanas de tratamiento (50 mg bid, N=13) fueron comparables entre sí, lo que sugiere que no hay acumulación de fluvoxamina en estos pacientes. [ver ADVERTENCIAS Y PRECAUCIONES ].
Estudios clínicos
Estudios de TOC en adultos
La eficacia de las tabletas de maleato de fluvoxamina para el tratamiento del trastorno obsesivo compulsivo (TOC) se demostró en dos estudios multicéntricos de grupos paralelos de 10 semanas de duración en pacientes adultos ambulatorios. Los pacientes en estos ensayos fueron dosificados a una dosis diaria total de fluvox 50 mg de maleato de amina de 150 mg/día durante las primeras dos semanas del ensayo, luego de lo cual la dosis se ajustó dentro de un rango de 100-300 mg/día (en un programa de oferta) , sobre la base de la respuesta y la tolerancia. Los pacientes de estos estudios tenían TOC de moderado a grave (DSM-III-R), con puntuaciones iniciales medias en la escala obsesivo-compulsiva de Yale-Brown (Y-BOCS), puntuación total de 23. Los pacientes que recibieron fluvox 50 mg de maleato de amina experimentaron reducciones medias de aproximadamente 4 a 5 unidades en la puntuación total de Y-BOCS, en comparación con una reducción de 2 unidades para los pacientes que recibieron placebo.
La Tabla 6 proporciona la clasificación de resultados por grupo de tratamiento en el ítem de Mejoría Global de la escala de Impresiones Clínicas Globales (CGI) para ambos estudios combinados.
TABLA 6: CLASIFICACIÓN DE RESULTADOS (%) EN CGI-ÍTEM DE MEJORA GLOBAL PARA LOS TERMINADORES EN EL GRUPO DE DOS ESTUDIOS DE TOC EN ADULTOS
Los análisis exploratorios de los efectos de la edad y el género en los resultados no sugirieron ninguna respuesta diferencial en función de la edad o el sexo.
Estudio de mantenimiento del TOC en adultos
En un ensayo de mantenimiento de pacientes adultos ambulatorios con TOC, 114 pacientes que cumplían con los criterios del DSM-IV para el TOC y con una puntuación de la Escala Obsesivo-Compulsiva de Yale-Brown (Y-BOCS) ≥18 se ajustaron a una dosis efectiva de comprimidos de maleato de fluvoxamina de 100 a 300 mg /día como parte de una fase inicial de tratamiento simple ciego de 10 semanas. La respuesta al tratamiento durante esta fase simple ciego se definió como puntajes de Y-BOCS al menos un 30 % más bajos que el valor inicial al final de las semanas 8 y 10. De los pacientes que respondieron, la duración promedio de la respuesta fue de 4 semanas. Los pacientes que respondieron durante esta fase inicial fueron aleatorizados para continuar con las tabletas de maleato de amina de 50 mg de Fluvox (N=56) o con el placebo (N=58) en una fase doble ciego para observar la recaída. La recaída durante la fase doble ciego se definió como un aumento en la puntuación Y-BOCS de al menos un 30 % sobre el valor inicial de esa fase o la negativa del paciente a continuar con el tratamiento debido a un aumento sustancial de los síntomas del TOC. En la fase doble ciego, los pacientes que recibieron tratamiento continuo con tabletas de maleato de fluvoxamina experimentaron, en promedio, una tasa de recaída significativamente menor que aquellos que recibieron placebo.
Un examen de los subgrupos de población de este ensayo no reveló ninguna evidencia clara de un efecto de mantenimiento diferencial sobre la base de la edad o el sexo.
Estudio de TOC pediátrico
La eficacia de las tabletas de maleato de fluvoxamina para el tratamiento del TOC también se demostró en un estudio multicéntrico de grupos paralelos de 10 semanas en una población de pacientes ambulatorios pediátricos (niños y adolescentes, de 8 a 17 años). Los pacientes de este estudio recibieron una dosis diaria total de fluvox de 100 mg de amina de aproximadamente 100 mg/día durante las dos primeras semanas del ensayo, luego de lo cual la dosis se ajustó dentro de un rango de 50 a 200 mg/día (en un programa de oferta) sobre la base de la respuesta y la tolerancia. Todos los pacientes tenían TOC de moderado a grave (DSM-III-R) con puntuaciones iniciales medias en la escala obsesiva compulsiva de Yale-Brown para niños (CY-BOCS) con una puntuación total de 24. Los pacientes que recibieron fluvox 100 mg de maleato de amina experimentaron reducciones medias de aproximadamente seis unidades en la puntuación total de CY-BOCS, en comparación con una reducción de tres unidades para los pacientes que recibieron placebo.
La Tabla 7 proporciona la clasificación de resultados por grupo de tratamiento en el ítem de Mejoría Global de la escala de Impresión Clínica Global (CGI) para el estudio pediátrico.
TABLA 7: CLASIFICACIÓN DE RESULTADOS (%) EN CGI-ÍTEM DE MEJORA GLOBAL PARA TERMINADORES EN ESTUDIO PEDIÁTRICO
Los análisis exploratorios post hoc de los efectos del género en los resultados no sugirieron ninguna sensibilidad diferencial sobre la base del género. Análisis exploratorios adicionales revelaron un efecto de tratamiento prominente en el grupo de edad de 8 a 11 años y esencialmente ningún efecto en el grupo de edad de 12 a 17 años. Si bien la importancia de estos resultados no está clara, las concentraciones plasmáticas de fluvoxamina en estado estacionario de 2 a 3 veces más altas en niños en comparación con los adolescentes [ver FARMACOLOGÍA CLÍNICA ] sugiere que la disminución de la exposición en adolescentes puede haber sido un factor, y el ajuste de la dosis en adolescentes (hasta la dosis máxima para adultos de 300 mg) puede estar indicado para lograr un beneficio terapéutico.
INFORMACIÓN DEL PACIENTE
Fluvox 100mgamina (Flu VOX ah meen) Tabletas de maleato
Lea la Guía del medicamento que viene con las tabletas de maleato de amina Fluvox de 100 mg antes de comenzar a tomarlas y cada vez que renueve su receta. Es posible que haya nueva información. Esta Guía del medicamento no reemplaza la conversación con su proveedor de atención médica sobre su condición médica o tratamiento. Hable con su proveedor de atención médica si hay algo que no entiende o sobre lo que desea obtener más información.
¿Cuál es la información más importante que debo saber sobre Fluvox 50mgamine Maleate Tablets?
La fluvoxamina es el mismo tipo de medicamento que se usa para tratar la depresión y puede causar efectos secundarios graves, que incluyen:
1. Pensamientos o acciones suicidas:
- Las tabletas de maleato de fluvoxamina y los medicamentos antidepresivos pueden aumentar los pensamientos o acciones suicidas. en algunos niños, adolescentes o adultos jóvenes dentro de los primeros meses de tratamiento o cuando se cambia la dosis.
- La depresión u otras enfermedades mentales graves son las causas más importantes de pensamientos o acciones suicidas.
- Esté atento a estos cambios y llame a su proveedor de atención médica de inmediato si nota:
- Cambios nuevos o repentinos en el estado de ánimo, el comportamiento, las acciones, los pensamientos o los sentimientos, especialmente si son graves.
- Preste especial atención a tales cambios cuando se inicia Fluvox 100mgamine Maleate Tablets o cuando se cambia la dosis.
Mantenga todas las visitas de seguimiento con su proveedor de atención médica y llame entre visitas si le preocupan los síntomas.
Llame a su proveedor de atención médica de inmediato si tiene alguno de los siguientes síntomas, o llame al 911 en caso de emergencia, especialmente si son nuevos, empeoran o le preocupan:
- intentos de suicidio
- actuando sobre impulsos peligrosos
- actuando agresivo o violento
- pensamientos sobre el suicidio o la muerte
- depresión nueva o peor
- nuevos o peores ataques de ansiedad o pánico
- sentirse agitado, inquieto, enojado o irritable
- problemas para dormir
- un aumento en la actividad o hablar más de lo normal para usted
- otros cambios inusuales en el comportamiento o el estado de ánimo
Informe a su proveedor de atención médica de inmediato si tiene alguno de los siguientes síntomas o llame al 911 en caso de emergencia. Las tabletas de maleato de fluvoxamina pueden estar asociadas con estos efectos secundarios graves:
2. Síndrome de serotonina: esta afección puede poner en peligro la vida y puede incluir:
- agitación, alucinaciones, coma u otros cambios en el estado mental
- problemas de coordinación o espasmos musculares (reflejos hiperactivos)
- latidos cardíacos acelerados, presión arterial alta o baja
- sudoración o fiebre
- náuseas, vómitos o diarrea
- rigidez muscular
3. Problemas visuales
- dolor de ojo
- cambios en la visión
- hinchazón o enrojecimiento en o alrededor del ojo
Solo algunas personas corren el riesgo de tener estos problemas. Es posible que desee someterse a un examen de la vista para ver si está en riesgo y recibir tratamiento preventivo si lo está.
4. Reacciones alérgicas graves:
- dificultad para respirar
- hinchazón de la cara, la lengua, los ojos o la boca
- sarpullido, ronchas que pican (urticaria) o ampollas, solo o con fiebre o dolor en las articulaciones
5. Sangrado anormal: Las tabletas de maleato de amina de 100 mg de Fluvox y los medicamentos antidepresivos pueden aumentar su riesgo de sangrado o moretones, especialmente si toma warfarina, un anticoagulante (Coumadin®, Jantoven®), o un medicamento antiinflamatorio no esteroideo (AINE, como ibuprofeno, naproxeno o aspirina).
6. Ataques o convulsiones
7. Episodios maníacos:
- gran aumento de energía
- problemas severos para dormir
- pensamientos acelerados
- comportamiento temerario
- ideas inusualmente grandiosas
- felicidad excesiva o irritabilidad
- hablando más o más rápido de lo habitual
8. Cambios en el apetito o el peso. A los niños y adolescentes se les debe controlar la altura y el peso durante el tratamiento.
9. Niveles bajos de sal (sodio) en la sangre. Las personas mayores pueden estar en mayor riesgo de esto. Los síntomas pueden incluir:
- dolor de cabeza
- debilidad o sensación de inestabilidad
- confusión, problemas para concentrarse o pensar o problemas de memoria
10. Problemas sexuales (disfunción). Tomar inhibidores selectivos de la recaptación de serotonina (ISRS), incluidas las tabletas de maleato de amina Fluvox de 50 mg, puede causar problemas sexuales.
- Los síntomas en los hombres pueden incluir:
- Eyaculación retardada o incapacidad para tener una eyaculación
- Disminución del deseo sexual
- Problemas para conseguir o mantener una erección
- Los síntomas en las mujeres pueden incluir:
- Disminución del deseo sexual
- Orgasmo retrasado o incapacidad para tener un orgasmo
Hable con su proveedor de atención médica si desarrolla algún cambio en su función sexual o si tiene alguna pregunta o inquietud sobre problemas sexuales durante el tratamiento con Fluvox 50mgamine Maleate Tablets. Puede haber tratamientos que su proveedor de atención médica pueda sugerir.
No suspenda las tabletas de maleato de fluvoxamina sin antes hablar con su proveedor de atención médica.
Suspender las tabletas de maleato de fluvoxamina demasiado rápido puede causar síntomas graves que incluyen:
- ansiedad, irritabilidad, estado de ánimo alto o bajo, sensación de inquietud o cambios en los hábitos de sueño
- dolor de cabeza, sudoración, náuseas, mareos
- sensaciones de descarga eléctrica, temblores, confusión
¿Qué son las tabletas de maleato de fluvoxamina?
Las tabletas de maleato de fluvoxamina son un medicamento recetado que se usa para tratar el trastorno obsesivo compulsivo (TOC). Es importante hablar con su proveedor de atención médica sobre los riesgos de tratar el TOC y también sobre los riesgos de no tratarlo. Debe analizar todas las opciones de tratamiento con su proveedor de atención médica.
Hable con su proveedor de atención médica si no cree que su condición esté mejorando con el tratamiento con Fluvox 100mgamine Maleate Tablets.
¿Quién no debe tomar Fluvox 100 mg comprimidos de maleato de amina?
No tome tabletas de maleato de fluvoxamina si usted:
- es alérgico al maleato de amina de 50 mg de fluvox o a cualquiera de los ingredientes de las tabletas de maleato de fluvoxamina. Consulte el final de esta Guía del medicamento para obtener una lista completa de los ingredientes de las tabletas de maleato de amina Fluvox de 50 mg.
- tomar un inhibidor de la monoaminooxidasa (IMAO). Pregúntele a su proveedor de atención médica o farmacéutico si no está seguro si está tomando un IMAO, incluido el antibiótico linezolid.
- No tome un IMAO dentro de las 2 semanas posteriores a la suspensión de las tabletas de maleato de fluvoxamina a menos que su médico se lo indique.
- No comience a tomar Fluvox 50mgamine Maleate Tablets si dejó de tomar un IMAO en las últimas 2 semanas, a menos que su médico se lo indique.
Las personas que toman tabletas de maleato de fluvoxamina cerca de un IMAO pueden tener efectos secundarios graves o incluso potencialmente mortales. Obtenga ayuda médica de inmediato si tiene alguno de estos síntomas:
-
- fiebre alta
- espasmos musculares incontrolables
- músculos rígidos
- cambios rápidos en la frecuencia cardíaca o la presión arterial
- confusión
- pérdida del conocimiento (desmayo)
- tome Mellaril® (tioridazina). No tome Mellaril® dentro de las 2 semanas posteriores a la suspensión de las tabletas de maleato de amina de 50 mg de Fluvox porque esto puede causar problemas graves del ritmo cardíaco o muerte súbita.
- tome Orap® (pimozida) porque tomar este medicamento con Fluvox 50mgamine Maleate Tablets puede causar problemas graves del ritmo cardíaco o muerte súbita.
- tome Zanaflex® (tizanidina). Las tabletas de maleato de fluvoxamina podrían aumentar la cantidad de Zanaflex en su cuerpo, lo que podría aumentar sus acciones y efectos secundarios. Esto podría incluir somnolencia y una caída en la presión arterial y afectar qué tan bien hace las cosas que requieren estar alerta.
- Tome Lotronex® (alosetrón). Las tabletas de maleato de amina Fluvox 50 mg pueden aumentar la cantidad de Lotronex en su cuerpo, lo que podría aumentar sus acciones y efectos secundarios.
¿Qué debo decirle a mi proveedor de atención médica antes de tomar tabletas de maleato de amina Fluvox de 50 mg? Pregunte si no está seguro.
Antes de comenzar a tomar tabletas de maleato de fluvoxamina, informe a su proveedor de atención médica si usted:
- Están tomando ciertos medicamentos como:
- Inhibidores de la monoaminooxidasa (IMAO) como Emsam® (selegilina), Nardil® (fenelzina) o Parnate® (tranilcipromina)
- Mellaril® (tioridazina): se usa para tratar problemas mentales o del estado de ánimo
- Zanaflex® (tizanidina): se usa para tratar la espasticidad (una afección en la que los músculos se tensan y se contraen)
- Orap® (pimozida): se usa para tratar el síndrome de Tourette (una afección cerebral que causa tics)
- Lotronex® (alosetrón): se usa para tratar una afección con diarrea, dolor de estómago continuo, calambres e hinchazón
- Triptanos: utilizados para tratar la migraña
- Medicamentos utilizados para tratar el estado de ánimo, la ansiedad, los trastornos psicóticos o del pensamiento, incluidos los tricíclicos, el litio, los ISRS, los IRSN o los antipsicóticos
- Tramadol: utilizado para reducir el dolor.
- Benzodiazepinas: utilizadas para reducir la ansiedad, el estrés, el malestar emocional o las convulsiones; te ayuda a dormir; ayuda con la abstinencia de alcohol; reduce la inquietud; y relaja los músculos
- Metadona: se usa para aliviar el dolor o ayudar con la adicción
- Clozapina: se utiliza para tratar trastornos mentales
- Mexiletina: se utiliza para tratar anomalías en el ritmo cardíaco
- Teofilina: se usa para tratar la inflamación de las vías respiratorias en los pulmones, para relajar los músculos del pecho y aliviar la dificultad para respirar, a menudo para tratar el asma
- Warfarina y otros medicamentos que afectan la coagulación de la sangre
- Diuréticos para tratar la presión arterial alta, la insuficiencia cardíaca congestiva o la hinchazón
- Suplementos de venta libre como triptófano o hierba de San Juan
- tiene problemas hepáticos
- tiene problemas renales
- tener problemas del corazón
- tiene o ha tenido ataques o convulsiones
- tiene trastorno bipolar o manía
- tiene niveles bajos de sodio en la sangre
- tiene antecedentes de un derrame cerebral
- tiene presión arterial alta
- tiene o ha tenido problemas de sangrado
- está embarazada o planea quedar embarazada. Hable con su proveedor de atención médica sobre el riesgo para su bebé por nacer si toma tabletas de maleato de amina Fluvox de 50 mg.
- Hable con su proveedor de atención médica sobre los beneficios y riesgos de tratar el TOC durante el embarazo.
- Si queda embarazada durante el tratamiento con tabletas de maleato de amina de 50 mg de Fluvox, hable con su proveedor de atención médica acerca de registrarse en el Registro Nacional de Embarazo para Antidepresivos. Puede registrarse llamando al 1-844-405-6185.
- está amamantando o planea amamantar. Las tabletas de maleato de fluvoxamina pasan a la leche materna. Hable con su proveedor de atención médica acerca de la mejor manera de alimentar a su bebé mientras toma tabletas de maleato de amina Fluvox de 50 mg.
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluyendo medicamentos recetados y de venta libre, vitaminas y suplementos herbales. Las tabletas de maleato de fluvoxamina y algunos medicamentos pueden interactuar entre sí, pueden no funcionar tan bien o pueden causar efectos secundarios graves.
Su proveedor de atención médica o farmacéutico puede decirle si es seguro tomar tabletas de maleato de fluvoxamina con sus otros medicamentos. No comience ni suspenda ningún medicamento mientras toma tabletas de maleato de fluvoxamina sin hablar primero con su proveedor de atención médica.
Si toma Fluvox 100mgamine Maleate Tablets, no debe tomar ningún otro medicamento que contenga fluvoxamina, incluidos: LUVOX 50mg CR®
¿Cómo debo tomar tabletas de maleato de fluvoxamina?
- Tome las tabletas de maleato de fluvoxamina exactamente según lo recetado. Es posible que su proveedor de atención médica deba cambiar la dosis de tabletas de maleato de amina Fluvox de 100 mg hasta que sea la dosis adecuada para usted.
- Las tabletas de maleato de amina de 100 mg de Fluvox se pueden tomar con o sin alimentos.
- Si olvida una dosis de tabletas de maleato de fluvoxamina, tome la dosis olvidada tan pronto como lo recuerde. Si es casi la hora de la próxima dosis, omita la dosis olvidada y tome la siguiente dosis a la hora habitual. No tome dos dosis de Fluvox 100mgamine Maleate Tablets al mismo tiempo.
- Si toma demasiadas tabletas de maleato de amina Fluvox de 50 mg, llame a su proveedor de atención médica o al centro de control de intoxicaciones de inmediato, o busque tratamiento de emergencia.
¿Qué debo evitar mientras tomo fluvox 50mgamine maleate tablets?
Las tabletas de maleato de amina de 100 mg de Fluvox pueden causar somnolencia o pueden afectar su capacidad para tomar decisiones, pensar con claridad o reaccionar rápidamente. No debe conducir, operar maquinaria pesada ni realizar otras actividades peligrosas hasta que sepa cómo le afecta el maleato de fluvoxamina. No beba alcohol mientras usa las tabletas de maleato de fluvoxamina.
¿Cuáles son los posibles efectos secundarios de las tabletas de maleato de amina Fluvox de 100 mg?
- Las tabletas de maleato de fluvoxamina pueden causar efectos secundarios graves, que incluyen:
- Consulte "¿Cuál es la información más importante que debo saber sobre las tabletas de maleato de amina Fluvox de 100 mg?"
Sensación de ansiedad o dificultad para dormir
Los posibles efectos secundarios comunes en personas que toman Fluvox 100mgamine Maleate Tablets incluyen:
- náuseas
- somnolencia
- debilidad
- indigestión
- transpiración
- pérdida de apetito
- sacudida
- vómitos
- eyaculación retardada
- incapacidad para tener un orgasmo
- disminución del deseo sexual
- boca seca
- congestión nasal
- sabor inusual
- micción frecuente
Otros efectos secundarios en niños y adolescentes incluyen:
- agitación o aumento anormal de la actividad
- sentirse deprimido o triste
- gas excesivo
- periodos menstruales abundantes
- sarpullido
- posible tasa de crecimiento más lenta y cambio de peso.
Informe a su proveedor de atención médica si tiene algún efecto secundario que le moleste o que no desaparezca. Estos no son todos los posibles efectos secundarios de Fluvox 50mgamine Maleate Tablets. Para obtener más información, consulte a su proveedor de atención médica o farmacéutico.
LLAME A SU MÉDICO PARA OBTENER CONSEJOS MÉDICOS SOBRE LOS EFECTOS SECUNDARIOS. PUEDE INFORMAR EFECTOS SECUNDARIOS al 1-800-308-6755 o a la FDA al 1-800-FDA-1088
¿Cómo debo almacenar las tabletas de maleato de amina Fluvox 50mg?
Guarde las tabletas de maleato de fluvoxamina a temperatura ambiente entre 59 °F y 86 °F (15 °C y 30 °C).
- Mantenga las tabletas de maleato de fluvoxamina lejos de la humedad alta.
- Mantenga el frasco de tabletas de maleato de fluvoxamina bien cerrado.
Mantenga las tabletas de maleato de fluvoxamina y todos los medicamentos fuera del alcance de los niños.
Información general sobre las tabletas de maleato de amina Fluvox 100mg
A veces, los medicamentos se recetan para fines distintos a los enumerados en la Guía del medicamento. No use las tabletas de maleato de fluvoxamina para una condición para la cual no fue recetado. No le dé Fluvox 100mgamine Maleate Tablets a otras personas, incluso si tienen la misma condición. Puede que les haga daño.
Esta Guía del medicamento resume la información más importante sobre las tabletas de maleato de fluvoxamina. Si desea obtener más información, hable con su proveedor de atención médica. Puede pedirle a su proveedor de atención médica o farmacéutico información sobre las tabletas de maleato de fluvoxamina que está escrita para profesionales de la salud.
Para obtener más información acerca de las tabletas de maleato de amina Fluvox de 50 mg, llame sin cargo al 1-800-308-6755 o visite www.anipharmaceuticals.com.
¿Cuáles son los ingredientes de las tabletas de maleato de fluvoxamina?
Principio activo: maleato de fluvoxamina
Ingredientes inactivos:
Las tabletas de 25 mg: cera de carnauba, hipromelosa, manitol, polietilenglicol, polisorbato 80, almidón pregelatinizado (papa), dióxido de silicio, estearilfumarato de sodio, almidón (maíz) y dióxido de titanio.
Las tabletas de 50 mg y 100 mg: Además de los ingredientes inactivos anteriores, contienen óxidos de hierro sintéticos.
Esta Guía del medicamento ha sido aprobada por la Administración de Alimentos y Medicamentos de EE. UU.
