Amoxil 250mg, 500mg, 625mg, 1000mg Amoxicillin Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es la amoxicilina y cómo se usa?
¿Qué es Amoxil 1000mg?
Amoxil es un medicamento recetado que se usa para tratar los síntomas de muchos tipos diferentes de infecciones bacterianas, como amigdalitis, bronquitis, neumonía e infecciones del oído, la nariz, la garganta, la piel o el tracto urinario. Amoxil 1000mg puede usarse solo o con otros medicamentos.
Amoxil pertenece a una clase de medicamentos llamados Penicilinas, Amino.
¿Cuáles son los posibles efectos secundarios de Amoxil?
Amoxil puede causar efectos secundarios graves que incluyen:
- urticaria,
- respiración dificultosa,
- hinchazón de la cara, los labios, la lengua o la garganta,
- fiebre,
- dolor de garganta,
- ojos irritados,
- dolor de piel,
- erupción cutánea roja o morada con ampollas y descamación,
- dolor de estómago intenso y
- diarrea acuosa o con sangre (incluso si ocurre meses después de su última dosis)
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Amoxil incluyen:
- náuseas,
- vómitos,
- diarrea, y
- sarpullido
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Amoxil. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
DESCRIPCIÓN
Las formulaciones de AMOXIL contienen amoxicilina, un antibiótico semisintético, un análogo de la ampicilina, con un amplio espectro de actividad bactericida contra muchos microorganismos Gram-positivos y Gram-negativos. Químicamente, es (2S,5,R,6,R)-6-[(,R)-(-)-2-amino-2-(p-hidroxifenil)acetamido]-3,3-dimetil-7- Trihidrato de ácido oxo-4-tia-1-azabiciclo[3.2.0]heptano-2-carboxílico. Puede representarse estructuralmente como:
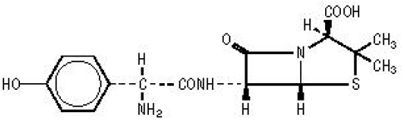
La fórmula molecular de la amoxicilina es C16H19N3O5S•3H2O y el peso molecular es 419,45.
Cápsulas : Cada cápsula de AMOXIL, con tapa opaca azul real y cuerpo opaco rosa, contiene 250 mg o 500 mg de amoxicilina como trihidrato. La tapa y el cuerpo de la cápsula de 250 mg están impresos con el nombre del producto AMOXIL 1000 mg y 250; la tapa y el cuerpo de la cápsula de 500 mg están impresos con AMOXIL 1000 mg y 500. Ingredientes inactivos: D&C Red No. 28, FD&C Blue No. 1, FD&C Red No. 40, gelatina, estearato de magnesio y dióxido de titanio.
Cada comprimido contiene 500 mg u 875 mg de amoxicilina como trihidrato. Cada comprimido rosa, recubierto con película, en forma de cápsula, está grabado con AMOXIL 500 mg centrado sobre 500 o 875, respectivamente. La tableta de 875 mg está ranurada en el reverso. Ingredientes inactivos: dióxido de silicio coloidal, crospovidona, laca de aluminio FD&C Red No. 30, hipromelosa, estearato de magnesio, celulosa microcristalina, polietilenglicol, glicolato de almidón de sodio y dióxido de titanio.
Polvo para Suspensión Oral Cada 5 ml de suspensión reconstituida contiene 125 mg, 200 mg, 250 mg o 400 mg de amoxicilina como trihidrato. Cada 5 ml de la suspensión reconstituida de 125 mg contiene 0,11 mEq (2,51 mg) de sodio. Cada 5 ml de la suspensión reconstituida de 200 mg contiene 0,15 mEq (3,39 mg) de sodio. Cada 5 ml de la suspensión reconstituida de 250 mg contiene 0,15 mEq (3,36 mg) de sodio; cada 5 ml de la suspensión reconstituida de 400 mg contiene 0,19 mEq (4,33 mg) de sodio. Ingredientes inactivos: FD&C Red No. 3, saborizantes, gel de sílice, benzoato de sodio, citrato de sodio, sacarosa y goma xantana.
INDICACIONES
Infecciones del oído, la nariz y la garganta
AMOXIL® está indicado en el tratamiento de infecciones debidas a aislados de especies de Streptococcus susceptibles (ÚNICAMENTE β-lactamasa negativas). (aislados hemolíticos α y β solamente), Streptococcus pneumoniae, Staphylococcus spp. o Haemophilus influenzae.
Infecciones Del Tracto Genitourinario
AMOXIL® está indicado en el tratamiento de infecciones debidas a aislados susceptibles (ÚNICAMENTE β-lactamasa negativos) de Escherichia coli, Proteus mirabilis o Enterococcus faecalis.
Infecciones De La Piel Y La Estructura De La Piel
AMOXIL® está indicado en el tratamiento de infecciones debidas a aislados susceptibles (SOLO β-lactamasa negativos) de Streptococcus spp. (aislados hemolíticos α y β solamente), Staphylococcus spp. o E. coli.
Infecciones Del Tracto Respiratorio Inferior
AMOXIL® está indicado en el tratamiento de infecciones debidas a aislados susceptibles (SOLO β-lactamasa negativos) de Streptococcus spp. (aislados hemolíticos α y β solamente), S. pneumoniae, Staphylococcus spp. o H. influenzae.
Infección por Helicobacter Pylori
Triple Terapia para Helicobacter Pylori con Claritromicina y Lansoprazol
AMOXIL, en combinación con claritromicina más lansoprazol como terapia triple, está indicado para el tratamiento de pacientes con infección por H. pylori y enfermedad de úlcera duodenal (úlcera duodenal activa o de 1 año de evolución) para erradicar H. pylori. Se ha demostrado que la erradicación de H. pylori reduce el riesgo de recurrencia de la úlcera duodenal.
Terapia Dual para H. Pylori con Lansoprazol
AMOXIL, en combinación con lansoprazol en cápsulas de liberación retardada como terapia dual, está indicado para el tratamiento de pacientes con infección por H. pylori y enfermedad ulcerosa duodenal (activa o con antecedentes de úlcera duodenal de 1 año) que son alérgicos o intolerantes a la claritromicina o en quienes se conoce o sospecha resistencia a la claritromicina. (Ver el prospecto de claritromicina , Microbiología .) Se ha demostrado que la erradicación de H. pylori reduce el riesgo de recurrencia de la úlcera duodenal.
Uso
Para reducir el desarrollo de bacterias resistentes a los medicamentos y mantener la eficacia de AMOXIL (amoxicilina) y otros medicamentos antibacterianos, AMOXIL 250 mg debe usarse solo para tratar infecciones que se compruebe o se sospeche que son causadas por bacterias. Cuando la información de cultivo y susceptibilidad esté disponible, se debe considerar al seleccionar o modificar la terapia antibacteriana. En ausencia de tales datos, la epidemiología local y los patrones de susceptibilidad pueden contribuir a la selección empírica de la terapia.
DOSIFICACIÓN Y ADMINISTRACIÓN
Dosificación para pacientes adultos y pediátricos > 3 meses de edad
El tratamiento debe continuarse durante un mínimo de 48 a 72 horas más allá del momento en que el paciente se vuelva asintomático o se haya obtenido evidencia de erradicación bacteriana. Se recomienda un tratamiento de al menos 10 días para cualquier infección causada por Streptococcus pyogenes para prevenir la aparición de fiebre reumática aguda. En algunas infecciones, la terapia puede ser necesaria durante varias semanas. Puede ser necesario continuar el seguimiento clínico y/o bacteriológico durante varios meses después de la interrupción del tratamiento.
Posología en recién nacidos y lactantes de ≤ 12 semanas (≤ 3 meses)
El tratamiento debe continuarse durante un mínimo de 48 a 72 horas más allá del momento en que el paciente se vuelva asintomático o se haya obtenido evidencia de erradicación bacteriana. Se recomienda un tratamiento de al menos 10 días para cualquier infección causada por Streptococcus pyogenes para prevenir la aparición de fiebre reumática aguda. Debido al desarrollo incompleto de la función renal que afecta la eliminación de amoxicilina en este grupo de edad, la dosis máxima recomendada de AMOXIL es de 30 mg/kg/día dividida cada 12 horas. Actualmente no hay recomendaciones de dosificación para pacientes pediátricos con insuficiencia renal.
Dosificación para la infección por H. Pylori
Triple terapia
La dosis oral recomendada para adultos es 1 gramo de AMOXIL 1000 mg, 500 mg de claritromicina y 30 mg de lansoprazol, todos administrados dos veces al día (cada 12 horas) durante 14 días.
Terapia dual
La dosis oral recomendada para adultos es de 1 gramo de AMOXIL 625 mg y 30 mg de lansoprazol, administrados cada uno tres veces al día (cada 8 horas) durante 14 días. Consulte la información de prescripción completa de claritromicina y lansoprazol.
Dosificación en insuficiencia renal
- Los pacientes con insuficiencia renal generalmente no requieren una reducción de la dosis a menos que la insuficiencia sea grave.
- Pacientes con insuficiencia grave con una tasa de filtración glomerular
- Los pacientes con una tasa de filtración glomerular de 10 a 30 ml/min deben recibir 500 mg o 250 mg cada 12 horas, según la gravedad de la infección.
- Los pacientes con una tasa de filtración glomerular inferior a 10 ml/min deben recibir 500 mg o 250 mg cada 24 horas, según la gravedad de la infección.
- Los pacientes en hemodiálisis deben recibir 500 mg o 250 mg cada 24 horas, según la gravedad de la infección. Deben recibir una dosis adicional tanto durante como al final de la diálisis.
Instrucciones para mezclar la suspensión oral
Golpee la botella hasta que todo el polvo fluya libremente. Agregue aproximadamente 1/3 de la cantidad total de agua para la reconstitución (consulte la Tabla 2) y agite vigorosamente hasta obtener un polvo húmedo. Agregue el resto del agua y vuelva a agitar vigorosamente.
Después de la reconstitución, la cantidad requerida de suspensión debe colocarse directamente en la lengua del niño para que la trague. Los medios alternativos de administración son agregar la cantidad requerida de suspensión a la fórmula, leche, jugo de frutas, agua, ginger ale o bebidas frías. Estos preparados deben tomarse inmediatamente.
NOTA: AGITE BIEN LA SUSPENSIÓN ORAL ANTES DE USAR. Mantenga la botella bien cerrada. Cualquier porción no utilizada de la suspensión reconstituida debe desecharse después de 14 días. La refrigeración es preferible, pero no obligatoria.
CÓMO SUMINISTRADO
Formas de dosificación y concentraciones
Cápsulas
250 mg, 500 mg. Cada cápsula de AMOXIL 625 mg, con tapa azul royal opaca y cuerpo rosa opaco, contiene 250 mg o 500 mg de amoxicilina como trihidrato. La tapa y el cuerpo de la cápsula de 250 mg están impresos con el nombre del producto AMOXIL y 250; la tapa y el cuerpo de la cápsula de 500 mg están impresos con AMOXIL y 500.
tabletas
500 mg, 875 mg. Cada comprimido contiene 500 mg u 875 mg de amoxicilina como trihidrato. Cada comprimido rosado, recubierto con película, en forma de cápsula, está grabado con AMOXIL centrado sobre 500 u 875, respectivamente. La tableta de 875 mg está ranurada en el reverso.
Polvo para Suspensión Oral
125 mg/5 ml, 200 mg/5 ml, 250 mg/5 ml, 400 mg/5 ml. Cada 5 ml de suspensión reconstituida con sabor a fresa contiene 125 mg de amoxicilina como trihidrato. Cada 5 ml de suspensión reconstituida con sabor a chicle contiene 200 mg, 250 mg o 400 mg de amoxicilina como trihidrato.
Almacenamiento y manipulación
Cápsulas: Cada cápsula de AMOXIL, con tapa opaca azul real y cuerpo opaco rosa, contiene 250 mg o 500 mg de amoxicilina como trihidrato. La tapa y el cuerpo de la cápsula de 250 mg están impresos con el nombre del producto AMOXIL y 250; la tapa y el cuerpo de la cápsula de 500 mg están impresos con AMOXIL y 500.
Cápsula de 250 mg
CDN 43598-025-01 Botellas de 100 CDN 43598-025-05 Botellas de 500
Cápsula de 500 mg
CDN 43598-005-01 Botellas de 100 CDN 43598-005-05 Botellas de 500
Cada comprimido contiene 500 mg u 875 mg de amoxicilina como trihidrato. Cada comprimido rosado, recubierto con película, en forma de cápsula, está grabado con AMOXIL centrado sobre 500 u 875, respectivamente. La tableta de 875 mg está ranurada en el reverso.
Tableta de 500 mg
CDN 43598-024-01 Botellas de 100 CDN 43598-024-05 Botellas de 500
Tableta de 875 mg
CDN 43598-019-01 Botellas de 100 CDN 43598-019-14 Botellas de 20
Polvo para Suspensión Oral: Cada 5 ml de suspensión reconstituida con sabor a fresa contiene 125 mg de amoxicilina como trihidrato. Cada 5 ml de suspensión reconstituida con sabor a chicle contiene 200 mg, 250 mg o 400 mg de amoxicilina como trihidrato.
125 mg/5 ml
CDN 43598-022-80 Botella de 80 ml CDN 43598-022-52 Botella de 100 ml CDN 43598-022-53 Botella de 150 ml
200 mg/5 ml
CDN 43598-023-50 Botella de 50 ml CDN 43598-023-51 Botella de 75 ml CDN 43598-023-52 Botella de 100 ml
250 mg/5 ml
CDN 43598-009-80 Botella de 80 ml CDN 43598-009-52 Botella de 100 ml CDN 43598-009-53 Botella de 150 ml
400 mg/5 ml
CDN 43598-007-50 Botella de 50 ml CDN 43598-007-51 botella de 75 ml CDN 43598-007-52 Botella de 100 ml
Almacenar a 20° C (68° F) o menos - Cápsulas de 250 mg y 500 mg y polvo sin reconstituir de 125 mg y 250 mg.
Almacenar a 25 °C (77 °F) o menos. Comprimidos de 500 mg y 875 mg y polvo no reconstituido de 200 mg y 400 mg.
Dispensar en un recipiente hermético.
Fabricado. Por: Dr. Reddy's Laboratories Tennessee, LLC. Bristol, TN 37620. Revisado: septiembre de 2015
EFECTOS SECUNDARIOS
Lo siguiente se discute con más detalle en otras secciones del etiquetado:
- Reacciones anafilácticas [ver ADVERTENCIAS Y PRECAUCIONES ]
- CDAD [ver ADVERTENCIAS Y PRECAUCIONES ]
Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy diversas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no pueden compararse directamente con las tasas de los ensayos clínicos de otro fármaco y es posible que no reflejen las tasas observadas en la práctica.
Las reacciones adversas más comunes (> 1 %) observadas en los ensayos clínicos de cápsulas, tabletas o suspensión oral de AMOXIL fueron diarrea, sarpullido, vómitos y náuseas.
Triple terapia : Los eventos adversos informados con mayor frecuencia en pacientes que recibieron terapia triple (amoxicilina/claritromicina/lansoprazol) fueron diarrea (7 %), dolor de cabeza (6 %) y alteración del gusto (5 %).
Terapia dual : Los eventos adversos informados con mayor frecuencia en los pacientes que recibieron la terapia doble de amoxicilina/lansoprazol fueron diarrea (8 %) y dolor de cabeza (7 %). Para obtener más información sobre las reacciones adversas con claritromicina o lansoprazol, consulte la sección Reacciones adversas de sus prospectos.
Experiencia posterior a la comercialización u otra experiencia
Además de los eventos adversos informados en los ensayos clínicos, se identificaron los siguientes eventos durante el uso posterior a la comercialización de las penicilinas. Debido a que son reportados voluntariamente por una población de tamaño desconocido, no se pueden hacer estimaciones de frecuencia. Estos eventos han sido elegidos para su inclusión debido a una combinación de su gravedad, frecuencia de notificación o posible conexión causal con AMOXIL.
- Infecciones e Infestaciones : Candidiasis mucocutánea.
- Gastrointestinal : Lengua vellosa negra y colitis hemorrágica/pseudomembranosa. El inicio de los síntomas de la colitis pseudomembranosa puede ocurrir durante o después del tratamiento antibacteriano [ver ADVERTENCIAS Y PRECAUCIONES ].
- Reacciones hipersensibles : anafilaxia [ver ADVERTENCIAS Y PRECAUCIONES ]. Se han informado reacciones similares a la enfermedad del suero, erupciones maculopapulares eritematosas, eritema multiforme, síndrome de Stevens-Johnson, dermatitis exfoliativa, necrólisis epidérmica tóxica, pustulosis exantemática aguda generalizada, vasculitis por hipersensibilidad y urticaria.
- Hígado Se ha observado un aumento moderado de AST y/o ALT, pero se desconoce el significado de este hallazgo. Se han informado casos de disfunción hepática que incluyen ictericia colestásica, colestasis hepática y hepatitis citolítica aguda.
- Renal : Se ha notificado cristaluria [ver SOBREDOSIS ].
- Sistemas Hemático y Linfático : Se ha notificado anemia, incluida anemia hemolítica, trombocitopenia, púrpura trombocitopénica, eosinofilia, leucopenia y agranulocitosis. Estas reacciones suelen ser reversibles al interrumpir el tratamiento y se cree que son fenómenos de hipersensibilidad.
- Sistema nervioso central : Se han informado hiperactividad reversible, agitación, ansiedad, insomnio, confusión, convulsiones, cambios de comportamiento y/o mareos.
- Misceláneas : Se ha informado decoloración de los dientes (tinción marrón, amarilla o gris). La mayoría de los informes ocurrieron en pacientes pediátricos. La decoloración se redujo o eliminó con cepillado o limpieza dental en la mayoría de los casos.
INTERACCIONES CON LA DROGAS
probenecid
El probenecid disminuye la secreción tubular renal de amoxicilina. El uso simultáneo de amoxicilina y probenecid puede resultar en un aumento y prolongación de los niveles sanguíneos de amoxicilina.
Anticoagulantes orales
Se ha notificado una prolongación anormal del tiempo de protrombina (aumento del índice internacional normalizado [INR]) en pacientes que reciben amoxicilina y anticoagulantes orales. Se debe realizar un control adecuado cuando se prescriben anticoagulantes al mismo tiempo. Pueden ser necesarios ajustes en la dosis de anticoagulantes orales para mantener el nivel deseado de anticoagulación.
alopurinol
La administración concomitante de alopurinol y amoxicilina aumenta la incidencia de erupciones cutáneas en pacientes que reciben ambos fármacos en comparación con pacientes que reciben amoxicilina sola. No se sabe si esta potenciación de las erupciones por amoxicilina se debe al alopurinol oa la hiperuricemia presente en estos pacientes.
Anticonceptivos orales
AMOXIL puede afectar la flora intestinal, lo que lleva a una menor reabsorción de estrógenos y a una reducción de la eficacia de los anticonceptivos orales combinados de estrógeno/progesterona.

Otros antibacterianos
El cloranfenicol, los macrólidos, las sulfonamidas y las tetraciclinas pueden interferir con los efectos bactericidas de la penicilina. Esto se ha demostrado in vitro; sin embargo, la importancia clínica de esta interacción no está bien documentada.
Efectos en las pruebas de laboratorio
Las concentraciones altas de ampicilina en la orina pueden dar lugar a reacciones falsas positivas cuando se analiza la presencia de glucosa en la orina con CLINITEST®, la solución de Benedict o la solución de Fehling. Dado que este efecto también puede ocurrir con amoxicilina, se recomienda utilizar pruebas de glucosa basadas en reacciones enzimáticas de glucosa oxidasa (como CLINISTIX®).
Después de la administración de ampicilina o amoxicilina a mujeres embarazadas, se ha observado una disminución transitoria en la concentración plasmática de estriol conjugado total, estriol-glucurónido, estrona conjugada y estradiol.
ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Reacciones anafilácticas
Se han notificado reacciones de hipersensibilidad (anafilácticas) graves y, en ocasiones, mortales en pacientes tratados con penicilina, incluida la amoxicilina. Aunque la anafilaxia es más frecuente después de la terapia parenteral, ha ocurrido en pacientes que toman penicilinas orales. Es más probable que estas reacciones ocurran en personas con antecedentes de hipersensibilidad a la penicilina y/o antecedentes de sensibilidad a múltiples alérgenos. Ha habido informes de personas con antecedentes de hipersensibilidad a la penicilina que han experimentado reacciones graves cuando se les trata con cefalosporinas. Antes de iniciar la terapia con AMOXIL, se debe realizar una investigación cuidadosa sobre las reacciones de hipersensibilidad previas a las penicilinas, cefalosporinas u otros alérgenos.
Diarrea asociada a Clostridium difficile
Se ha informado diarrea asociada a Clostridium difficile (CDAD) con el uso de casi todos los agentes antibacterianos, incluido AMOXIL, y puede variar en gravedad desde diarrea leve hasta colitis fatal. El tratamiento con agentes antibacterianos altera la flora normal del colon y conduce al crecimiento excesivo de C. difficile.
C. difficile produce toxinas A y B que contribuyen al desarrollo de CDAD. Las cepas de C. difficile productoras de hipertoxina causan mayor morbilidad y mortalidad, ya que estas infecciones pueden ser refractarias a la terapia antimicrobiana y pueden requerir colectomía. Se debe considerar CDAD en todos los pacientes que presenten diarrea después del uso de antibacterianos. Es necesaria una cuidadosa historia clínica ya que se ha informado que la CDAD ocurre más de 2 meses después de la administración de agentes antibacterianos.
Si se sospecha o se confirma CDAD, es posible que deba suspenderse el uso continuo de antibióticos no dirigidos contra C. difficile. Se debe instituir el manejo adecuado de líquidos y electrolitos, la suplementación con proteínas, el tratamiento con antibióticos de C. difficile y la evaluación quirúrgica según esté clínicamente indicado.
Desarrollo de bacterias resistentes a los medicamentos
Prescribir AMOXIL en ausencia de una infección bacteriana comprobada o fuertemente sospechada es poco probable que brinde beneficios al paciente y aumenta el riesgo de desarrollo de bacterias resistentes a los medicamentos.
Uso en pacientes con mononucleosis
Un alto porcentaje de pacientes con mononucleosis que reciben amoxicilina desarrollan una erupción cutánea eritematosa. Por lo tanto, la amoxicilina no debe administrarse a pacientes con mononucleosis.
fenilcetonúricos
Los comprimidos masticables de Amoxil 250 mg contienen aspartamo, que contiene fenilalanina. Cada comprimido masticable de 200 mg contiene 1,82 mg de fenilalanina; cada comprimido masticable de 400 mg contiene 3,64 mg de fenilalanina. Las suspensiones orales de Amoxil no contienen fenilalanina y pueden ser utilizadas por fenilcetonúricos.
Toxicología no clínica
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
No se han realizado estudios a largo plazo en animales para evaluar el potencial carcinogénico. No se han realizado estudios para detectar el potencial mutagénico de la amoxicilina sola; sin embargo, la siguiente información está disponible a partir de pruebas en una mezcla 4:1 de amoxicilina y clavulanato de potasio (AUGMENTIN). AUGMENTIN no fue mutagénico en el ensayo de mutación bacteriana de Ames y en el ensayo de conversión de genes de levadura. AUGMENTIN fue débilmente positivo en el ensayo de linfoma de ratón, pero la tendencia hacia el aumento de las frecuencias de mutación en este ensayo se produjo en dosis que también se asociaron con una disminución de la supervivencia celular. AUGMENTIN fue negativo en la prueba de micronúcleos de ratón y en el ensayo letal dominante en ratones. El clavulanato de potasio solo se probó en el ensayo de mutación bacteriana de Ames y en la prueba de micronúcleo de ratón, y dio negativo en cada uno de estos ensayos. En un estudio de reproducción multigeneracional en ratas, no se observaron alteraciones de la fertilidad ni otros efectos reproductivos adversos con dosis de hasta 500 mg/kg (aproximadamente 2 veces la dosis humana de 3 g en función del área de superficie corporal).
Uso en poblaciones específicas
El embarazo
Efectos teratogénicos
Embarazo Categoría B. Se han realizado estudios de reproducción en ratones y ratas a dosis de hasta 2000 mg/kg (3 y 6 veces la dosis humana de 3 g, según el área de superficie corporal). No hubo evidencia de daño al feto debido a la amoxicilina. Sin embargo, no existen estudios adecuados y bien controlados en mujeres embarazadas. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, la amoxicilina debe usarse durante el embarazo solo si es claramente necesario.
Trabajo y entrega
La ampicilina oral se absorbe poco durante el trabajo de parto. No se sabe si el uso de amoxicilina en humanos durante el parto tiene efectos adversos inmediatos o retardados en el feto, prolonga la duración del trabajo de parto o aumenta la probabilidad de necesidad de una intervención obstétrica.
Madres lactantes
Se ha demostrado que las penicilinas se excretan en la leche humana. El uso de amoxicilina por parte de madres lactantes puede provocar la sensibilización de los bebés. Se debe tener precaución cuando se administra amoxicilina a una mujer lactante.
Uso pediátrico
Debido al desarrollo incompleto de la función renal en recién nacidos y niños pequeños, la eliminación de amoxicilina puede retrasarse. La dosificación de AMOXIL 625 mg debe modificarse en pacientes pediátricos de 12 semanas o menos (≤ 3 meses). [Ver DOSIFICACIÓN Y ADMINISTRACIÓN ]
Uso geriátrico
Se realizó un análisis de estudios clínicos de AMOXIL 250 mg para determinar si los sujetos de 65 años o más responden de manera diferente a los sujetos más jóvenes. Estos análisis no han identificado diferencias en las respuestas entre los pacientes mayores y los más jóvenes, pero no se puede descartar una mayor sensibilidad de algunos individuos mayores.
Se sabe que este fármaco se excreta sustancialmente por vía renal, y el riesgo de reacciones tóxicas a este fármaco puede ser mayor en pacientes con insuficiencia renal. Debido a que es más probable que los pacientes de edad avanzada tengan una función renal disminuida, se debe tener cuidado en la selección de la dosis y puede ser útil monitorear la función renal.
Dosificación en insuficiencia renal
La amoxicilina se elimina principalmente por vía renal y generalmente se requiere un ajuste de dosis en pacientes con insuficiencia renal grave (TFG Dosificación en insuficiencia renal para recomendaciones específicas en pacientes con insuficiencia renal.
SOBREDOSIS
En caso de sobredosis, suspenda la medicación, trate sintomáticamente e instituya medidas de apoyo según sea necesario. Un estudio prospectivo de 51 pacientes pediátricos en un centro de toxicología sugirió que las sobredosis de menos de 250 mg/kg de amoxicilina no están asociadas con síntomas clínicos significativos.
Se ha informado nefritis intersticial que resultó en insuficiencia renal oligúrica en un pequeño número de pacientes después de una sobredosis con amoxicilina1.
También se ha notificado cristaluria, que en algunos casos conduce a insuficiencia renal, después de una sobredosis de amoxicilina en pacientes adultos y pediátricos. En caso de sobredosis, se debe mantener una ingesta adecuada de líquidos y diuresis para reducir el riesgo de cristaluria por amoxicilina.
La insuficiencia renal parece ser reversible con el cese de la administración del fármaco. Los niveles sanguíneos altos pueden ocurrir más fácilmente en pacientes con función renal alterada debido a la disminución de la depuración renal de amoxicilina. La amoxicilina puede eliminarse de la circulación mediante hemodiálisis.
CONTRAINDICACIONES
AMOXIL 625 mg está contraindicado en pacientes que han experimentado una reacción de hipersensibilidad grave (p. ej., anafilaxia o síndrome de Stevens-Johnson) a AMOXIL oa otros antibióticos betalactámicos (p. ej., penicilinas y cefalosporinas).
FARMACOLOGÍA CLÍNICA
Mecanismo de acción
La amoxicilina es un fármaco antibacteriano. [ver Microbiología ].
Farmacocinética
Absorción
La amoxicilina es estable en presencia de ácido gástrico y se absorbe rápidamente después de la administración oral. Se ha investigado parcialmente el efecto de los alimentos sobre la absorción de amoxicilina de las tabletas y suspensión de AMOXIL; Las formulaciones de 400 mg y 875 mg se han estudiado solo cuando se administran al comienzo de una comida ligera.
Las dosis administradas por vía oral de cápsulas de amoxicilina de 250 mg y 500 mg dan como resultado niveles sanguíneos máximos promedio de 1 a 2 horas después de la administración en el rango de 3.5 mcg/mL a 5.0 mcg/mL y 5.5 mcg/mL a 7.5 mcg/mL, respectivamente .
Los parámetros farmacocinéticos promedio de amoxicilina de un estudio de bioequivalencia cruzado de dosis única, abierto, de dos partes en 27 adultos que compararon 875 mg de AMOXIL con 875 mg de AUGMENTIN® (amoxicilina/clavulanato de potasio) mostraron que la tableta de 875 mg de AMOXIL 500 mg produce una AUC0-∞ de 35,4 ± 8,1 mcg•hr/mL y una Cmax de 13,8 ± 4,1 mcg/mL. La dosificación se realizó al comienzo de una comida ligera después de un ayuno nocturno.
Las dosis de suspensión de amoxicilina administradas por vía oral, 125 mg/5 ml y 250 mg/5 ml, dan como resultado niveles sanguíneos máximos promedio de 1 a 2 horas después de la administración en el rango de 1,5 mcg/ml a 3,0 mcg/ml y 3,5 mcg/ml a 5,0 mcg/mL, respectivamente.
La administración oral de dosis únicas de tabletas masticables de 400 mg y una suspensión de 400 mg/5 ml de AMOXIL 625 mg a 24 voluntarios adultos produjo datos farmacocinéticos comparables:
Distribución
La amoxicilina se difunde fácilmente en la mayoría de los tejidos y fluidos corporales, con excepción del cerebro y el líquido cefalorraquídeo, excepto cuando las meninges están inflamadas. En el suero sanguíneo, la amoxicilina se une a proteínas en aproximadamente un 20%. Después de una dosis de 1 gramo y utilizando una técnica especial de ventana de piel para determinar los niveles del antibiótico, se observó que se encontraron niveles terapéuticos en el líquido intersticial.
Metabolismo y Excreción
La vida media de la amoxicilina es de 61,3 minutos. Aproximadamente el 60% de una dosis de amoxicilina administrada por vía oral se excreta en la orina dentro de las 6 a 8 horas. Los niveles séricos detectables se observan hasta 8 horas después de una dosis de amoxicilina administrada por vía oral. Dado que la mayor parte de la amoxicilina se excreta sin cambios en la orina, su excreción puede retrasarse mediante la administración concomitante de probenecid [ver INTERACCIONES CON LA DROGAS ].
Microbiología
Mecanismo de acción
La amoxicilina es similar a la penicilina en su acción bactericida contra bacterias susceptibles durante la etapa de multiplicación activa. Actúa a través de la inhibición de la biosíntesis de la pared celular que conduce a la muerte de la bacteria.
Mecanismo de Resistencia
La resistencia a la amoxicilina está mediada principalmente a través de enzimas llamadas betalactamasas que rompen el anillo betalactámico de la amoxicilina, volviéndolo inactivo.
Se ha demostrado que la amoxicilina es activa contra la mayoría de los aislamientos de las bacterias enumeradas a continuación, tanto in vitro como en infecciones clínicas, como se describe en la INDICACIONES Y USO sección.
bacterias grampositivas
Enterococcus faecalis Staphylococcus spp. Streptococcus pneumoniae Streptococcus spp. (alfa y beta-hemolítico)
Bacterias Gram-negativo
Escherichia coli Haemophilus influenzae Helicobacter pylori Proteus mirabilis
Métodos de prueba de susceptibilidad
Cuando esté disponible, el laboratorio de microbiología clínica debe proporcionar al médico los resultados acumulados de las pruebas de susceptibilidad in vitro para los medicamentos antimicrobianos utilizados en hospitales locales y áreas de práctica como informes periódicos que describen el perfil de susceptibilidad de los patógenos nosocomiales y adquiridos en la comunidad. Estos informes deberían ayudar al médico a seleccionar el antimicrobiano más eficaz.
Técnicas de dilución: Los métodos cuantitativos se utilizan para determinar las concentraciones inhibitorias mínimas (CIM) antimicrobianas. Estos MIC proporcionan estimaciones de la susceptibilidad de las bacterias a los compuestos antimicrobianos. Las CIM deben determinarse utilizando un método de prueba estandarizado (caldo o agar)2,4. Los valores de MIC deben interpretarse de acuerdo con los criterios de la Tabla 4.
Técnicas de difusión: Los métodos cuantitativos que requieren la medición de los diámetros de las zonas también pueden proporcionar estimaciones reproducibles de la susceptibilidad de las bacterias a los compuestos antimicrobianos3,4. El tamaño de la zona debe determinarse utilizando un método de prueba estandarizado3.
La susceptibilidad a la amoxicilina de Enterococcus spp., Enterobacteriaceae y H. influenzae puede inferirse mediante la prueba de ampicilina4. La susceptibilidad a la amoxicilina de Staphylococcus spp., y Streptococcus spp. beta-hemolítico, puede inferirse mediante la prueba de penicilina4. La mayoría de los aislamientos de Enterococcus spp. que son resistentes a la ampicilina o la amoxicilina producen una betalactamasa de tipo TEM. Una prueba de betalactamasa puede proporcionar un medio rápido para determinar la resistencia a la ampicilina y la amoxicilina4.
La susceptibilidad a la amoxicilina de Streptococcus pneumoniae (aislados que no son de meningitis) se puede inferir mediante pruebas de penicilina u oxacilina4. Los criterios de interpretación de S. pneumoniae a la amoxicilina se proporcionan en la Tabla 44.
Un informe de "Sensible" indica que es probable que el antimicrobiano inhiba el crecimiento del patógeno si el compuesto antimicrobiano alcanza una concentración en el sitio de infección necesaria para inhibir el crecimiento del patógeno. Un informe de "Intermedio" indica que el resultado debe considerarse equívoco y, si el microorganismo no es completamente susceptible a fármacos alternativos clínicamente factibles, la prueba debe repetirse. Esta categoría implica una posible aplicabilidad clínica en sitios del cuerpo donde el fármaco se concentra fisiológicamente. Esta categoría también proporciona una zona de amortiguamiento que evita que pequeños factores técnicos no controlados causen grandes discrepancias en la interpretación. Un informe de "Resistente" indica que no es probable que el antimicrobiano inhiba el crecimiento del patógeno si el compuesto antimicrobiano alcanza la concentración que normalmente se alcanza en el sitio de la infección; debe seleccionarse otra terapia.
Pruebas de susceptibilidad para Helicobacter Pylori
Los métodos de prueba de susceptibilidad in vitro de amoxicilina para determinar las concentraciones inhibitorias mínimas (MIC) y los tamaños de zona no han sido estandarizados, validados o aprobados para probar H. pylori. Las muestras para H. pylori y los resultados de las pruebas de susceptibilidad a la claritromicina se deben obtener en aislamientos de pacientes que no respondieron a la terapia triple. Si se encuentra resistencia a la claritromicina, se debe usar un régimen que no contenga claritromicina.
Control de calidad
Los procedimientos de prueba de susceptibilidad estandarizados2,3,4 requieren el uso de controles de laboratorio para monitorear y garantizar la exactitud y precisión de los suministros y reactivos utilizados en el ensayo, y las técnicas de las personas que realizan el control de la prueba. El polvo de amoxicilina estándar debe proporcionar el siguiente rango de valores de MIC que se proporcionan en la Tabla 54. Para la técnica de difusión, se deben lograr los criterios proporcionados en la Tabla 5.
Estudios clínicos
Erradicación de H. pylori para reducir el riesgo de recurrencia de la úlcera duodenal
Los estudios clínicos aleatorizados, doble ciego realizados en los Estados Unidos en pacientes con H. pylori y enfermedad de úlcera duodenal (definida como una úlcera activa o antecedentes de una úlcera dentro de 1 año) evaluaron la eficacia de lansoprazol en combinación con cápsulas de amoxicilina y tabletas de claritromicina. como terapia triple de 14 días, o en combinación con cápsulas de amoxicilina como terapia dual de 14 días, para la erradicación de H. pylori. Con base en los resultados de estos estudios, se estableció la seguridad y eficacia de 2 regímenes de erradicación diferentes: Terapia triple: Amoxicilina 1 gramo dos veces al día/claritromicina 500 mg dos veces al día/lansoprazol 30 mg dos veces al día (ver Tabla 6). Terapia dual: Amoxicilina 1 gramo tres veces al día/lansoprazol 30 mg tres veces al día (ver Tabla 7. Todos los tratamientos fueron por 14 días. La erradicación de H. pylori se definió como 2 pruebas negativas (cultivo e histología) a las 4 a 6 semanas después de la final del tratamiento La terapia triple ha demostrado ser más eficaz que todas las combinaciones posibles de terapia dual La terapia dual ha demostrado ser más eficaz que ambas monoterapias Se ha demostrado que la erradicación de H. pylori reduce el riesgo de recurrencia de la úlcera duodenal
REFERENCIAS
1. Swanson-Biearman B, Dean BS, López G, Krenzelok EP. Los efectos de la ingestión de penicilinas y cefalosporinas en niños menores de seis años. Vet Hum Toxicol. 1988; 30: 66-67.
2. Instituto de Normas Clínicas y de Laboratorio (CLSI). Métodos para pruebas de susceptibilidad antimicrobiana por dilución para bacterias que crecen aeróbicamente; Norma Aprobada – Décima Edición. Documento CLSI M07-A10, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, EE. UU., 2015.
3. Instituto de Normas Clínicas y de Laboratorio (CLSI). Normas de rendimiento para las pruebas de susceptibilidad a la difusión por disco de antimicrobianos; Norma Aprobada – Duodécima Edición. Documento CLSI M02-A12, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, EE. UU., 2015.
4. Instituto de Normas Clínicas y de Laboratorio (CLSI). Estándares de Desempeño para Pruebas de Susceptibilidad Antimicrobiana; Vigésimo Quinto Suplemento Informativo, CLSI documento M100-S25. Documento CLSI M100-S25, Clinical and Laboratory Standards Institute, 950 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087, EE. UU., 2015.
INFORMACIÓN DEL PACIENTE
- Se debe advertir a los pacientes que AMOXIL puede tomarse cada 8 horas o cada 12 horas, según la dosis prescrita.
- Se debe advertir a los pacientes que los medicamentos antibacterianos, incluido AMOXIL, solo deben usarse para tratar infecciones bacterianas. No tratan infecciones virales (p. ej., el resfriado común). Cuando se prescribe AMOXIL 250 mg para tratar una infección bacteriana, se debe informar a los pacientes que, aunque es común que se sientan mejor al comienzo de la terapia, el medicamento debe tomarse exactamente como se indica. Omitir dosis o no completar el curso completo de la terapia puede: (1) disminuir la eficacia del tratamiento inmediato y (2) aumentar la probabilidad de que las bacterias desarrollen resistencia y no sean tratables con AMOXIL 625 mg u otros medicamentos antibacterianos en el futuro .
- Se debe advertir a los pacientes que la diarrea es un problema común causado por los antibióticos y que, por lo general, desaparece cuando se suspende el antibiótico. A veces, después de comenzar el tratamiento con antibióticos, los pacientes pueden desarrollar heces acuosas y sanguinolentas (con o sin calambres estomacales y fiebre) incluso 2 o más meses después de haber tomado la última dosis del antibiótico. Si esto ocurre, los pacientes deben comunicarse con su médico lo antes posible.
- Los pacientes deben saber que AMOXIL contiene un medicamento de la clase de las penicilinas que puede causar reacciones alérgicas en algunas personas.
