Minocin 50mg, 100mg Minocycline Hydrochloride Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es la suspensión oral de Minocin y cómo se usa?
Minocin (clorhidrato de minociclina) es un antibiótico de tetraciclina que se usa para tratar muchas infecciones bacterianas diferentes, como infecciones del tracto urinario, infecciones respiratorias, infecciones de la piel, acné severo, gonorrea, fiebre por garrapatas, clamidia y otras.
¿Cuáles son los efectos secundarios de la suspensión oral de Minocin?
Los efectos secundarios comunes de Minocin incluyen:
- mareo,
- sensación de cansancio,
- sensación de giro,
- dolor articular o muscular,
- decoloración de la piel, las uñas o las encías,
- náuseas,
- Diarrea,
- dolor de barriga,
- erupción o picazón en la piel,
- lengua hinchada, o
- picazón o secreción vaginal.
Informe a su médico si tiene efectos secundarios graves de Minocin 50 mg, incluidos:
- calambres en el estómago,
- diarrea acuosa o con sangre,
- sintomas de gripe,
- llagas en la boca y la garganta,
- debilidad,
- orina de color oscuro,
- sangrado inusual,
- puntos morados o rojos debajo de la piel,
- fiebre,
- erupción cutanea,
- hematomas,
- hormigueo intenso o entumecimiento,
- debilidad muscular,
- pérdida de apetito,
- coloración amarillenta de la piel o los ojos,
- Dolor de pecho,
- ritmo cardíaco irregular,
- tos,
- sibilancias,
- dificultad para respirar,
- confusión,
- vómitos,
- hinchazón,
- aumento de peso,
- orinar menos de lo normal o no orinar en absoluto,
- dolor de cabeza o dolor detrás de los ojos,
- zumbando en tus oídos,
- problemas de la vista,
- dolor en las articulaciones o hinchazón con fiebre,
- glándulas inflamadas,
- dolores musculares,
- malestar general,
- pensamientos o comportamientos inusuales,
- ataques (convulsiones), o
- una reacción severa de la piel.
Para reducir el desarrollo de bacterias resistentes a los medicamentos y mantener la eficacia de MINOCIN® Suspensión oral y otros medicamentos antibacterianos, MINOCIN Suspensión oral debe usarse solo para tratar o prevenir infecciones que se haya comprobado o que se sospeche que sean causadas por bacterias.
DESCRIPCIÓN
MINOCIN 100mg clorhidrato de minociclina, es un derivado semisintético de la tetraciclina, 4,7Bis(dimetilamino)-1,4,4a,5,5a,6,11,12a-octahidro-3,10,12,12a-tetrahidroxi-1,11 -monoclorhidrato de dioxo-2naftacenocarboxamida.
Su fórmula estructural es:
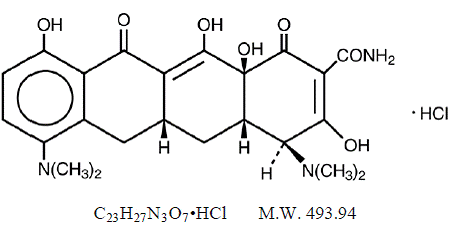 C23H27N3O7•HCl PM 493,94
C23H27N3O7•HCl PM 493,94 MINOCIN 50 mg suspensión oral contiene clorhidrato de minociclina equivalente a 50 mg de minociclina por 5 ml (10 mg/ml) y los siguientes ingredientes inactivos: alcohol, butilparabeno, hidróxido de calcio, celulosa, tetraoleato de decaglicerilo, edetato cálcico disódico, goma guar, polisorbato 80 , propilparabeno, propilenglicol, sacarina de sodio, sulfito de sodio (ver ADVERTENCIAS ) y Sorbitol.
INDICACIONES
MINOCIN 100 mg suspensión oral está indicado en el tratamiento de las siguientes infecciones debidas a cepas susceptibles de los microorganismos designados:
Fiebre maculosa de las Montañas Rocosas, fiebre tifoidea y el grupo del tifus, fiebre Q, rickettsiosis viruela y fiebres por garrapatas causadas por rickettsias.
Infecciones del tracto respiratorio causadas por Mycoplasma pneumoniae.
Linfogranuloma venéreo causado por Chlamydia trachomatis.
Psitacosis (ornitosis) por Chlamydophila psittaci.
Tracoma causado por Chlamydia trachomatis, aunque no siempre se elimina el agente infeccioso, a juzgar por la inmunofluorescencia.
Conjuntivitis de inclusión causada por Chlamydia trachomatis.
Uretritis no gonocócicas, infecciones endocervicales o rectales en adultos causadas por Ureaplasma urealyticum o Chlamydia trachomatis.
Fiebre recurrente por Borrelia recurrentis.
Chancroide causado por Haemophilus ducreyi.
Peste por Yersinia pestis.
Tularemia por Francisella tularensis.
Cólera causado por Vibrio cholerae.
Infecciones por Campylobacter fetus causadas por Campylobacter fetus.
Brucelosis debida a especies de Brucella (junto con estreptomicina).
Bartonelosis por Bartonella bacilliformis.
Granuloma inguinal causado por Klebsiella granulomatis.
La minociclina está indicada para el tratamiento de infecciones causadas por los siguientes microorganismos gramnegativos cuando las pruebas bacteriológicas indican una susceptibilidad adecuada al fármaco:
Escherichia coli.
Enterobacter aerogenes.
especies de Shigela.
especies de Acinetobacter.
Infecciones del tracto respiratorio causadas por Haemophilus influenzae.
Infecciones del tracto respiratorio y del tracto urinario causadas por especies de Klebsiella.
La suspensión oral de MINOCIN está indicada para el tratamiento de infecciones causadas por los siguientes microorganismos grampositivos cuando las pruebas bacteriológicas indican una susceptibilidad adecuada al fármaco:
Infecciones del tracto respiratorio superior causadas por Streptococcus pneumoniae. Infecciones de la piel y de la estructura de la piel causadas por Staphylococcus aureus (nota: la minociclina no es el fármaco de elección en el tratamiento de ningún tipo de infección estafilocócica).
Cuando la penicilina está contraindicada, la minociclina es un fármaco alternativo en el tratamiento de las siguientes infecciones:
Uretritis no complicada en hombres debida a Neisseria gonorrhoeae y para el tratamiento de otras infecciones gonocócicas.
Infecciones en mujeres causadas por Neisseria gonorrhoeae.
Sífilis causada por Treponema pallidum subespecie pallidum.
Pian causado por Treponema pallidum subespecie pertenue.
Listeriosis por Listeria monocytogenes.
Ántrax por Bacillus anthracis.
Infección de Vincent causada por Fusobacterium fusiforme.
Actinomicosis causada por Actinomyces israelii.
Infecciones causadas por especies de Clostridium.
En la amebiasis intestinal aguda, la minociclina puede ser un complemento útil de los amebicidas.
En el acné severo, la minociclina puede ser una terapia adyuvante útil.
La minociclina oral está indicada en el tratamiento de portadores asintomáticos de Neisseria meningitidis para eliminar los meningococos de la nasofaringe. Para preservar la utilidad de la minociclina en el tratamiento de portadores meningocócicos asintomáticos, se deben realizar procedimientos de diagnóstico de laboratorio, incluidos serotipificación y pruebas de susceptibilidad, para establecer el estado de portador y el tratamiento correcto. Se recomienda reservar el uso profiláctico de la minociclina para situaciones en las que el riesgo de meningitis meningocócica es alto.
La minociclina oral no está indicada para el tratamiento de la infección meningocócica.
Aunque no se han realizado estudios de eficacia clínica controlados, los datos clínicos limitados muestran que el clorhidrato de minociclina oral se ha utilizado con éxito en el tratamiento de infecciones causadas por Mycobacterium marinum.
Para reducir el desarrollo de bacterias resistentes a los medicamentos y mantener la eficacia de MINOCIN 100 mg Suspensión oral y otros medicamentos antibacterianos, MINOCIN Suspensión oral debe usarse solo para tratar o prevenir infecciones que se haya comprobado o que se sospeche que son causadas por bacterias susceptibles. Cuando la información de cultivo y susceptibilidad esté disponible, se debe considerar al seleccionar o modificar la terapia antibacteriana. En ausencia de tales datos, la epidemiología local y los patrones de susceptibilidad pueden contribuir a la selección empírica de la terapia.
DOSIFICACIÓN Y ADMINISTRACIÓN
LA DOSIS HABITUAL Y LA FRECUENCIA DE ADMINISTRACIÓN DE LA MINOCICLINA DIFEREN DE LAS DEMÁS TETRACICLINAS. SUPERAR LA DOSIS RECOMENDADA PUEDE RESULTAR EN UNA MAYOR INCIDENCIA DE EFECTOS SECUNDARIOS.
La terapia debe continuarse durante al menos 24 a 48 horas después de que los síntomas y la fiebre hayan desaparecido.
Los estudios realizados hasta la fecha han indicado que la absorción de MINOCIN Suspensión Oral no se ve notablemente influenciada por los alimentos y los productos lácteos.
La farmacocinética de la minociclina en pacientes con insuficiencia renal (CLCR ADVERTENCIAS ).
En el tratamiento de infecciones estreptocócicas, se debe administrar una dosis terapéutica de tetraciclina durante al menos diez días.
Para pacientes pediátricos mayores de 8 años
La dosis pediátrica habitual de MINOCIN es de 4 mg/kg inicialmente, seguida de 2 mg/kg cada 12 horas, sin exceder la dosis habitual para adultos.
Adultos
La dosis habitual de MINOCIN es de 200 mg inicialmente seguida de 100 mg cada 12 horas.
Para el tratamiento de la sífilis, la dosis habitual de MINOCIN debe administrarse durante un período de 10 a 15 días. Se recomienda un seguimiento estrecho, incluidas pruebas de laboratorio.
Los pacientes con gonorrea sensibles a la penicilina pueden tratarse con MINOCIN 50 mg, administrados inicialmente en dosis de 200 mg, seguidos de 100 mg cada 12 horas durante un mínimo de 4 días, con cultivos posteriores a la terapia dentro de los 2 a 3 días.
En el tratamiento del estado de portador meningocócico, la dosis recomendada es de 100 mg cada 12 horas durante 5 días.
Infecciones por Mycobacterium marinum: aunque no se han establecido las dosis óptimas, se han utilizado con éxito 100 mg cada 12 horas durante 6 a 8 semanas en un número limitado de casos.
Infección uretral, endocervical o rectal no complicada en adultos causada por Chlamydia trachomatis o Ureaplasma urealyticum: 100 mg por vía oral, cada 12 horas durante al menos 7 días.
En el tratamiento de la uretritis gonocócica no complicada en hombres, se recomiendan 100 mg dos veces al día por vía oral durante 5 días.
CÓMO SUMINISTRADO
MINOCIN (clorhidrato de minociclina) Suspensión oral contiene clorhidrato de minociclina equivalente a 50 mg de minociclina por cucharadita (5 ml). Conservado con propilparabeno 0,10% y butilparabeno 0,06% con Alcohol USP 5% v/v. Con sabor a natillas.
CDN 16781-473-60 - Botella 2 fl. Onz. (60 ml)
Almacenar a temperatura ambiente controlada de 20° a 25°C (68° a 77°F).
NO CONGELAR.
Fabricado para: Onset Dermatologics, LLC Cumberland, RI 02864. Revisado: noviembre de 2018
EFECTOS SECUNDARIOS
Debido a la absorción virtualmente completa de la minociclina oral, los efectos secundarios en la parte inferior del intestino, en particular la diarrea, han sido poco frecuentes. Se han observado las siguientes reacciones adversas en pacientes que reciben tetraciclinas.
Cuerpo en su conjunto: Fiebre y decoloración de las secreciones.
Gastrointestinal: Anorexia, náuseas, vómitos, diarrea, dispepsia, estomatitis, glositis, disfagia, hipoplasia del esmalte, enterocolitis, colitis pseudomembranosa, pancreatitis, lesiones inflamatorias (con sobrecrecimiento monilial) en las regiones oral y anogenital.
Genitourinario: Vulvovaginitis.
Toxicidad hepática: Hiperbilirrubinemia, colestasis hepática, aumento de las enzimas hepáticas, insuficiencia hepática mortal e ictericia. Se han notificado casos de hepatitis, incluida la hepatitis autoinmunitaria, e insuficiencia hepática (ver PRECAUCIONES ).

Piel: Alopecia, eritema nudoso, hiperpigmentación de las uñas, prurito, necrólisis epidérmica tóxica, vasculitis, erupción maculopapular y erupción eritematosa. Se ha informado dermatitis exfoliativa. Se han informado erupciones medicamentosas fijas, incluida la balanitis. Se han notificado eritema multiforme y síndrome de Stevens-Johnson. La fotosensibilidad se discutió anteriormente (ver ADVERTENCIAS ). Se ha informado pigmentación de la piel y las membranas mucosas.
Respiratorio: Tos, disnea, broncoespasmo, exacerbación del asma y neumonitis.
Toxicidad renal: Nefritis intersticial. Se han informado elevaciones en BUN y aparentemente están relacionadas con la dosis (ver ADVERTENCIAS ). Se ha informado insuficiencia renal aguda reversible.
Musculoesquelético: Artralgia, artritis, decoloración de los huesos, mialgia, rigidez articular e inflamación articular.
Reacciones hipersensibles: Se han notificado urticaria, edema angioneurótico, poliartralgia, anafilaxia/reacción anafilactoide (incluidos shock y muertes), púrpura anafilactoide, miocarditis, pericarditis, exacerbación del lupus eritematoso sistémico e infiltrados pulmonares con eosinofilia. También se ha informado un síndrome transitorio similar al lupus y reacciones similares a la enfermedad del suero.
Sangre: Se han informado agranulocitosis, anemia hemolítica, trombocitopenia, leucopenia, neutropenia, pancitopenia y eosinofilia.
Sistema nervioso central: Convulsiones, mareos, hipoestesia, parestesia, sedación y vértigo. Pseudotumor cerebri (hipertensión intracraneal benigna) en adultos y fontanelas abultadas en bebés (ver PRECAUCIONES - General ). También se ha informado dolor de cabeza.
Otro: Se ha informado cáncer de tiroides en el entorno posterior a la comercialización en asociación con productos de minociclina. Cuando la terapia con minociclina se administra durante períodos prolongados, se debe considerar el control de signos de cáncer de tiroides. Cuando se administran durante períodos prolongados, se ha informado que las tetraciclinas producen una decoloración microscópica marrón-negra de la glándula tiroides. Se han informado casos de función tiroidea anormal.
Decoloración de los dientes en niños menores de 8 años (ver ADVERTENCIAS ) y también en adultos.
Se ha informado decoloración de la cavidad oral (incluyendo lengua, labios y encías).
Se han informado tinnitus y disminución de la audición en pacientes tratados con MINOCIN (clorhidrato de minociclina).
Se han informado los siguientes síndromes. En algunos casos relacionados con estos síndromes, se ha informado la muerte. Al igual que con otras reacciones adversas graves, si se reconoce alguno de estos síndromes, el medicamento debe suspenderse inmediatamente:
Síndrome de hipersensibilidad que consiste en una reacción cutánea (como erupción cutánea o dermatitis exfoliativa), eosinofilia y uno o más de los siguientes: hepatitis, neumonitis, nefritis, miocarditis y pericarditis. Puede haber fiebre y linfadenopatía.
Síndrome similar al lupus que consiste en anticuerpos antinucleares positivos; artralgia, artritis, rigidez de las articulaciones o hinchazón de las articulaciones; y uno o más de los siguientes: fiebre, mialgia, hepatitis, erupción y vasculitis.
Síndrome similar a la enfermedad del suero que consiste en fiebre; urticaria o sarpullido; y artralgia, artritis, rigidez articular o inflamación articular y linfadenopatía. Puede haber eosinofilia.
Para informar SOSPECHAS DE REACCIONES ADVERSAS, comuníquese con Valeant Pharmaceuticals North America LLC al 1-800-321-4576 o con la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch.
INTERACCIONES CON LA DROGAS
Debido a que se ha demostrado que las tetraciclinas deprimen la actividad de la protrombina plasmática, los pacientes que reciben terapia anticoagulante pueden requerir un ajuste a la baja de su dosis de anticoagulante.
Dado que los fármacos bacteriostáticos pueden interferir con la acción bactericida de la penicilina, se recomienda evitar administrar fármacos del tipo de las tetraciclinas junto con la penicilina.
La absorción de tetraciclinas se ve afectada por los antiácidos que contienen aluminio, calcio o magnesio y las preparaciones que contienen hierro.
Se ha informado que el uso concomitante de tetraciclina y metoxiflurano produce toxicidad renal mortal.
El uso concomitante de tetraciclinas con anticonceptivos orales puede hacer que los anticonceptivos orales sean menos efectivos.
Debe evitarse la administración de isotretinoína poco antes, durante y poco después del tratamiento con minociclina. Cada fármaco por sí solo se ha asociado con pseudotumor cerebral (ver PRECAUCIONES ).
Mayor riesgo de ergotismo cuando los alcaloides del cornezuelo del centeno o sus derivados se administran con tetraciclinas.
ADVERTENCIAS
Desarrollo dental
La suspensión oral de MINOCIN, al igual que otros antibióticos de la clase de las tetraciclinas, puede causar daño fetal cuando se administra a una mujer embarazada. Si se usa cualquier tetraciclina durante el embarazo o si la paciente queda embarazada mientras toma estos medicamentos, se debe informar a la paciente sobre el peligro potencial para el feto. El uso de medicamentos de la clase de las tetraciclinas durante el desarrollo de los dientes (última mitad del embarazo, infancia y niñez hasta los 8 años) puede causar una decoloración permanente de los dientes (amarillo-gris-marrón).
Esta reacción adversa es más común durante el uso a largo plazo del fármaco, pero se ha observado después de cursos repetidos a corto plazo. También se ha informado hipoplasia del esmalte. Los medicamentos de tetraciclina, por lo tanto, no deben usarse durante el desarrollo de los dientes a menos que otros medicamentos probablemente no sean efectivos o estén contraindicados.
Desarrollo esquelético
Todas las tetraciclinas forman un complejo de calcio estable en cualquier tejido formador de hueso. Se ha observado una disminución en la tasa de crecimiento del peroné en bebés humanos prematuros que recibieron tetraciclina oral en dosis de 25 mg/kg cada seis horas. Se demostró que esta reacción es reversible cuando se suspende el fármaco.
Uso en el embarazo
Los resultados de los estudios en animales indican que las tetraciclinas atraviesan la placenta, se encuentran en los tejidos fetales y pueden tener efectos tóxicos en el feto en desarrollo (a menudo relacionados con el retraso del desarrollo esquelético). Se ha observado evidencia de embriotoxicidad en animales tratados al principio del embarazo. No se ha establecido la seguridad de MINOCIN para su uso durante el embarazo.
Reacción dermatológica
Se han notificado casos de erupción cutánea con eosinofilia y síntomas sistémicos (DRESS), incluidos casos mortales, con el uso de minociclina. Si se reconoce este síndrome, el fármaco debe suspenderse inmediatamente.
Acción Antianabólica
La acción antianabólica de las tetraciclinas puede provocar un aumento del BUN. Si bien esto no es un problema en aquellos con una función renal normal, en pacientes con una función significativamente alterada, los niveles séricos más altos de tetraciclina pueden provocar azotemia, hiperfosfatemia y acidosis. En tales condiciones, se recomienda monitorear la creatinina y el BUN, y la dosis diaria total no debe exceder los 200 mg en 24 horas (ver DOSIFICACIÓN Y ADMINISTRACIÓN ). Si existe insuficiencia renal, incluso las dosis orales o parenterales habituales pueden provocar una acumulación sistémica del fármaco y una posible toxicidad hepática.
fotosensibilidad
Se ha observado fotosensibilidad manifestada por una reacción de quemadura solar exagerada en algunas personas que toman tetraciclinas. Esto se ha informado con minociclina.
Efectos del sistema nervioso central
Se han informado efectos secundarios del sistema nervioso central que incluyen mareos, mareos o vértigo con la terapia con minociclina. Se debe advertir a los pacientes que experimentan estos síntomas sobre la conducción de vehículos o el uso de maquinaria peligrosa mientras reciben terapia con minociclina. Estos síntomas pueden desaparecer durante la terapia y generalmente desaparecen rápidamente cuando se suspende el medicamento.
Diarrea asociada a Clostridium difficile
Se ha informado diarrea asociada a Clostridium difficile (CDAD) con el uso de casi todos los agentes antibacterianos, incluido MINOCIN 50 mg, y puede variar en gravedad desde diarrea leve hasta colitis fatal. El tratamiento con agentes antibacterianos altera la flora normal del colon y conduce al crecimiento excesivo de C. difficile.
C. difficile produce toxinas A y B que contribuyen al desarrollo de CDAD. Las cepas de C. difficile productoras de hipertoxina causan mayor morbilidad y mortalidad, ya que estas infecciones pueden ser refractarias a la terapia antimicrobiana y pueden requerir colectomía. Se debe considerar CDAD en todos los pacientes que presenten diarrea después del uso de antibióticos. Es necesaria una cuidadosa historia clínica ya que se ha informado que la CDAD ocurre más de dos meses después de la administración de agentes antibacterianos.
Si se sospecha o se confirma CDAD, es posible que deba suspenderse el uso continuo de antibióticos no dirigidos contra C. difficile. Se debe instituir el manejo adecuado de líquidos y electrolitos, la suplementación con proteínas, el tratamiento con antibióticos de C. difficile y la evaluación quirúrgica según esté clínicamente indicado.
Hipersensibilidad al sulfito de sodio
La suspensión oral de MINOCIN contiene sulfito de sodio, un sulfito que puede causar reacciones de tipo alérgico, incluidos síntomas anafilácticos y episodios asmáticos potencialmente mortales o menos graves en ciertas personas susceptibles. La prevalencia general de la sensibilidad al sulfito en la población general es desconocida y probablemente baja. La sensibilidad al sulfito se observa con mayor frecuencia en personas asmáticas que en personas no asmáticas.
Hipertensión Intracraneal
La hipertensión intracraneal (IH, pseudotumor cerebri) se ha asociado con el uso de tetraciclinas, incluida MINOCIN. Las manifestaciones clínicas de la HI incluyen cefalea, visión borrosa, diplopía y pérdida de la visión; El papiledema se puede encontrar en la fundoscopia. Las mujeres en edad fértil que tienen sobrepeso o antecedentes de HI tienen mayor riesgo de desarrollar HI asociada a tetraciclina. Se debe evitar el uso concomitante de isotretinoína y MINOCIN porque también se sabe que la isotretinoína causa un pseudotumor cerebral.
Aunque la HI generalmente se resuelve después de la interrupción del tratamiento, existe la posibilidad de pérdida visual permanente. Si se desarrollan síntomas visuales durante el tratamiento, se justifica una evaluación oftalmológica inmediata. Dado que la presión intracraneal puede permanecer elevada durante semanas después de suspender el medicamento, los pacientes deben ser monitoreados hasta que se estabilicen.
PRECAUCIONES
General
Al igual que con otras preparaciones de antibióticos, el uso de este medicamento puede provocar un crecimiento excesivo de organismos no sensibles, incluidos los hongos. Si ocurre una sobreinfección, se debe suspender el antibiótico e instituir la terapia adecuada.
Se ha informado hepatotoxicidad con minociclina; por lo tanto, la minociclina debe usarse con precaución en pacientes con disfunción hepática y junto con otros fármacos hepatotóxicos.
La incisión y el drenaje u otros procedimientos quirúrgicos deben realizarse junto con la terapia con antibióticos cuando esté indicado.
Prescribir MINOCIN suspensión oral en ausencia de una infección bacteriana comprobada o fuertemente sospechada o una indicación profiláctica es poco probable que brinde beneficios al paciente y aumenta el riesgo de desarrollo de bacterias resistentes a los medicamentos.
Pruebas de laboratorio
Se deben realizar evaluaciones periódicas de laboratorio de los sistemas de órganos, incluidos hematopoyéticos, renales y hepáticos.
Todos los pacientes con gonorrea deben tener una prueba serológica para sífilis en el momento del diagnóstico. Los pacientes tratados con minociclina deben someterse a una prueba serológica de seguimiento para sífilis después de 3 meses.
Interacciones entre medicamentos y pruebas de laboratorio
Pueden producirse elevaciones falsas de los niveles de catecolaminas en la orina debido a la interferencia con la prueba de fluorescencia.
Carcinogénesis, Mutagénesis, Deterioro De La Fertilidad
La administración dietética de minociclina en estudios de tumorigenicidad a largo plazo en ratas resultó en evidencia de producción de tumores de tiroides. También se ha descubierto que la minociclina produce hiperplasia tiroidea en ratas y perros. Además, ha habido evidencia de actividad oncogénica en ratas en estudios con un antibiótico relacionado, oxitetraciclina (es decir, tumores suprarrenales y pituitarios). Asimismo, aunque no se han realizado estudios de mutagenicidad de la minociclina, se han informado resultados positivos en ensayos de células de mamíferos in vitro (es decir, linfoma de ratón y células de pulmón de hámster chino) para antibióticos relacionados (clorhidrato de tetraciclina y oxitetraciclina). Los estudios del segmento I (fertilidad y reproducción general) han proporcionado evidencia de que la minociclina altera la fertilidad en ratas macho.
El embarazo
Resumen de riesgos
Todos los embarazos tienen un riesgo de antecedentes de anomalías congénitas, pérdidas u otros resultados adversos, independientemente de la exposición al fármaco. No existen estudios adecuados y bien controlados sobre el uso de minociclina en mujeres embarazadas. La minociclina, al igual que otros antibióticos de la clase de las tetraciclinas, atraviesa la placenta y puede causar daño fetal cuando se administra a una mujer embarazada. En la experiencia posterior a la comercialización, se han notificado informes espontáneos raros de anomalías congénitas, incluida la reducción de extremidades. Solo hay información limitada disponible sobre estos informes; por lo tanto, no se puede establecer ninguna conclusión sobre la asociación causal. Si se usa minociclina durante el embarazo o si la paciente queda embarazada mientras toma este medicamento, se debe informar a la paciente sobre el peligro potencial para el feto.
Efectos no teratogénicos: (ver ADVERTENCIAS ).
Trabajo y entrega
Se desconoce el efecto de las tetraciclinas sobre el trabajo de parto y el parto.
Madres lactantes
Las tetraciclinas se excretan en la leche humana. Debido a la posibilidad de que las tetraciclinas produzcan reacciones adversas graves en los lactantes, se debe tomar la decisión de suspender la lactancia o suspender el fármaco, teniendo en cuenta la importancia del fármaco para la madre (ver ADVERTENCIAS ).
Uso pediátrico
No se recomienda el uso de minociclina en niños menores de 8 años a menos que los beneficios esperados de la terapia superen los riesgos (ver ADVERTENCIAS ).
Uso geriátrico
Los estudios clínicos de minociclina oral no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. En general, la selección de la dosis para un paciente anciano debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, lo que refleja la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedad concomitante u otra terapia con medicamentos (ver ADVERTENCIAS , DOSIFICACIÓN Y ADMINISTRACIÓN ).
La suspensión oral de 50 mg de MINOCIN contiene 4,3 mg (0,18 mEq) de sodio por 5 ml.
SOBREDOSIS
Los eventos adversos que se observan con más frecuencia en caso de sobredosis son mareos, náuseas y vómitos.
No se conoce un antídoto específico para la minociclina.
En caso de sobredosis, suspenda la medicación, trate sintomáticamente e instituya medidas de apoyo. La minociclina no se elimina en cantidades significativas por hemodiálisis o diálisis peritoneal.
CONTRAINDICACIONES
Este fármaco está contraindicado en personas que hayan mostrado hipersensibilidad a alguna de las tetraciclinas oa alguno de los componentes de la formulación del producto.
FARMACOLOGÍA CLÍNICA
Después de una dosis única de dos cápsulas llenas de polvo de minociclina HCl de 100 mg administrada a diez voluntarios adultos normales, los niveles séricos oscilaron entre 0,74 y 4,45 mcg/mL en 1 hora (promedio de 2,24); después de 12 horas oscilaron entre 0,34 y 2,36 mcg/mL (promedio 1,25). La semivida sérica después de una dosis única de 200 mg en 12 voluntarios esencialmente normales osciló entre 11 y 17 horas. En siete pacientes con disfunción hepática osciló entre 11 y 16 horas y en 5 pacientes con disfunción renal osciló entre 18 y 69 horas. La recuperación urinaria y fecal de la minociclina cuando se administró a 12 voluntarios normales fue de la mitad a un tercio de la de otras tetraciclinas.
Microbiología
Mecanismo de acción
Las tetraciclinas son principalmente bacteriostáticas y se cree que ejercen su efecto antimicrobiano mediante la inhibición de la síntesis de proteínas. Las tetraciclinas, incluida la minociclina, tienen un espectro de actividad antimicrobiano similar contra una amplia gama de organismos grampositivos y gramnegativos. La resistencia cruzada de estos organismos a la tetraciclina es común.
Actividad antimicrobiana
Se ha demostrado que la minociclina es activa contra la mayoría de las cepas de los siguientes microorganismos, tanto in vitro como en infecciones clínicas como se describe en el INDICACIONES sección:
bacterias grampositivas
Bacillus anthracis Listeria monocytogenes Staphylococcus aureus Streptococcus pneumoniae
Bacterias Gram-negativo
Bartonella bacilliformis Especies de Brucella Klebsiella granulomatis Campylobacter fetus Francisella tularensis Haemophilus ducreyi Vibrio cholerae Yersinia pestis Especies de Acinetobacter Enterobacter aerogenes Escherichia coli Haemophilus influenzae Especies de Klebsiella Neisseria gonorrhoeae Neisseria meningitidis Especies de Shigella
Otros microorganismos
Especies de Actinomyces Borrelia recurrentis Chlamydophila psittaci Chlamydia trachomatis Especies de Clostridium Especies de Entamoeba Fusobacterium nucleatum subespecie fusiforme Mycobacterium marinum Mycoplasma pneumoniae Propionibacterium acnes Rickettsiae Treponema pallidum subespecie pallidum Treponema pallidum subespecie pertenue Ureaplasma urealyticum
Pruebas de susceptibilidad
Para obtener información específica sobre los criterios de interpretación de las pruebas de susceptibilidad y los métodos de prueba asociados y los estándares de control de calidad reconocidos por la FDA para este medicamento, consulte: https://www.fda.gov/STIC.
Farmacología y Toxicología Animal
Se ha observado que la minociclina HCl causa una decoloración oscura de la tiroides en animales de experimentación (ratas, minicerdos, perros y monos). En la rata, el tratamiento crónico con clorhidrato de minociclina ha resultado en bocio acompañado de una captación elevada de yodo radiactivo y evidencia de producción de tumor tiroideo. También se ha descubierto que el clorhidrato de minociclina produce hiperplasia tiroidea en ratas y perros.
INFORMACIÓN DEL PACIENTE
La diarrea es un problema común causado por los antibióticos que generalmente termina cuando se suspende el antibiótico. A veces, después de comenzar el tratamiento con antibióticos, los pacientes pueden desarrollar heces acuosas y sanguinolentas (con o sin calambres estomacales y fiebre) incluso dos o más meses después de haber tomado la última dosis del antibiótico. Si esto ocurre, los pacientes deben comunicarse con su médico lo antes posible.
Se ha observado fotosensibilidad manifestada por una reacción de quemadura solar exagerada en algunas personas que toman tetraciclinas. Se debe advertir a los pacientes que puedan estar expuestos a la luz solar directa o a la luz ultravioleta que esta reacción puede ocurrir con medicamentos de tetraciclina, y se debe interrumpir el tratamiento ante la primera evidencia de eritema cutáneo. Esta reacción ha sido reportada con el uso de minociclina.
Se debe advertir a los pacientes que experimentan síntomas del sistema nervioso central sobre la conducción de vehículos o el uso de maquinaria peligrosa mientras reciben terapia con minociclina (ver ADVERTENCIAS ).
El uso concomitante de tetraciclina con anticonceptivos orales puede hacer que los anticonceptivos orales sean menos efectivos (ver INTERACCIONES CON LA DROGAS ).
Se debe advertir a los pacientes que los medicamentos antibacterianos, incluida la suspensión oral de 50 mg de MINOCIN, solo deben usarse para tratar infecciones bacterianas. No tratan infecciones virales (p. ej., el resfriado común). Cuando se prescribe MINOCIN Suspensión oral para tratar una infección bacteriana, se debe informar a los pacientes que, aunque es común que se sientan mejor al comienzo de la terapia, el medicamento debe tomarse exactamente como se indica. Omitir dosis o no completar el curso completo de la terapia puede (1) disminuir la eficacia del tratamiento inmediato y (2) aumentar la probabilidad de que las bacterias desarrollen resistencia y no sean tratables con MINOCIN 50 mg Suspensión oral u otros medicamentos antibacterianos en el futuro .
Los suministros no utilizados de antibióticos de tetraciclina deben desecharse antes de la fecha de vencimiento.
