Isoptin Sr 120mg, 240mg Uso, efectos secundarios, resistencia y dosis. Precio en farmacia online. Medicamentos genericos sin receta.
¿Qué es Isoptin y cómo se usa?
Isoptin es un medicamento recetado que se usa para tratar los síntomas del dolor de pecho (angina), la presión arterial alta (hipertensión) y ciertos trastornos del ritmo cardíaco. Isoptin puede usarse solo o con otros medicamentos.
- Isoptin pertenece a una clase de medicamentos llamados antiarrítmicos, IV; Bloqueadores de los canales de calcio; bloqueadores de los canales de calcio y no dihidropiridínicos.
- No se sabe si Isoptin es seguro y efectivo en niños menores de 1 año de edad.
¿Cuáles son los posibles efectos secundarios de Isoptin?
- Dolor de pecho,
- frecuencia cardíaca rápida o lenta,
- aturdimiento,
- dificultad para respirar,
- hinchazón,
- rápido aumento de peso,
- fiebre,
- dolor de estómago superior,
- no sentirse bien,
- ansiedad,
- transpiración,
- piel pálida,
- sibilancias,
- sin aliento, y
- tos con mucosidad espumosa
Obtenga ayuda médica de inmediato si tiene alguno de los síntomas mencionados anteriormente.
Los efectos secundarios más comunes de Isoptin incluyen:
- náuseas,
- estreñimiento,
- dolor de cabeza,
- mareos, y
- presión arterial baja
Informe al médico si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de Isoptin. Para obtener más información, consulte a su médico o farmacéutico.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
DESCRIPCIÓN
ISOPTIN® SR (clorhidrato de verapamilo) es un inhibidor del flujo de iones de calcio (bloqueador de canales lentos o antagonista de iones de calcio). ISOPTIN SR 240 mg está disponible para administración oral como comprimidos recubiertos con película, ranurados, con forma de cápsula, de color verde claro, que contienen 240 mg de clorhidrato de verapamilo, como comprimidos recubiertos con película, ranurados, de forma ovalada, de color rosa claro, que contienen 180 mg de clorhidrato de verapamilo, y como comprimidos recubiertos con película de color violeta claro. Comprimidos recubiertos con película de forma ovalada que contienen 120 mg de clorhidrato de verapamilo. Las tabletas están diseñadas para la liberación sostenida del fármaco en el tracto gastrointestinal, las características de liberación sostenida no se alteran cuando la tableta se divide por la mitad.
La fórmula estructural de verapamilo HCl se da a continuación.
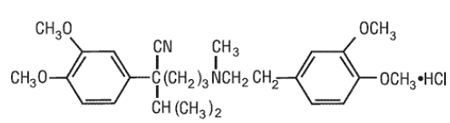 C27H38N2O4•HCl............. MW 491,08
C27H38N2O4•HCl............. MW 491,08 Bencenoacetronitrilo, clorhidrato de α [3-[[2-(3,4-dimetoxifenil) etil] metilamino] propil]-3,4dimetoxi-α-(1-metiletilo)
Verapamil HCl es un polvo cristalino casi blanco, prácticamente libre de olor, con un sabor amargo. Es soluble en agua, cloroformo y metanol. El clorhidrato de verapamilo no está químicamente relacionado con otros fármacos cardioactivos.
Además de verapamilo HCl, la tableta ISOPTIN SR 240 mg contiene los siguientes ingredientes: alginato, hipromelosa, estearato de magnesio, celulosa microcristalina, polietilenglicol, polivinilpirrolidona, talco y dióxido de titanio. Los siguientes son los aditivos de color por fuerza de tableta:
INDICACIONES
ISOPTIN SR (verapamil HCl) está indicado para el manejo de la hipertensión esencial.
DOSIFICACIÓN Y ADMINISTRACIÓN
Hipertensión esencial
La dosis de ISOPTIN SR 120 mg debe individualizarse por titulación y el fármaco debe administrarse con alimentos. Iniciar la terapia con 180 mg de clorhidrato de verapamilo de liberación sostenida, ISOPTIN SR, administrados por la mañana. Se pueden justificar dosis iniciales más bajas de 120 mg al día en pacientes que pueden tener una mayor respuesta al verapamilo (p. ej., ancianos o personas pequeñas, etc.). La titulación ascendente debe basarse en la eficacia y seguridad terapéuticas evaluadas semanalmente y aproximadamente 24 horas después de la dosis anterior. Los efectos antihipertensivos de ISOPTIN SR son evidentes dentro de la primera semana de tratamiento.
Si no se obtiene una respuesta adecuada con 180 mg de ISOPTIN SR 240 mg, se puede aumentar la dosis de la siguiente manera:
Al cambiar de ISOPTIN de liberación inmediata a ISOPTIN SR, la dosis diaria total en miligramos puede permanecer igual.
CÓMO SUMINISTRADO
ISOPTIN® SR 240 mg Los comprimidos se suministran como comprimidos recubiertos con película, ranurados, con forma de cápsula, de color verde claro, que contienen 240 mg de clorhidrato de verapamilo. La tableta está grabada con "pp" en un lado y "ST" en el otro lado. Los comprimidos de ISOPTIN® SR de 180 mg se suministran como comprimidos recubiertos con película ranurados, ovalados, de color rosa claro que contienen 180 mg de clorhidrato de verapamilo. La tableta está grabada con "pp" en un lado y "SK" en el otro lado. Los comprimidos de ISOPTIN® SR 120 mg se suministran en forma de comprimidos recubiertos con película de color violeta claro, de forma ovalada, que contienen 120 mg de clorhidrato de verapamilo. La tableta está grabada con una "p" en un lado y "SC" en el otro lado.
240 miligramos (verde claro)- Botella de 100- CDN # 10631-490-01 Botella de 500- CDN # 10631-490-05 180 miligramos (rosa claro)- Botella de 100- CDN # 10631-489-01 120 miligramos (violeta claro)- Botella de 100- CDN # 10631-488-01
Almacenamiento
Conservar a 25 °C (77 °F); excursiones permitidas a 15 °–30 °C (59 °– 86 °F) [ver Temperatura ambiente controlada por USP ].
Proteger de la luz y la humedad.
Dispense en un recipiente hermético resistente a la luz como se define en la USP.
Puede informar los efectos secundarios a la FDA en 1-800-FDA-1088.
Fabricado por: Halo Pharmaceutical Inc. Whippany, NJ 07981, EE. UU. Fabricado para: Ranbaxy Laboratories Inc. Jacksonville, FL 32257 EE. UU. octubre de 2011EFECTOS SECUNDARIOS
Las reacciones adversas graves son poco comunes cuando la terapia con verapamilo se inicia con una titulación ascendente de la dosis dentro de la dosis diaria única y total recomendada. Ver ADVERTENCIAS para la discusión de insuficiencia cardíaca, hipotensión, enzimas hepáticas elevadas, bloqueo AV y respuesta ventricular rápida. Se ha notificado con poca frecuencia íleo paralítico no obstructivo reversible (tras la suspensión del verapamilo) en asociación con el uso de verapamilo. Las siguientes reacciones al verapamilo administrado por vía oral ocurrieron en tasas superiores al 1,0 % o en tasas más bajas, pero aparecieron claramente relacionadas con el medicamento en ensayos clínicos en 4954 pacientes.
Enzimas hepáticas elevadas
(ver ADVERTENCIAS )
En ensayos clínicos relacionados con el control de la respuesta ventricular en pacientes digitalizados que tenían fibrilación auricular o aleteo auricular, se produjeron frecuencias ventriculares inferiores a 50 lpm en reposo en el 15 % de los pacientes y se produjo hipotensión asintomática en el 5 % de los pacientes.
Las siguientes reacciones, notificadas en el 1,0 % o menos de los pacientes, ocurrieron en condiciones (ensayos abiertos, experiencia de comercialización) en las que la relación causal es incierta; se enumeran para alertar al médico sobre una posible relación.
Cardiovascular: angina de pecho, disociación auriculoventricular, dolor torácico, claudicación, infarto de miocardio, palpitaciones, púrpura (vasculitis), síncope.
Sistema digestivo: diarrea, sequedad de boca, malestar gastrointestinal, hiperplasia gingival.
hemico y linfatico: equimosis o hematomas.
Sistema nervioso: accidente cerebrovascular, confusión, trastornos del equilibrio, insomnio, calambres musculares, parestesia, síntomas psicóticos, temblores, somnolencia, síntomas extrapiramidales.
Piel: artralgia y erupción cutánea, exantema, pérdida de cabello, hiperqueratosis, máculas, sudoración, urticaria, síndrome de Stevens-Johnson, eritema multiforme.
Sentidos especiales: visión borrosa, tinnitus.
urogenitales: ginecomastia, impotencia, galactorrea/hiperprolactinemia, aumento de la orina, menstruación irregular.
Tratamiento de reacciones adversas cardiovasculares agudas
La frecuencia de reacciones adversas cardiovasculares que requieren tratamiento es rara, por lo que la experiencia con su tratamiento es limitada. Siempre que ocurra hipotensión grave o bloqueo AV completo después de la administración oral de verapamilo, se deben aplicar las medidas de emergencia apropiadas de inmediato, por ejemplo, isoproterenol HCl administrado por vía intravenosa, bitartrato de norepinefrina, sulfato de atropina (todo en las dosis habituales) o gluconato de calcio (solución al 10%). ). En pacientes con miocardiopatía hipertrófica (IHSS), se deben usar agentes alfa-adrenérgicos (HCl de fenilefrina, bitartrato de metaraminol o HCl de metoxamina) para mantener la presión arterial, y se deben evitar el isoproterenol y la norepinefrina. Si se necesita apoyo adicional, se puede administrar (dopamina HCl o dobutamina HCl). El tratamiento y la dosis reales deben depender de la gravedad de la situación clínica y del juicio y experiencia del médico tratante.
INTERACCIONES CON LA DROGAS
Se han observado hipotensión y bradiarritmias en pacientes que reciben simultáneamente teletromicina, un antibiótico de la clase de antibióticos cetólidos.
Inhibidores de la HMG-CoA reductasa
El uso de inhibidores de la HMG-CoA reductasa que son sustratos de CYP3A4 en combinación con verapamilo se ha asociado con informes de miopatía/rabdomiólisis.
La coadministración de dosis múltiples de 10 mg de verapamilo con 80 mg de simvastatina resultó en una exposición a la simvastatina 2,5 veces mayor que la que siguió a la simvastatina sola. Limite la dosis de simvastatina en pacientes que toman verapamilo a 10 mg al día. Limite la dosis diaria de lovastatina a 40 mg. Es posible que se requieran dosis iniciales y de mantenimiento más bajas de otros sustratos de CYP3A4 (p. ej., atorvastatina), ya que el verapamilo puede aumentar la concentración plasmática de estos fármacos.
clonidina
Se ha informado bradicardia sinusal que resultó en hospitalización e inserción de marcapasos en asociación con el uso de clonidina junto con verapamilo. Vigile la frecuencia cardíaca en pacientes que reciben verapamilo y clonidina de forma concomitante.
Inductores/inhibidores de citocromos
Estudios metabólicos in vitro indican que el verapamilo es metabolizado por el citocromo P450 CYP3A4, CYP1A2, CYP2C8, CYP2C9 y CYP2C18. Se han notificado interacciones clínicamente significativas con inhibidores de CYP3A4 (p. ej., eritromicina, ritonavir) que provocan una elevación de los niveles plasmáticos de verapamilo, mientras que los inductores de CYP3A4 (p. ej., rifampicina) han provocado una disminución de los niveles plasmáticos de verapamilo, por lo que se debe controlar a los pacientes para detectar interacciones farmacológicas. .
Aspirina
En unos pocos casos informados, la coadministración de verapamilo con aspirina ha llevado a un aumento del tiempo de sangrado mayor que el observado con aspirina sola.
Jugo de uva
La ingesta de jugo de toronja puede aumentar los niveles del fármaco de verapamilo.
Bloqueadores beta
La terapia concomitante con bloqueadores beta-adrenérgicos y verapamilo puede resultar en efectos negativos aditivos sobre la frecuencia cardíaca, la conducción auriculoventricular y/o la contractilidad cardíaca. No se ha estudiado la combinación de verapamilo de liberación sostenida y agentes bloqueadores beta-adrenérgicos. Sin embargo, ha habido informes de bradicardia excesiva y bloqueo AV, incluido bloqueo cardíaco completo, cuando la combinación se ha utilizado para el tratamiento de la hipertensión. Para los pacientes hipertensos, los riesgos de la terapia combinada pueden superar los beneficios potenciales. La combinación debe usarse solo con precaución y una estrecha vigilancia.
Se ha observado bradicardia asintomática (36 latidos/min) con un marcapasos auricular errante en un paciente que recibe colirios de timolol (un bloqueador beta-adrenérgico) concomitantemente y verapamilo oral.
Se ha observado una disminución en el aclaramiento de metoprolol y propranolol cuando cualquiera de los fármacos se administra concomitantemente con verapamilo. Se ha observado un efecto variable cuando se administran juntos verapamilo y atenolol.
Digital
El uso clínico de verapamilo en pacientes digitalizados ha demostrado que la combinación es bien tolerada si las dosis de digoxina se ajustan adecuadamente. El tratamiento crónico con verapamilo puede aumentar los niveles séricos de digoxina entre un 50 y un 75 % durante la primera semana de tratamiento, y esto puede provocar toxicidad digitálica. En pacientes con cirrosis hepática, se magnifica la influencia del verapamilo sobre la cinética de la digoxina. El verapamilo puede reducir el aclaramiento corporal total y el aclaramiento extrarrenal de digitoxina en un 27 % y un 29 %, respectivamente. Las dosis de mantenimiento y digitalización deben reducirse cuando se administra verapamilo, y el paciente debe ser monitoreado cuidadosamente para evitar la digitalización excesiva o insuficiente. Siempre que se sospeche sobredigitalización, la dosis diaria de digitálicos debe reducirse o suspenderse temporalmente. Tras la interrupción de ISOPTIN (verapamilo HCl), el paciente debe ser reevaluado para evitar la subdigitalización.
Agentes antihipertensivos
El verapamilo administrado concomitantemente con agentes antihipertensivos orales (p. ej., vasodilatadores, inhibidores de la enzima convertidora de angiotensina, diuréticos, bloqueadores beta) generalmente tendrá un efecto aditivo en la reducción de la presión arterial. Los pacientes que reciben estas combinaciones deben ser controlados adecuadamente. El uso concomitante de agentes que atenúan la función alfa-adrenérgica con verapamilo puede resultar en una reducción excesiva de la presión arterial en algunos pacientes. Tal efecto se observó en un estudio luego de la administración concomitante de verapamilo y prazosin.
Agentes antiarrítmicos
disopiramida
Hasta que se obtengan datos sobre las posibles interacciones entre el verapamilo y el fosfato de disopiramida, la disopiramida no debe administrarse dentro de las 48 horas anteriores o las 24 horas posteriores a la administración de verapamilo.
flecainida
Un estudio de voluntarios sanos mostró que la administración concomitante de flecainida y verapamilo puede tener efectos aditivos sobre la contractilidad miocárdica, la conducción AV y la repolarización. El tratamiento concomitante con flecainida y verapamilo puede provocar un efecto inotrópico negativo aditivo y una prolongación de la conducción auriculoventricular.
quinidina
En un pequeño número de pacientes con miocardiopatía hipertrófica (IHSS), el uso concomitante de verapamilo y quinidina resultó en hipotensión significativa. Hasta que se obtengan más datos, probablemente se deba evitar la terapia combinada de verapamilo y quinidina en pacientes con miocardiopatía hipertrófica.
Los efectos electrofisiológicos de la quinidina y el verapamilo sobre la conducción AV se estudiaron en 8 pacientes. El verapamilo contrarrestó significativamente los efectos de la quinidina sobre la conducción AV. Ha habido un informe de niveles elevados de quinidina durante la terapia con verapamilo.
nitratos
El verapamilo se ha administrado concomitantemente con nitratos de acción corta y prolongada sin interacciones farmacológicas indeseables. El perfil farmacológico de ambos fármacos y la experiencia clínica sugieren interacciones beneficiosas.
Otro
Alcohol
Se ha descubierto que el verapamilo inhibe significativamente la eliminación de etanol, lo que da como resultado concentraciones elevadas de etanol en la sangre que pueden prolongar los efectos intoxicantes del alcohol. (Ver FARMACOLOGÍA CLÍNICA , Farmacocinética y Metabolismo ).

cimetidina
No se ha estudiado la interacción entre cimetidina y verapamilo administrado crónicamente. Se han obtenido resultados variables sobre el aclaramiento en estudios agudos de voluntarios sanos; el aclaramiento de verapamilo se redujo o no cambió.
Litio
Se ha notificado una mayor sensibilidad a los efectos del litio (neurotoxicidad) durante el tratamiento concomitante con verapamilo y litio; Se ha observado que los niveles de litio a veces aumentan, a veces disminuyen y, a veces, no cambian. Los pacientes que reciben ambos medicamentos deben ser monitoreados cuidadosamente.
Carbamazepina
El verapamilo puede aumentar las concentraciones de carbamazepina durante la terapia combinada. Esto puede producir efectos secundarios de carbamazepina como diplopía, dolor de cabeza, ataxia o mareos.
rifampicina
La terapia con rifampicina puede reducir notablemente la biodisponibilidad del verapamilo oral.
fenobarbital
La terapia con fenobarbital puede aumentar la eliminación de verapamilo.
ciclosporina
La terapia con verapamilo puede aumentar los niveles séricos de ciclosporina.
teofilina
La terapia con verapamilo puede inhibir el aclaramiento y aumentar los niveles plasmáticos de teofilina.
Anestésicos de inhalación
Los experimentos con animales han demostrado que los anestésicos por inhalación deprimen la actividad cardiovascular al disminuir el movimiento hacia el interior de los iones de calcio. Cuando se usan concomitantemente, los anestésicos inhalatorios y los antagonistas del calcio, como el verapamilo, deben titularse cuidadosamente para evitar una depresión cardiovascular excesiva.
Agentes bloqueantes neuromusculares
Los datos clínicos y los estudios en animales sugieren que el verapamilo puede potenciar la actividad de los agentes bloqueantes neuromusculares (tipo curare y despolarizantes). Puede ser necesario disminuir la dosis de verapamilo y/o la dosis del bloqueante neuromuscular cuando los medicamentos se usan concomitantemente.
ADVERTENCIAS
Insuficiencia cardiaca
El verapamilo tiene un efecto inotrópico negativo que, en la mayoría de los pacientes, se compensa con sus propiedades de reducción de la poscarga (disminución de la resistencia vascular sistémica) sin un deterioro neto del rendimiento ventricular. En la experiencia clínica con 4.954 pacientes, 87 (1,8 %) desarrollaron insuficiencia cardíaca congestiva o edema pulmonar. Se debe evitar el verapamilo en pacientes con disfunción ventricular izquierda grave (p. ej., fracción de eyección inferior al 30 % o síntomas de insuficiencia cardíaca de moderados a graves) y en pacientes con cualquier grado de disfunción ventricular si están recibiendo un bloqueador beta adrenérgico (ver INTERACCIONES CON LA DROGAS ). Los pacientes con disfunción ventricular más leve deben, si es posible, ser controlados con dosis óptimas de digitálicos y/o diuréticos antes del tratamiento con verapamilo (Observe las interacciones con digoxina en: PRECAUCIONES).
Hipotensión
Ocasionalmente, la acción farmacológica del verapamilo puede producir una disminución de la presión arterial por debajo de los niveles normales, lo que puede provocar mareos o hipotensión sintomática. La incidencia de hipotensión observada en 4.954 pacientes inscritos en ensayos clínicos fue del 2,5 %. En pacientes hipertensos, las disminuciones de la presión arterial por debajo de lo normal son inusuales. La prueba de mesa basculante (60 grados) no pudo inducir hipotensión ortostática.
Enzimas hepáticas elevadas
Se han informado elevaciones de transaminasas con y sin elevaciones concomitantes de fosfatasa alcalina y bilirrubina. Estas elevaciones a veces han sido transitorias y pueden desaparecer incluso ante la continuación del tratamiento con verapamilo. Se han probado varios casos de daño hepatocelular relacionado con el verapamilo por reexposición; la mitad de estos tenían síntomas clínicos (malestar general, fiebre y/o dolor en el cuadrante superior derecho) además de elevaciones de SGOT, SGPT y fosfatasa alcalina. Por lo tanto, es prudente el control periódico de la función hepática en pacientes que reciben verapamilo.
Vía de derivación accesoria (Wolff-Parkinson-White o Lown-Ganong-Levine)
Algunos pacientes con fibrilación auricular paroxística y/o crónica o aleteo auricular y una vía AV accesoria coexistente han desarrollado un aumento de la conducción anterógrada a través de la vía accesoria sin pasar por el nódulo AV, produciendo una respuesta ventricular muy rápida o fibrilación ventricular después de recibir verapamilo intravenoso (o digitálicos). . Aunque no se ha establecido el riesgo de que esto ocurra con verapamilo oral, los pacientes que reciben verapamilo oral pueden estar en riesgo y su uso en estos pacientes está contraindicado (ver CONTRAINDICACIONES ). El tratamiento suele ser DC-cardioversión. La cardioversión se ha utilizado de forma segura y eficaz después de ISOPTIN oral.
Bloqueo auriculoventricular
El efecto del verapamilo sobre la conducción AV y el nódulo SA puede causar bloqueo AV de primer grado asintomático y bradicardia transitoria, a veces acompañada de ritmos de escape nodal. La prolongación del intervalo PR se correlaciona con las concentraciones plasmáticas de verapamilo, especialmente durante las primeras fases de titulación de la terapia. Sin embargo, se observaron con poca frecuencia (0,8 %) grados más altos de bloqueo AV. El bloqueo marcado de primer grado o el desarrollo progresivo a un bloqueo AV de segundo o tercer grado requiere una reducción de la dosis o, en raras ocasiones, la interrupción del verapamilo HCI y la institución de la terapia adecuada según la situación clínica.
Pacientes con Miocardiopatía Hipertrófica (IHSS)
En 120 pacientes con miocardiopatía hipertrófica (la mayoría de ellos refractarios o intolerantes al propranolol) que recibieron terapia con verapamilo a dosis de hasta 720 mg/día, se observaron diversos efectos adversos graves. Tres pacientes fallecieron por edema pulmonar; todos tenían obstrucción grave del flujo de salida del ventrículo izquierdo y antecedentes de disfunción ventricular izquierda. Otros ocho pacientes tenían edema pulmonar y/o hipotensión grave; En la mayoría de estos pacientes se presentó una presión de enclavamiento pulmonar anormalmente alta (más de 20 mmHg) y una marcada obstrucción del flujo de salida del ventrículo izquierdo. La administración concomitante de quinidina (ver INTERACCIONES CON LA DROGAS precedió a la hipotensión severa en 3 de los 8 pacientes (2 de los cuales desarrollaron edema pulmonar). Se produjo bradicardia sinusal en el 11 % de los pacientes, bloqueo AV de segundo grado en el 4 % y paro sinusal en el 2 %. Debe apreciarse que este grupo de pacientes tenía una enfermedad grave con una alta tasa de mortalidad. La mayoría de los efectos adversos respondieron bien a la reducción de la dosis y solo en raras ocasiones hubo que suspender el verapamilo.
PRECAUCIONES
General
Uso en pacientes con funciones hepáticas alteradas
Dado que el verapamilo es altamente metabolizado por el hígado, debe administrarse con precaución a pacientes con insuficiencia hepática. La disfunción hepática grave prolonga la vida media de eliminación del verapamilo de liberación inmediata a alrededor de 14 a 16 horas; por lo tanto, se debe administrar a estos pacientes aproximadamente el 30% de la dosis administrada a pacientes con función hepática normal. Vigilancia cuidadosa de la prolongación anormal del intervalo PR u otros signos de efectos farmacológicos excesivos (ver SOBREDOSIS ) debería ser llevado a cabo.
Uso en pacientes con transmisión neuromuscular atenuada (disminuida)
Se ha informado que el verapamilo disminuye la transmisión neuromuscular en pacientes con distrofia muscular de Duchenne, prolonga la recuperación del bloqueante neuromuscular vecuronio y provoca un empeoramiento de la miastenia grave. Puede ser necesario disminuir la dosis de verapamilo cuando se administra a pacientes con transmisión neuromuscular atenuada.
Uso en pacientes con insuficiencia renal
Alrededor del 70% de una dosis administrada de verapamilo se excreta como metabolitos en la orina. El verapamilo no se elimina por hemodiálisis. Hasta que se disponga de más datos, el verapamilo debe administrarse con precaución a pacientes con función renal alterada. Estos pacientes deben ser monitoreados cuidadosamente para detectar una prolongación anormal del intervalo PR u otros signos de sobredosis (ver SOBREDOSIS ).
Carcinogénesis, mutagénesis, deterioro de la fertilidad
Un estudio de toxicidad de 18 meses en ratas, a un múltiplo bajo (6 veces) de la dosis máxima recomendada en humanos, y no la dosis máxima tolerada, no sugirió un potencial tumorigénico. No hubo evidencia de un potencial carcinogénico de verapamilo administrado en la dieta de ratas durante dos años en dosis de 10, 35 y 120 mg/kg por día o aproximadamente 1x, 3.5x y 12x, respectivamente, el máximo diario humano recomendado. dosis (480 mg por día o 9,6 mg/kg/día).
Verapamilo no fue mutagénico en la prueba de Ames en 5 cepas de prueba a 3 mg por placa, con o sin activación metabólica.
Los estudios en ratas hembra con dosis dietéticas diarias de hasta 5,5 veces (55 mg/kg/día) la dosis máxima recomendada en humanos no mostraron alteración de la fertilidad. No se han determinado los efectos sobre la fertilidad masculina.
El embarazo
Embarazo Categoría C Se han realizado estudios de reproducción en conejos y ratas con dosis orales de hasta 1,5 (15 mg/kg/día) y 6 (60 mg/kg/día) veces la dosis diaria oral en humanos, respectivamente, y no han revelado evidencia de teratogenicidad. En la rata, sin embargo, este múltiplo de la dosis humana fue embriocida y retardó el crecimiento y desarrollo fetal, probablemente debido a los efectos maternos adversos reflejados en la reducción del aumento de peso de las madres. También se ha demostrado que esta dosis oral causa hipotensión en ratas. No existen estudios adecuados y bien controlados en mujeres embarazadas. Debido a que los estudios de reproducción en animales no siempre predicen la respuesta humana, este medicamento debe usarse durante el embarazo solo si es claramente necesario. El verapamilo atraviesa la barrera placentaria y puede detectarse en la sangre de la vena umbilical en el momento del parto.
Trabajo y entrega
No se sabe si el uso de verapamilo durante el trabajo de parto o el parto tiene efectos adversos inmediatos o tardíos en el feto, o si prolonga la duración del trabajo de parto o aumenta la necesidad de parto con fórceps u otra intervención obstétrica. Tales experiencias adversas no se han informado en la literatura, a pesar de una larga historia de uso de verapamilo en Europa en el tratamiento de los efectos secundarios cardíacos de los agentes agonistas beta-adrenérgicos utilizados para tratar el trabajo de parto prematuro.
Madres lactantes
El verapamilo se excreta en la leche humana. Debido al potencial de reacciones adversas en lactantes por verapamilo, se debe interrumpir la lactancia mientras se administra verapamilo.
Uso pediátrico
No se ha establecido la seguridad y eficacia de los comprimidos de ISOPTIN en pacientes pediátricos menores de 18 años.
SOBREDOSIS
La sobredosis de verapamilo puede provocar hipotensión pronunciada, bradicardia y anomalías del sistema de conducción (p. ej., ritmo de la unión con disociación AV y bloqueo AV de alto grado, incluida la asistolia). Pueden ser evidentes otros síntomas secundarios a la hipoperfusión (p. ej., acidosis metabólica, hiperglucemia, hiperpotasemia, disfunción renal y convulsiones).
Tratar todas las sobredosis de verapamilo como graves y mantener en observación durante al menos 48 horas [especialmente ISOPTIN® SR (clorhidrato de verapamilo)] preferiblemente bajo atención hospitalaria continua. Pueden ocurrir consecuencias farmacodinámicas retardadas con la formulación de liberación sostenida. Se sabe que el verapamilo disminuye el tiempo de tránsito gastrointestinal.
En caso de sobredosis, se ha informado ocasionalmente que comprimidos de ISOPTIN SR 240 mg forman concreciones en el estómago o los intestinos. Estas concreciones no han sido visibles en las radiografías simples del abdomen, y ningún medio médico de vaciamiento gastrointestinal tiene eficacia comprobada para eliminarlas. La endoscopia podría considerarse razonablemente en casos de sobredosis masiva cuando los síntomas son inusualmente prolongados.
El tratamiento de la sobredosis debe ser de apoyo. La estimulación betaadrenérgica o la administración parenteral de soluciones de calcio pueden aumentar el flujo de iones de calcio a través del canal lento y se han utilizado eficazmente en el tratamiento de la sobredosis deliberada de verapamilo. El tratamiento continuado con grandes dosis de calcio puede producir una respuesta. En unos pocos casos informados, la sobredosis con bloqueadores de los canales de calcio que inicialmente era refractaria a la atropina respondía mejor a este tratamiento cuando los pacientes recibían dosis altas (cerca de 1 gramo/hora durante más de 24 horas) de cloruro de calcio. El verapamilo no se puede eliminar por hemodiálisis. Las reacciones hipotensivas clínicamente significativas o el bloqueo AV de alto grado deben tratarse con agentes vasopresores o marcapasos cardíaco, respectivamente. La asistolia debe manejarse con las medidas habituales, incluida la reanimación cardiopulmonar.
CONTRAINDICACIONES
El clorhidrato de verapamilo está contraindicado en:
FARMACOLOGÍA CLÍNICA
ISOPTIN (HCl de verapamilo) es un inhibidor de la entrada de iones de calcio (bloqueador de canales lentos o antagonista de los iones de calcio) que ejerce sus efectos farmacológicos al modular la entrada de calcio iónico a través de la membrana celular del músculo liso arterial, así como en las células miocárdicas conductivas y contráctiles. .
Mecanismo de acción
Hipertensión esencial
ISOPTIN ejerce efectos antihipertensivos al disminuir la resistencia vascular sistémica, generalmente sin disminuciones ortostáticas en la presión arterial o taquicardia refleja; la bradicardia (frecuencia inferior a 50 latidos/min) es poco frecuente (1,4%). Durante el ejercicio isométrico o dinámico, ISOPTIN no altera la función cardíaca sistólica en pacientes con función ventricular normal. ISOPTIN no altera los niveles de calcio sérico total. Sin embargo, un informe sugirió que los niveles de calcio por encima del rango normal pueden alterar el efecto terapéutico de ISOPTIN.
Otras acciones farmacológicas de ISOPTIN incluyen las siguientes
ISOPTIN (HCl de verapamilo) dilata las principales arterias coronarias y las arteriolas coronarias, tanto en regiones normales como isquémicas, y es un potente inhibidor del espasmo de las arterias coronarias, ya sea espontáneo o inducido por ergonovina. Esta propiedad aumenta el suministro de oxígeno al miocardio en pacientes con espasmo de la arteria coronaria y es responsable de la eficacia de ISOPTIN en la angina vasoespástica (de Prinzmetal o variante), así como en la angina inestable en reposo. No está claro si este efecto juega algún papel en la angina de esfuerzo clásica, pero los estudios de tolerancia al ejercicio no han mostrado un aumento en el producto máximo de frecuencia de ejercicio-presión, una medida ampliamente aceptada de utilización de oxígeno. Esto sugiere que, en general, el alivio del espasmo o la dilatación de las arterias coronarias no es un factor importante en la angina clásica.
ISOPTIN reduce regularmente la resistencia sistémica total (poscarga) contra la que trabaja el corazón tanto en reposo como en un nivel determinado de ejercicio al dilatar las arteriolas periféricas.
La actividad eléctrica a través del nódulo AV depende, en gran medida, de la entrada de calcio a través del canal lento. Al disminuir la entrada de calcio, ISOPTIN prolonga el período refractario efectivo dentro del nódulo AV y ralentiza la conducción AV de manera relacionada con la frecuencia.
El ritmo sinusal normal generalmente no se ve afectado, pero en pacientes con síndrome del seno enfermo, ISOPTIN puede interferir con la generación de impulsos del nódulo sinusal y puede inducir un paro sinusal o un bloqueo sinoauricular. El bloqueo auriculoventricular puede ocurrir en pacientes sin defectos de conducción preexistentes (ver ADVERTENCIAS ).
ISOPTIN no altera el potencial de acción auricular normal ni el tiempo de conducción intraventricular, pero reduce la amplitud, la velocidad de despolarización y la conducción en las fibras auriculares deprimidas. ISOPTIN puede acortar el período refractario efectivo anterógrado de las vías accesorias de derivación. Se ha notificado aceleración de la frecuencia ventricular y/o fibrilación ventricular en pacientes con aleteo auricular o fibrilación auricular y una vía AV accesoria coexistente después de la administración de verapamilo (ver ADVERTENCIAS ).
ISOPTIN tiene una acción anestésica local 1,6 veces mayor que la de la procaína en base equimolar. No se sabe si esta acción es importante a las dosis utilizadas en el hombre.
Farmacocinética y Metabolismo
Con la formulación de liberación inmediata, se absorbe más del 90 % de la dosis de ISOPTIN administrada por vía oral. Debido a la rápida biotransformación del verapamilo durante su primer paso por la circulación portal, la biodisponibilidad oscila entre el 20 % y el 35 %. Las concentraciones plasmáticas máximas se alcanzan entre 1 y 2 horas después de la administración oral. La administración oral crónica de 120 mg de ISOPTIN cada 6 horas resultó en niveles plasmáticos de verapamilo que oscilaron entre 125 y 400 ng/mL, con valores más altos informados ocasionalmente. Existe una correlación no lineal entre la dosis de verapamilo administrada y los niveles plasmáticos de verapamilo.
En la titulación temprana de la dosis con verapamilo existe una relación entre las concentraciones plasmáticas de verapamilo y la prolongación del intervalo PR. Sin embargo, durante la administración crónica esta relación puede desaparecer. La semivida de eliminación media en los estudios de dosis única osciló entre 2,8 y 7,4 horas. En estos mismos estudios, después de dosis repetidas, la vida media aumentó a un rango de 4,5 a 12,0 horas (después de menos de 10 dosis consecutivas administradas con 6 horas de diferencia). La vida media del verapamilo puede aumentar durante la titulación. No se ha establecido relación entre la concentración plasmática de verapamilo y una reducción de la presión arterial.
El envejecimiento puede afectar la farmacocinética del verapamilo. La semivida de eliminación puede prolongarse en los ancianos.
En estudios de dosis múltiples en ayunas, la biodisponibilidad medida por el AUC de ISOPTIN SR 240 mg fue similar a la de ISOPTIN de liberación inmediata; las tasas de absorción eran, por supuesto, diferentes. En un estudio cruzado, aleatorizado, de dosis única, con voluntarios sanos, la administración de 240 mg de ISOPTIN SR con alimentos produjo concentraciones plasmáticas máximas de verapamilo de 79 ng/ml, tiempo hasta la concentración plasmática máxima de verapamilo de 7,71 horas y AUC (0-24 horas). ) de 841 ng-hr/mL. Cuando se administró ISOPTIN SR a sujetos en ayunas, la concentración plasmática máxima de verapamilo fue de 164 ng/mL; el tiempo hasta la concentración máxima de verapamilo en plasma fue de 5,21 horas; y el AUC (0-24 h) fue de 1478 ng-h/mL. Se demostraron resultados similares para el norverapamilo en plasma. Por lo tanto, los alimentos producen una disminución de la biodisponibilidad (AUC) pero una relación pico a valle más estrecha. No se dispone de una buena correlación entre la dosis y la respuesta, pero los estudios controlados de ISOPTIN SR 120 mg han demostrado la eficacia de dosis similares a las dosis efectivas de ISOPTIN (liberación inmediata).
En el hombre sano, ISOPTIN administrado por vía oral sufre un extenso metabolismo en el hígado. Se han identificado doce metabolitos en plasma; todos, excepto el norverapamilo, están presentes solo en cantidades mínimas. El norverapamilo puede alcanzar concentraciones plasmáticas en estado estacionario aproximadamente iguales a las del propio verapamilo. La actividad cardiovascular del norverapamilo parece ser aproximadamente el 20% de la del verapamilo. Aproximadamente el 70 % de una dosis administrada se excreta como metabolitos en la orina y el 16 % o más en las heces en 5 días. Alrededor del 3% al 4% se excreta en la orina como fármaco inalterado. Aproximadamente el 90% se une a las proteínas plasmáticas. En pacientes con insuficiencia hepática, el metabolismo del verapamilo de liberación inmediata se retrasa y la vida media de eliminación se prolonga hasta 14 a 16 horas (ver PRECAUCIONES ); el volumen de distribución aumenta y el aclaramiento plasmático se reduce a alrededor del 30% de lo normal. Los valores de depuración de verapamilo sugieren que los pacientes con disfunción hepática pueden alcanzar concentraciones plasmáticas terapéuticas de verapamilo con un tercio de la dosis oral diaria requerida para pacientes con función hepática normal.
Después de cuatro semanas de dosificación oral (120 mg qid), se observaron niveles de verapamilo y norverapamilo en el líquido cefalorraquídeo con un coeficiente de partición estimado de 0,06 para verapamilo y 0,04 para norverapamilo.
En diez hombres sanos, la administración de verapamilo oral (80 mg cada 8 horas durante 6 días) y una dosis oral única de etanol (0,8 g/kg) resultó en un aumento del 17 % en las concentraciones máximas medias de etanol (106,45 ± 21,40 a 124,23 ± 24,74 mg•h/dL) en comparación con el placebo. El área bajo la curva de concentración de etanol en sangre versus tiempo (AUC durante 12 horas) aumentó un 30 % (365,67 ± 93,52 a 475,07 ± 97,24 mg•h/dL). Las AUC de verapamilo se correlacionaron positivamente (r = 0,71) con valores aumentados de AUC en sangre de etanol. (Ver PRECAUCIONES : INTERACCIONES CON LA DROGAS .)
Hemodinamia y Metabolismo Miocárdico
ISOPTIN reduce la poscarga y la contractilidad miocárdica. También se ha observado una función diastólica del ventrículo izquierdo mejorada en pacientes con IHSS y aquellos con enfermedad cardíaca coronaria con la terapia con ISOPTIN. En la mayoría de los pacientes, incluidos aquellos con enfermedad cardíaca orgánica, la acción inotrópica negativa de ISOPTIN se contrarresta con la reducción de la poscarga y el índice cardíaco generalmente no se reduce. Sin embargo, en pacientes con disfunción ventricular izquierda grave (p. ej., presión de enclavamiento pulmonar superior a 20 mmHg o fracción de eyección inferior al 30%), o en pacientes que toman bloqueadores beta-adrenérgicos u otros fármacos cardiodepresores, puede producirse un deterioro de la función ventricular (ver INTERACCIONES CON LA DROGAS ).
Función pulmonar
ISOPTIN no induce broncoconstricción y, por lo tanto, no altera la función ventilatoria.
Farmacología Animal y/o Toxicología Animal
En estudios de toxicología crónica en animales, el verapamilo causó cambios lenticulares y/o en la línea de sutura a 30 mg/kg/día o más y cataratas francas a 62,5 mg/kg/día o más en el perro beagle pero no en la rata. No se ha informado desarrollo de cataratas debido al verapamilo en humanos.
INFORMACIÓN DEL PACIENTE
No se proporcionó información. por favor refiérase a ADVERTENCIAS y PRECAUCIONES secciones.
